Азитромицин убивает кишечную палочку
В развитии острых или хронических воспалений кишечника у детей и взрослых играют роль бактерии (сальмонелла, возбудители дизентерии, холеры), токсины бактерий (ботулизм) и вирусы (ротавирус, энтеровирус). Также микробная инфекция может присоединяться в связи с другими нарушениями работы желудочно-кишечного тракта и хроническими заболеваниями кишечника.
Острые кишечные инфекции могут протекать в легкой форме. Тогда лечение проводится в домашних условиях. Однако тяжелые инфекции требуют серьезной терапии в стационаре, чтобы предупредить осложнения.
Для лечения воспалительных заболеваний нижних отделов желудочно-кишечного тракта используются противомикробные средства, которые создают высокую концентрацию активного вещества в кишечнике. Они относятся к группе «невсасывающихся», поскольку практически не всасываются в системный кровоток и обеспечивают активное действие локально.
Содержание
Показания для противомикробных препаратов в гастроэнтерологии
Заболевания кишечника, которые требуют противомикробной терапии
Особенности кишечных противомикробных средств
Кишечные антисептики
Нитрофураны
Кишечные антибиотики
Фторхинолоны
Макролиды
Хлорамфеникол
Сульфаниламиды
Рифаксимин
Лечение Helicobacter pylori
Противогрибковые препараты
Противопаразитарные препараты
Метронидазол
Противовирусные препараты
Советы при выборе противомикробного средства

Показания для противомикробных препаратов в гастроэнтерологии
Показания для приема противомикробных медикаментов в гастроэнтерологии последние годы существенно расширились. Это произошло после того, как была изучена и доказана роль микроорганизмов в развитии заболеваний ЖКТ, которые раньше не считались инфекционными.
Основные ситуации, когда требуется назначение противомикробных средств, можно разделить на три категории:
- Инфекционные болезни. Диареи бактериального происхождения, «диарея путешественников», острые кишечные инфекции, вирусные процессы протекают остро и требуют срочного назначения противомикробных препаратов.
- Заболевания, которые часто сопровождаются микробной инфекцией, но не относятся к типичным острым инфекциям (хронические воспалительные болезни кишечника, хеликобактерная инфекция ЖКТ).
- Профилактика воспалительных процессов при хирургических операциях на кишечнике.
Воспалительные заболевания опасны не только непосредственным действием микробов на ЖКТ. При развитии инфекции нарушается процесс пищеварения: питательные вещества не всасываются, и организм не получает нужные витамины, макро- и микроэлементы. Поэтому антимикробная терапия должна быть начата как можно скорее: это предупреждает обезвоживание и дефицит необходимых для жизни веществ.
Заболевания кишечника, которые требуют противомикробной терапии
Заболевания разделяют по уровню локализации инфекции:
- Энтерит – воспаление тонкой кишки, часто сопровождается диареей.
- Колит – поражение нижних отделов кишечника, протекает тяжелее.
- Энтероколит – заболевание распространяется на все отделы кишечника.
Особенности кишечных противомикробных средств
Кишечные антимикробные препараты относятся к категории местных, поскольку они реализуют свои эффекты в кишечнике. Преимущества применения местных препаратов:
- создается эффект максимального действия в месте воспаления;
- исключается взаимодействие при одновременном приеме нескольких лекарственных средств;
- уменьшаются риски побочных эффектов;
- предупреждается устойчивость микробов к действию препарата.
| Избавление от микроорганизмов – наиболее важный этап лечения инфекций ЖКТ. Параллельно с этим проводится восстановление нарушений метаболизма. Однако заболевание будет продолжаться, пока не будет устранена главная причина его развития. Поэтому важно с первого дня симптомов подобрать нужный препарат и пройти курс лечения. |
Кишечные антисептики
Препараты антисептического действия минимально влияют на симбиотическую микрофлору, при этом устраняют патогенных возбудителей. В практике часто используются производные нитрофуранов.
Нитрофураны
К нитрофуранам относятся:
- Нифуроксазид («Экофурил», «Адисорд», «Эрсефурил», «Стопдиар» в капсулах и суспензии) – средство выбора при бактериальных кишечных инфекциях. Активное вещество этого представителя нитрофурановых лекарственных средств блокирует биохимические процессы в микробных клетках и провоцирует их гибель. Также нифуроксазид способен нарушать целостность микробных стенок и уменьшать количество микробных токсинов. Важное преимущество нифуроксазида заключается в том, что он не проникает через кишечную стенку, поэтому действует локально. Активен в отношении большинства грамотрицательных и грамположительных бактерий.
- Препарат «Фуразолидон» действует преимущественно в просвете кишечника, поэтому он эффективен для лечения диареи бактериального происхождения. Активно действует на возбудителей брюшного тифа, паратифов А и В, дизентерии. Резистентность к препарату развивается медленно, поэтому он широко используется в клинической практике.
Антисептики в меньшей степени влияют на нормальную бактериальную микрофлору и редко вызывают дисбактериозы.

Кишечные антибиотики
Доказано, что большинство кишечных инфекций вызываются грамотрицательными бактериями. По этой причине максимальный антибактериальный эффект оказывают антибиотики, активные в отношении грамотрицательной микрофлоры.
Аминопенициллины, цефалоспорины и некоторые другие группы антибиотиков часто становятся причиной развития антибиотикоассоциированной диареи, поэтому в лечении заболеваний желудочно-кишечного тракта они практически не используются.
Фторхинолоны
Для лечения кишечных инфекций чаще всего назначаются препараты группы фторхинолонов II поколения:
- Ципрофлоксацин («Ципринол», «Цифран ОД»). Он активен в отношении большинства патогенных бактерий, при этом у него низкая токсичность по отношению к здоровым клеткам. Препарат обладает системным действием, поэтому вопрос о его назначении должен решать лечащий врач.
- Норфлоксацин («Нормакс», «Норбактин», «Нолицин»). Лекарство вызывает гибель патогенов, в том числе потенциальных источников кишечной инфекции. Часто назначается для лечения шигеллеза и сальмонеллеза.
- «Офлоксацин». Активно борется с кишечными палочками, клебсиеллами, сальмонеллами.
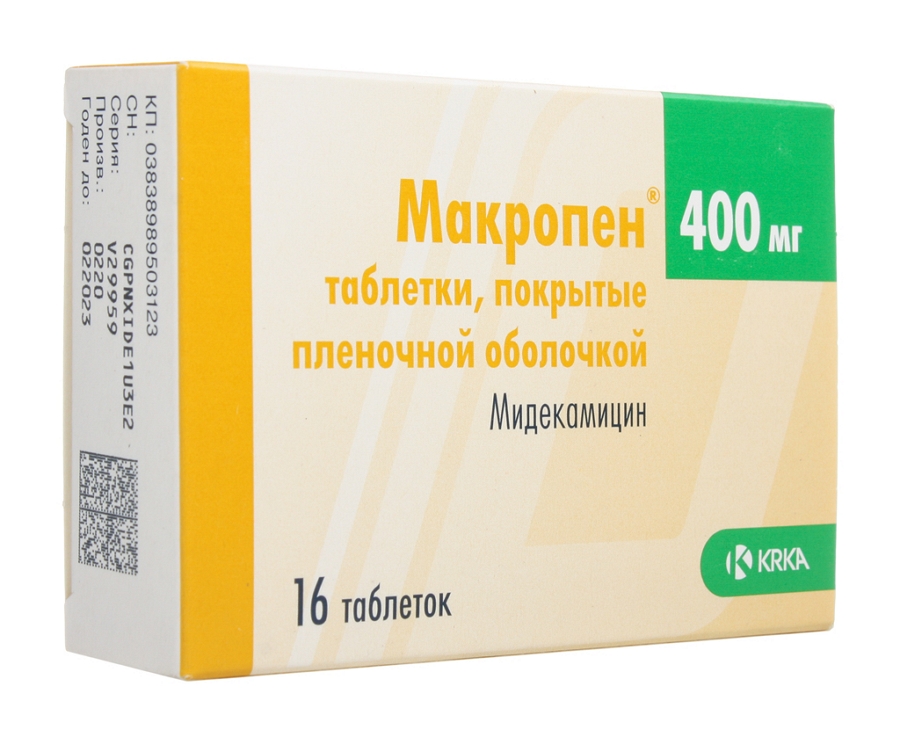
Макролиды
Представитель группы лекарственных средств – антибиотик Мидекамицин («Макропен»). Обладает бактериостатическим или бактерицидным эффектом в зависимости от дозы. Мидекамицин легко всасывается в пищеварительном тракте, однако потом быстро оказывает системное действие, поэтому при легких кишечных инфекциях препараты группы макролидов назначается редко. Проявляет активность в отношении всех типичных возбудителей кишечных инфекций.
Хлорамфеникол
Известный антибиотик «Левомицетин» нарушает выработку белковых структур клеток бактерий и угнетает их ферментативную активность. Однако при кишечных инфекциях он применяется только в случае тяжелых расстройств системного характера, поскольку вещество быстро проникает в кровь и проходит через все барьеры. Назначают препарат при недостаточном действии местных антибиотиков. Он эффективно борется с брюшным тифом, сальмонеллезом, паратифами.
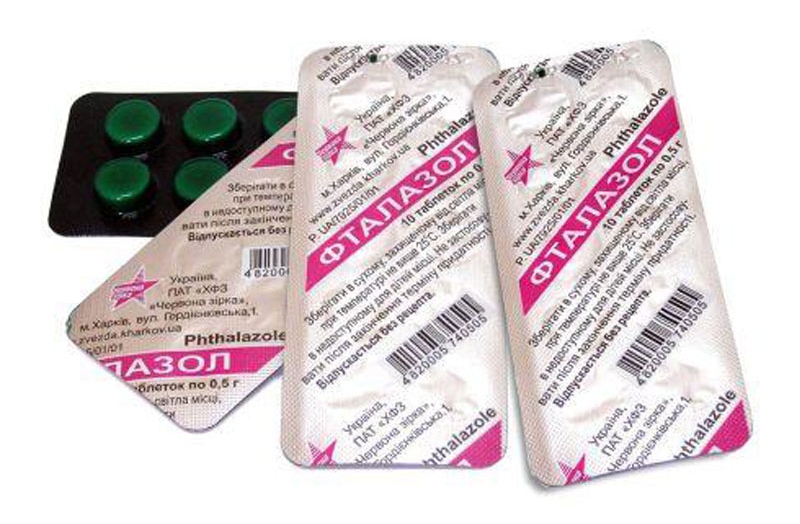
Сульфаниламиды
Таблетки «Фталазол» – яркий представитель группы сульфаниламидов, который часто используется в лечении острой кишечной инфекции. Он входит в состав обязательного набора лекарств для путешествий. Препарат доступен и эффективен, действует быстро. Действующее вещество фталилсульфатиазол тормозит обмен веществ в клетках микроорганизмов, а также препятствует их размножению. Бактериостатическое действие важно в случае, если речь идет о бактериях с мощными экзо- и эндотоксинами, которые при разрушении только ухудшают состояние пациента. Также «Фталазол» проявляет противовоспалительный эффект: он способствует выработке собственных механизмов защиты от воспаления.
Препарат применяется для лечения любых инфекций и воспалительных инфекционных заболеваний кишечника, кроме состояний, которые вызваны простейшими. Именно фталилсульфатиазол считается «золотым стандартом» для лечения «диареи путешественников», которые пребывают в местах с сомнительными санитарно-гигиеническими условиями. Также показан для лечения диарейного синдрома неизвестного происхождения не только у взрослых, но и у детей.

Другие препараты из группы сульфаниламидных средств применяются преимущественно для профилактики инфекции во время операций на органах ЖКТ.
Рифаксимин
Более 10 лет на фармацевтическом рынке существует кишечный антибиотик, который относится к группе «невсасывающихся», поскольку он минимально поступает в кровеносное русло. Итальянская компания презентовала препарат «Альфа Нормикс» с рифаксимином в роли действующего вещества. Он относится к группе рифамицинов, оказывает бактерицидное действие в кишечнике.
Максимальная концентрация лекарственного средства создается в просвете кишечника, что определяет высокую активность при микробных патологиях практически любого происхождения.
В различных исследованиях было установлено, что рифаксимин обладает бактерицидным действием – влияет на генетический материал возбудителя. Спектр активности препарата включает в себя действие против грамположительных и грамотрицательных аэробов и анаэробов. Рифаксимин не влияет на работу желудочно-кишечного тракта, не вызывает нарушений работы других органов и систем организма. Побочные эффекты при его приеме возникают редко.
Лечение Helicobacter pylori
Язвенная болезнь двенадцатиперстной кишки или гастродуоденит с позитивным тестом на бактерию хеликобактер (H.pylori) лечится с применением антибиотиков. Для терапии хеликобактерной инфекции в разных схемах применяется метронидазол, амоксициллин и кларитромицин. Схемы содержат два антибиотика для комплексного действия и стойкого эффекта избавления от хеликобактера.
Противогрибковые препараты
Для лечения кандидозов и других грибковых поражений кишечника используются такие группы противогрибковых средств:
- Полиены: «Нистатин», «Пимафуцин» (для приема внутрь) и «Амфотерицин В» (вводится внутривенно, выпускается в виде порошка для приготовления раствора).
- Триазолы: флуконазол («Микосист», «Дифлазон», «Дифлюкан»), итраконазол («Орунгал», «Румикоз», «Итразол»).
| Системные грибковые воспаления (висцеральные микозы) – достаточно редкие заболевания, однако у людей со сниженным иммунитетом усиливается грибковый рост. Важно вовремя понять причину развития симптомов и начать специфическое противогрибковое лечение в таблетках или инъекциях. |
Противопаразитарные препараты
Лямблиоз и амебиаз – наиболее распространенные инфекции ЖКТ, вызванные простейшими микроорганизмами. Лямблиоз затрагивает преимущественно тонкий кишечник, в то время как амебиаз вызывает колиты и поражает отделы толстого кишечника. Для лечения протозойных кишечных инфекций применяются специфические препараты, активные в отношении простейших.
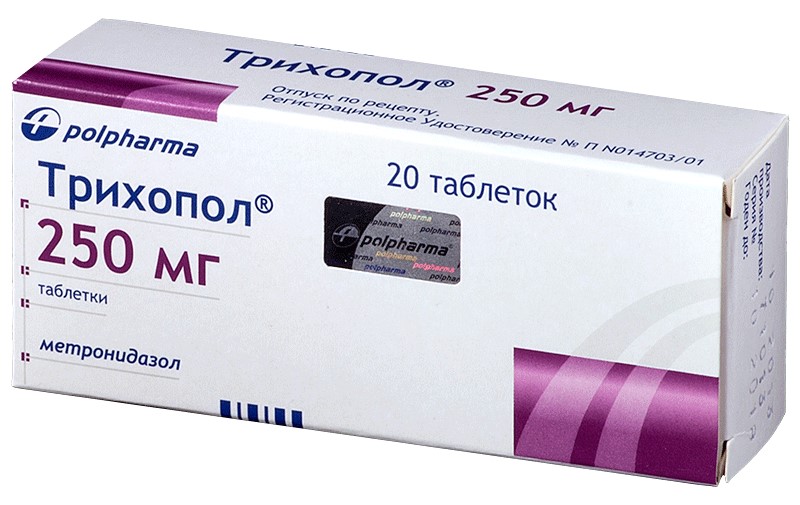
Метронидазол
Лекарство из группы производных 5-нитроимидазола обладает не только антибактериальными, но и противопротозойными свойствами. Применяется для борьбы с дизентерийной амебой, кишечной лямблией. Препарат проникает в дыхательные цепи простейших, прекращая их жизнедеятельность.
При приеме в виде таблеток этот препарат быстро проникает в кишечные стенки. Также метронидазол используется в лечении болезни Крона – хронического воспалительного заболевания кишечника. В ассортименте сети аптек «Ригла» с этим действующим веществом можно найти такие торговые названия, как «Клион», «Флагил», «Трихопол».
Противовирусные препараты
Эффективность антимикробных медикаментов с активностью против вирусов остается на стадии изучения. Однако большинство исследований позволяют делать выводы о необходимости применения некоторых средств с противовирусным действием при ротавирусной или энтеровирусной инфекциях, особенно у детей.
Например, хорошие результаты дает препарат «Арбидол» (действующее вещество – умифеновир). Он препятствует проникновению вирусов внутрь клеточных мембран организма, поэтому останавливает прогрессирование вирусной инфекции. Также лекарство стимулирует иммунитет – активизирует собственные механизмы защиты.
Советы при выборе противомикробного средства
При возникновении характерных симптомов кишечного инфекционного воспаления важно обратиться за помощью к врачу (инфекционисту, терапевту или гастроэнтерологу). Только специалист может оценить степень тяжести инфекции, определить вид возбудителя, а также остановить развитие болезни. Если симптомы указывают на острую инфекцию в кишечнике, то обязательно нужно проверить окружающих людей – членов семьи или коллектива, поскольку заболевания передаются контактным путем.
Для выбора лекарства необходимо пройти ряд обследований. Изначально используются кишечные антимикробные медикаменты широкого спектра действия: благодаря им можно начать лечение еще до того, как результаты анализов будут готовы.
| Правильный и своевременный подбор препарата предупреждает развитие серьезных осложнений, таких как обезвоживание, недостаток питательных веществ, распространение инфекции, нарушение работы ЖКТ. |
Источник
Комментарии
Опубликовано в журнале:
КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ И ТЕРАПИЯ »» 2000, 9 (1) В. А. Исаков, Л. В. Кудрявцева
Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского,
Лаборатория клинической микробиологии ЦКБ МЦ УД Президента РФ, Москва
В настоящее время антихеликобактерная терапия является стандартом лечения язвенной болезни, что отражено в международных и Российских рекомендациях [1, 2]. Согласно этим рекомендациям, наиболее эффективным режимом лечения считается тройная терапия, состоящая из базисного препарата (обычно препарат висмута или блокатор протонного насоса) и двух антибиотиков. Выбор антибиотиков имеет ключевое значение, так как именно они определяют эффективность, переносимость и стоимость лечения. Существуют несколько факторов, существенно влияющих на результат тройной терапии. Основным из них является резкое увеличение в популяции доли штаммов Н. pylori, устойчивых к антибиотикам, используемым в схемах лечения. Так, за 5 лет активного лечения заболеваний, ассоциированных с Н. pylori, в Гонконге доля штаммов H. pylori, резистентных к метронидазолу, увеличилась с 22 до 75 % [3]. Клинические исследования показывают, что эффективность схем тройной терапии, содержащих метронидазол, в среднем ниже на 30 %, если штамм Н. pylori устойчив к этому препарату.
Другой не менее важной проблемой является стоимость лечения. Чем она выше, тем больший процент эрадикации Н. pylori должна обеспечивать схема терапии, чтобы быть экономически выгодной. Стандартные схемы лечения были экономически выгодными при своей достаточно высокой стоимости, если частота эрадикации Н. pylori составляла 80 – 90 %. В настоящее время, когда распространенность штаммов Н. pylori, устойчивых к метронидазолу, достаточно высока, а эффективность стандартных схем лечения далека от идеальной, они перестают быть экономически выгодными.
В связи с этим, в схемах антихеликобактерной терапии стали широко использовать макролиды, главным образом кларитромицин. Однако, несмотря на высокую эффективность, препарат является дорогостоящим и вызывал ряд побочных реакций (диарея), которые ухудшали переносимость терапии в целом. Указанные обстоятельства послужили основанием для поиска макролидов, которые бы не уступали кларитромицину по эффективности, но стоили бы дешевле и давали меньше нежелательных эффектов. Одним из таких препаратов является азитромицин.
Азитромицин (Сумамед, “Pliva”) — первый представитель новой группы макролидных антибиотиков – азалидов. Он обладает широким спектром противомикробного действия. Связываясь с 50S-субъединицей рибосомы, азитромицин подавляет биосинтез белков микроорганизма. Препарат активен в отношении ряда грамположительных (S. pneumoniae, S. pyogenes, S. agalactiae, стрептококков групп С, F и G, Staphylococcus aureus и S. epidermidis) и грамотрицательных микроорганизмов (Haemophilus influenzae, Н. parainfluenzae и Н. ducreyi, Moraxella catarrhalis, Bordetella pertussis и В. parapertussis, Neisseria gonorrhoeae и N. meningitidis, Brucella melitensis, Helicobacter pylori, Gardnerella vaginalis), а также чувствительных анаэробных микробов (Clostridium spp., Peptostreptococcus spp. и Peptococcus spp.). Кроме того, азитромицин обладает активностью в отношении внутриклеточных и других микроорганизмов, в том числе Legionella pneumophila, Chlamydia trachomatis и С. pneumoniae, Mycoplasma pneumoniae, Ureaplasma urealyticum, Listeria monocitogenes, Treponema pallidum, Borrelia burgdorferi. Препарат не действует на грамположительные бактерии, устойчивые к эритромицину.
При приеме внутрь азитромицин хорошо всасывается и быстро распределяется, причем в тканях достигаются высокие концентрации антибиотика. Обладает длительным периодом полувыведения и медленно выделяется из тканей. Указанные свойства позволяют применять препарат один раз в сутки в течение 3 дней с высоким эффектом. Хорошее проникновение внутрь клеток и накопление в фагоцитах, с помощью которых азитромицин транспортируется к месту инфекции, способствуют в свою очередь повышению эффективности азитромицина. Выводится в основном с желчью в неизмененном виде, небольшая часть выводится почками.
Азитромицин высоко активен в отношении Н. pylori: его МПК90 составляет всего 0,5 мг/л, а процент штаммов Н. pylori, устойчивых к препарату, в популяции очень низкий – 3,7 % [4]. В другом исследовании была изучена чувствительность 106 штаммов Н. pylori к азитромицину. 8,5 % штаммов были расценены как устойчивые (МПК>16 мг/л), однако треть из них восстановили чувствительность к азитромицину в присутствии лансопразола [5]. Это очень важный результат, поскольку он демонстрирует наличие синергизма между азитромицином и лансопразолом — блокатором протонного насоса, который широко используется в схемах антихеликобактерной терапии.
Наиболее важным преимуществом азитромицина перед другими макролидами является его распределение в плазме крови, желудочной слизи, желудочном соке и ткани желудка после однократного приема. Так, изучая эти показатели у 27 больных раком желудка, которым назначали азитромицин в дозе 500 мг за 24, 48, 72, 96 и 120 ч до гастрэктомии, исследователи обнаружили увеличение концентрации азитромицина в желудочном соке на протяжении 73 – 96 ч до 2,0 мг/л. При этом в желудочной слизи концентрация азитромицина была в два раза выше и сохранялась на протяжении 120 ч после приема препарата. Еще более высокие концентрации азитромицина наблюдались в ткани желудка (в 10 раз выше, чем в слизи, и в 20 раз выше, чем в желудочном соке), они сохранялись на протяжении 24 ч и медленно уменьшались в течение 5 дней [6]. К подобным выводам пришли и другие исследователи, показавшие, что концентрация азитромицина в слизистой оболочке желудка существенно превосходит таковую в крови [7].
В другом исследовании у больных хроническим хеликобактерным гастритом, получавших тройную терапию пантопразолом, метронидазолом и азитромицином (1-й день 500 мг и 2 – 5-й дни по 250 мг), ежедневно определяли концентрацию азитромицина в ткани желудка и желудочном соке [8]. За весь период лечения, а также спустя три дня после окончания приема азитромицина концентрация его в ткани желудка была не меньше 0,25 мкг/г (рис. 1) и, по мнению авторов, соответствовала МПК90, азитромицина для Н. pylori. Результаты данного исследования исключительно важны, так как они являются основанием для разработки схем лечения с низкими дозировками азитромицина. Полученные данные показали, что препарат может быть эффективным даже в дозе 250 мг/сут, а использование низких дозировок препарата снижает риск нежелательных реакций и стоимость лечения.
Рис. 1.
Динамика концентрации азитромицина в слизистой оболочке желудка. (цит. по 8).
Еще одним фактором, снижающим эффективность антихеликобактерной терапии, является способность Н. pylori к паразитированию внутри клеток. Полагают, что персистирование Н. pylori в эпителиоцитах, париетальных клетках и фагоцитах предохраняет микроорганизмы от воздействия антибиотиков и приводит к рецидиву инфекции вскоре после терапии. При специальном изучении влияния азитромицина на внутриклеточно расположенные Н. pylori в трех различных клеточных линиях было показано, что препарат существенно уменьшает количество клеток с внутриклеточно персистирующими Н. pylori, а обработка этих клеток азитромицином и лансопразолом полностью блокирует этот феномен [9, 10].
Число клинических исследований, в которых изучалась эффективность азитромицина в лечении хеликобактерной инфекции, невелико, однако с каждым годом оно увеличивается, что свидетельствует о возрастающем интересе к препарату как компоненту тройной терапии. По данным W. Dohmen и R. Seelis (1998), с 1990 по 1997 год было проведено 19 исследований, в которых азитромицин изучался в качестве компонента антихеликобактерной тройной терапии [11]. Частота эрадикации Н. pylori в этих исследованиях составляла 47 – 94 %. Такой широкий интервал указывает на то, что довольно часто изучались новые схемы лечения с эмпирически подобранными дозировками и кратностью приема препарата. Это не удивительно, так как фундаментальные работы, посвященные фармакокинетике азитромицина в слизистой оболочке желудка и желудочном соке, а также важные исследования синергизма азитромицина с различными базисными препаратами в отношении Н. pylori появились лишь в последние 2—3 года.
Открытые неконтролируемые исследования показали, что однонедельная тройная терапия омепразолом, азитромицином и метронидазолом приводит к эрадикации Н. pylori в среднем в 75 – 85 % случаев и рубцеванию более 95 % язв (в случае язвенной болезни) через 4 недели от начала лечения, что соответствует эффективности стандартных схем тройной терапии с использованием кларитромицина [11, 12]. При сравнении эффективности однонедельных схем лечения пантопразол (40 мг 2 раза в сутки)+амоксициллин (1000 мг 2 раза в сутки)+кларитромицин (500 мг 2 раза в сутки) или азитромицин (500 мг/сут в течение 6 дней) оказалось, что схема лечения с кларитромицином обеспечивала эрадикацию Н. pylori у 81 % больных, а с азитромицином — у 78 % (различия недостоверны) [13].
Наиболее интересны данные, полученные при изучении низкодозировочных или укороченных по времени режимов тройной терапии с использованием азитромицина и лансопразола, учитывая уникальный синергизм между двумя препаратами. Так, в сравнительном исследовании однонедельной тройной терапии омепразол 40 мг/сут+кларитромицин 500 мг/сут + тинидазол 1000 мг/сут и терапии лансопразол 30 мг/сут 7 дней + азитромицин 500 мг/сут 3 дня+метронидазол 500 мг/сут 3 дня частота эрадикации Н. pylori существенно не различалась (93,3 и 91,2% соответственно) [14]. В другом исследовании у 160 больных сравнивалась эффективность однонедельной тройной терапии (омепразол 20 мг/сут + кларитромицин 500 мг/сут + тинидазол 1000 мг/сут) с ультракоротким режимом лечения (лансопразол 30 мг/сут 1 – 4-й дни лечения, азитромицин 500 мг/сут 2 – 4-й дни лечения, тинидазол 2000 мг однократно на 3-й день). Частота эрадикации Н. pylori составила 85,5 и 80,8 % соответственно, а язвы к контрольному сроку зарубцевались у 100 и 97,8 % больных (различия недостоверны) [15]. В открытом исследовании такая же схема лечения обеспечивала эрадикацию Н. pylori у 86,3 % больных [16]. Следует отметить, что частота побочных реакций при использовании коротких схем лечения примерно такая же, как при использовании стандартных схем антихеликобактерной терапии или даже ниже. Важнейшим их достоинством является снижение затрат на лечение больного. Так, если сравнить стоимость эквивалентных по длительности схем лечения с использованием кларитромицина и азитромицина, то стоимость последнего оказывается примерно вдвое ниже, а в схемах с низкими дозами и укороченными сроками применения – в три раза ниже.
Все это, безусловно, делает азитромицин (Сумамед) одним из наиболее привлекательных представителей группы макролидов для включения в схемы антихеликобактерной терапии. Необходимо проведение сравнительных контролируемых исследований по изучению эффективности таких схем лечения (особенно ультракоротких).
1. Рекомендации по диагностике Helicobacter pylori у больных язвенной болезнью и методам их лечения. Росс. журнал гастроэнтерологии, гепатологии и колопроктологии, 1998, 1, 105–107.
2. Current European concepts in the management of Helicobacter pylori infection. The Maastricht Consensus Report. Gut, 1997, 41, 8–13.
3. Ling Т., Cheng A., Sung J. et al. An increase in Helicobacter pylori strains resistant to metronidazole: a five-year study. Helicobacter, 1996, 1, 57–61.
4. Gosciniak G., Kovacic D., Przondo-Mordarska A. In vitro susceptibility of Helicobacter pylori strains to Azithromycin. In: Proceedings of the 8th European Congress of Clinical Microbiology and Infectious Diseases, Lausanne, Switzerland, 1997, 945 (abstract).
5. Trautmann M., Riediger C., Moricke A. et al. Combined activity of azithromycin and lansoprazole against Helicobacter pylori. Helicobacter, 1999, 4, 113–120.
6. Harrison J.D., Jones J.A., Morris D.L. Azithromycin levels in plasma and gastric tissue, juice and mucus. Eur. J. Clin. Microbiol. Infect. Dis., 1991, 10, 862-864.
7. Blandizzi C., Malizia Т., Gherardi G. et al. Gastric mucosal distribution and clinical efficacy of azithromycin in patients with Helicobacter pylori related gastritis. J. Antimicrob. Chemother., 1998, 42, 75–82.
8. Krichhoff R., Laufen Н., Schacke G. et al. Determination of azithromycin in gastric biopsy samples. Int. J. Clin. Pharmacol. Ther., 1999, 37, 361–364.
9. Rigo R., Holmberg M., Engstrand L. Eradication of intracellular Helicobacter pylori in multidrug resistant monocytes using azithromycin and lansoprazole. Gut, 1996, 39 (Suppl. 2), A10.
10. Hulten К., Cars O., Hjelm E. Engstrand L. In-vitro activity of azithromycin against intracellular Helicobacter pylori. J. Antimicrob. Chemother., 1996, 37, 483–489.
11. Dohmen W., Seelis R.E. The role of azithromycin in the treatment of Helicobacter pylori infection – a retrospective report. Infection, 1998, 26, 256–262.
12. Vcev A., Vceva A., Ivandic A. et al. Omeprazole and azithromycin with and without metronidazole in the eradication of Helicobacter pylori in duodenal ulcer disease. Lijecnicki Vjesnik, 1997, 119, 210–213.
13. Vcev A., Stimac D., Ivandic A. et al. Pantoprazole, amoxycillin and either azithromycin or clarithromycin for eradication of Helicobacter pylori in duodenal ulcer. Aliment. Pharmacol. Ther., 2000, 14, 69–72.
14. Caselli M., Trevisani L., Tursi A. et al. Short-term low-dose triple therapy with azithromycin, metronidazole and lansoprazole appears highly effective for the eradication of Helicobacter pylori. Europ. J. Gastroenterol. Hepatol., 1997, 9, 45–48.
15. Trevisani L., Sartori S., Caselli M. et al. A four-day low dose triple therapy regimen for the treatment of Helicobacter pylori infection. Am. J. Gastroenterol., 1998, 93, 390–393.
16. Trevisani L., Sartori S., Galvani F. et al. Evaluation of a new ultrashort triple therapy for Helicobacter pylori disease. Aliment. Pharmacol. Ther., 1998, 12, 1269–1272.
Сумамед® – Досье препарата
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник