Диарея от лучевого лечения
В данной статье рассматриваются следующие осложнения противоопухолевого лечения со стороны желудочно-кишечного тракта:
- снижение массы тела (недостаточность питания)
- пострезекционные синдромы (осложнения после операционных вмешательств на желудке, поджелудочной железе)
- нарушение стула на фоне лечения (диарея/запор)
- лучевые поражения кишечника
Снижение массы тела (недостаточность питания)
Снижение массы тела у онкологического пациента возникает вследствие многих факторов: необходимо учитывать лечение пациента сейчас и в прошлом, состояние больного, объем операционных вмешательств и т.д.
Причины потери массы тела:
- Проведенное оперативное лечение (пострезекционные синдромы)
- Последствия проводимого лечения: ХТ/ЛТ; нарушение стула, тошнота, рвота, лучевые поражения слизистой, снижение аппетита/изменение вкуса.
- Нарушение проходимости/моторики желудочно-кишечного тракта
- Прогрессирование основного заболевания, хронический болевой синдром.
- Другие причины
Оценка недостаточности питания
В амбулаторной практике используются различные шкалы для оценки недостаточности питания.
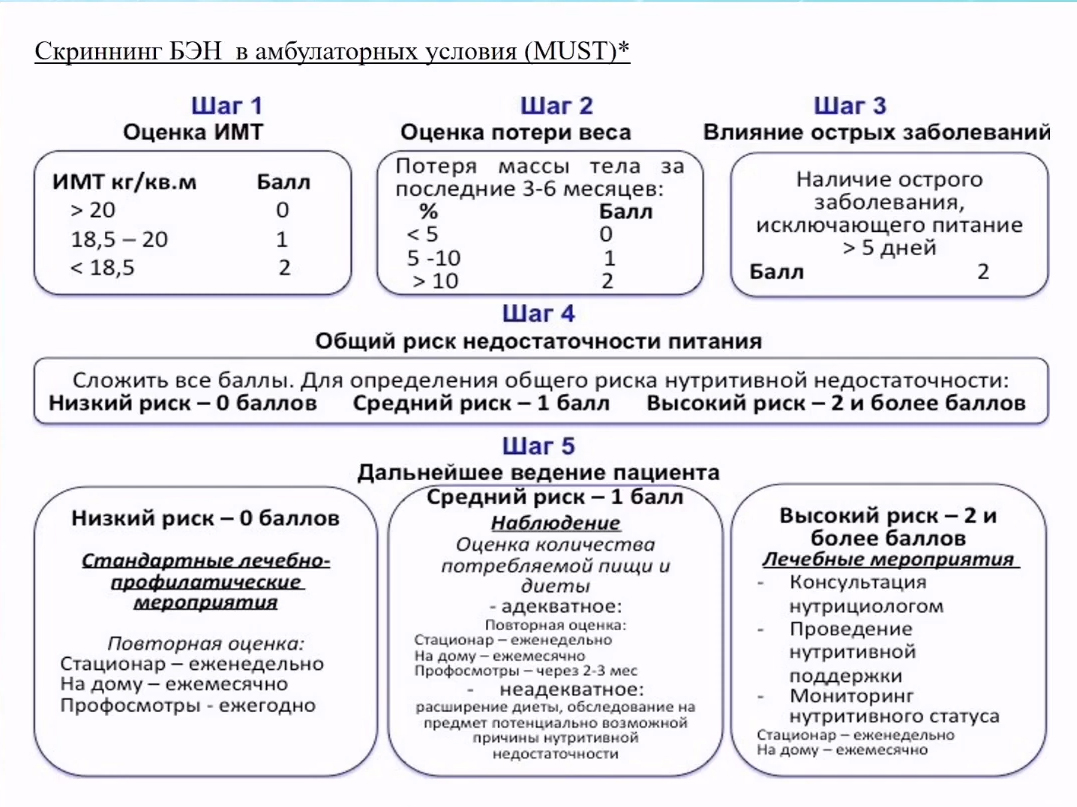
Оценка ситуации должна включать в себя как минимум следующие вопросы:
- Какой объем веса потерял пациент от момента начала заболевания до момента приема у гастроэнтеролога?
- Сколько из этого веса было потеряно за последние 1-3 месяца?
- Принимал ли пациент какие-то препараты лечебного питания?
- Какую дополнительную терапию получает пациент?
- Получает ли на сегодняшний день препараты лечебного питания? Если да, то в какой дозировке и что именно?
Алгоритм назначения нутриционной поддержки
Данный алгоритм должен разрабатываться совместно со специалистом, поскольку пациент не может самостоятельно подобрать для себя адекватную терапию, которая поспособствует улучшению самочувствия и облегчению симптоматики.
Для алгоритма назначения нутриционной поддержки необходимо ответить на следующие вопросы:
- Сколько?
Для расчета энергетических потребностей пациента необходимо оценить имеющуюся недостаточность питания, риски прогрессирования недостаточности питания.
- Как?
Осуществляется выбор оптимального пути введения лечебного питания. Возможны следующие варианты: сиппинг (лечебное питание, которое пациент может употреблять самостоятельно), зондовое питание, комбинированная нутриционовая поддержка (совмещение парентерального и энтерального питания). Отдельно стоит рассматривать ситуации, когда у пациента есть стома (гастростома, энтеростома, эзофагостома): в этом случае введение препаратов лечебного питания может осуществляться через нее.
- Когда?
Определяется режим кормления, режим введения препаратов лечебного питания.
- Как долго?
Определяются сроки нутриционной поддержки пациента.
- Чем?
Осуществляется выбор препаратов для конкретной ситуации.
Методы оценки эффективности проводимой нутриционной поддержки
- Биоэлектрический импедансный анализ
- Двухэнергетическая рентгеновская абсорбциометрия
Эти методы часто используются в рутинной практике. Они позволяют оценить изменение состава тела на фоне нутриционной поддержки, оценить объем жировой массы, внеклеточной и внутриклеточной жидкости, косвенно оценить количество мышечной массы.
- лабораторно-инструментальная оценка показателей
- калориметрия
Эти методы редко используются в рутинной практике. Однако их достоинство в доступности – врач может осуществить оценку состояния тела прямо во время приема.
Пострезекционные синдромы
Синдромы оперированного желудка
К ним относятся – депминг-синдром, гипогликемический синдром, анемический синдром, синдром приводящей петли, рефлюкс-эзофагит, недостаточность питания, моторные нарушения культи желудка, анастомоза.
Чаще всего с этими синдромами сталкиваются пациенты, которые перенесли операции на желудке, пищеводе или поджелудочной железе. Данные симптомы могут развиваться, как в раннем, так и в более отсроченном периоде.

Демпинг-синдром. Как правило, проявляется слабостью, потливостью после приема пищи, головокружением, зачастую возникает при приеме углеводистой пищи. Развивается, как в раннем, так и в позднем послеоперационном периоде. Синдром обусловлен быстрой эвакуацией пищи из пищевода в тонкую кишку с последующим развитием гипергликемии, то есть пища быстро попадает из пищевода в тонкую кишку, что вызывает повышение уровня глюкозы (сахара) в крови.
Обычно регулируется подбором режима питания и рациона, а также медикаментозными препаратами.
Пациентам, страдающим демпинг-синдромом, необходимо вести пищевой дневник. Это поможет отследить причины синдрома (определенное время суток, определенная еда и т.д.).
Гипогликемический синдром. Проявляется недостаточным уровнем сахара в крови. Является разновидностью позднего демпинг-синдрома.
Анемия. Обусловлена дефицитом железа и витамина В-12 после удаления желудка. Данное состояние необходимо корректировать и компенсировать препаратами.
Рефлюкс-эзофагит. Это заброс пищи из тонкой кишки в пищевод. Самыми частыми проявлениями рефлюкс-эзофагита является изжога, горечь во рту, тяжесть после приема пищи, ощущение жжения по ходу пищевода. Реже симптом проявляется жжением в области языка, кислым привкусом во рту. Корректируется режимом питания, новыми жизненными привычками и назначением медикаментозной терапии.
Недостаточность питания или потеря массы тела. Данный синдром требует коррекции рациона и режима питания, а также назначения дополнительной нутриционной поддержки.
Важно знать, сколько массы пациент потерял до операции, после операции, во время химио/лучевой терапии. Исходя из этого подбираются препараты лечебного питания.
Нарушение культи желудка, анастомоза (т.е. места соединения органов). Осложнение, которое относится к моторно-эвакуаторным нарушениям. Корректируется медикаментозно.
Болевой синдром. Может быть обусловлен разными факторами. При обращении к врачу важно описать, когда возникают боли, связаны ли они с приемом пищи, через какое время и в каком месте после приема пищи возникают, проходят самостоятельно или требуют применения препаратов, сопровождаются ли тошнотой, рвотой, нарушением стула.
Астения. Состояние общей слабости и утомляемости.
Эти и другие симптомы, которые могут беспокоить пациента в послеоперационном периоде или на фоне проводимого лечения. Любые жалобы требуют обращения к врачу.
Диагностика синдромов оперированного желудка
- ФГДС (фиброгастродуоденоскопия)
- клинический анализ крови
- биохимический анализ крови (при снижении массы тела + общий белок и альбумин)
- КТ грудной и брюшной полости по назначению онколога
- при развитии железодефицитного состояния рекомендовано два раза в год сдавать анализ крови на железо, ферритин, коэффицент насыщения трансферрина железом, витамин В-12, фолиевую кислоту
- рентгеноскопия (при появлении рвоты, стойкого болевого синдрома в эпигастральной области после приема пищи)
Обследования позволяют подобрать терапию, дать точные рекомендации по образу жизни.
Как установить причину рефлюкса (заброса пищи обратно в пищевод)?
В сложных случаях для оценки характера рефлюктата и оценки того, что именно забрасывается в пищевод, используется суточная импеданс-pH-метрия. Данное исследование особенно актуально для пациентов, которые перенесли гастрэктомию (удаление желудка), резекцию пищевода.
Обследование выполняется в тех клинических ситуациях, когда пациент получает медикаментозное лечение, но улучшения не наблюдаются. Либо, когда жалобы не соответствуют характеру проведенного оперативного вмешательства.
Консервативная терапия после оперативного вмешательства на желудке
- Коррекция недостаточности питания (подключение препаратов лечебного питания)
- Коррекция анемического синдрома (т.е. анемии). Назначаются препараты железа В12, фолиевая кислота. При железодефицитном состоянии возможно парентеральное введение препаратов железа.
- Симптоматическая терапия (т.е. терапия, которая снимает симптомы): ферменты, прокинетики и т.д.
- Подбор рациона питания в зависимости от симптомов.
- Формирование новых привычек. Например, пациентам после операции на желудке или его удалении лучше спать с приподнятым изголовьем, не переедать, распределять приемы пищи в течение дня и не ложиться после еды. Это позволит минимизировать заброс пищи в обратно пищевод.
Последствия оперативного вмешательства на поджелудочной железе
Хирургические вмешательства на поджелудочной железе зачастую влекут за собой недостаточность выработки ряда ферментов и гормонов в организме. Нехватка данных веществ может привести к потере массы тела, вторичному диабету, диарее, синдрому избыточного бактериального роста. Вторичной проблемой становится боль в животе.
Чтобы оценить недостаточность ферментов проводится анализ кала на панкреатическую эластазу.
Основное лечение патологии заключается в заместительной ферментативной терапии, подбор питания.
Нарушение стула на фоне лечения (диарея/запор)

Диарея
Основные факторы, которые вызывают диарею (в зависимости от них подбирается терапия):
- проведение химиотерапии
- проведение лучевой терапии
- гастроэктомия (удаление желудка)
- ферментативная недостаточность
- нарушение всасывания макро и микроэлементов после обширных резекций тонкой кишки
- гипоальбуминемия (низкая выработка белка альбумина может приводить к отечности кишки)
- инфекционная диарея из-за снижения иммунитета на фоне противоопухолевой терапии
- синдром избыточного бактериального роста (особенно усугубляется после проведенного оперативного лечения и на фоне химиолучевой терапии)
- прием антибиотиков
- развитие псевдомембранозного колита
Любой из вышеперечисленных симптомов требует обращения к врачу для назначения терапии.
Если на фоне диареи, у пациента отмечается подъемы температуры, интоксикация, то необходимо дополнительное обследование на псевдомембранозный колит.
Диарея и недержание кала
После операций на органах, расположенных в малом тазу, у пациента может наблюдаться комбинация сразу двух синдромов – диареи и недержания кала. Чаще всего данное расстройство наблюдается у пациентов гинекологического профиля.
У больного может наблюдаться неоформленный или полуоформленный стул, а также фрагментная дефекация в течение дня, трудности с удержанием кала и газов после возникновения позывов на дефекацию. Иногда бывает ночное недержание кала.
Чтобы оценить состояние анального сфинктера специалисты назначают сфинктерометрию.
При лечении патологии применяется комбинация методов – лекарственная терапия, физиотерапия, физические упражнения.
Запор / задержка стула
Симптом может сопровождаться такими жалобами, как напряжение и/или боли в животе, натуживание, вздутие живота, твердый кал, ощущение неполного опорожнения кишечника, необходимость ручного пособия при опорожнении, отсутствие позывов на дефекацию или ложные позывы на дефекацию без опорожнения кишечника.
Причинами запора/задержки стула могут послужить:
- проведение химиотерапии
- проведение лучевой терапии
- хирургическое лечение
- спаечная болезнь
- канцероматоз
- усугубление заболеваний, уже имеющихся до установки онкологического диагноза
Если пациент наблюдает у себя запор или задержку стула, необходима консультация специалиста.
Методы диагностики, которые помогут установить причину запоров:
- фиброколоноскопия
- анасфинктерометрия (позволяет изучить тонус мышц тазового дна и тонус анального сфиктера)
- рентгеноскопия
- обзорная рентгенограмма брюшной полости
- лабораторные исследования (посевы кала и др.)
Если на фоне лечения задержка стула длится от 4 суток, а также отмечаются повышенное газообразование, тошнота и/или рвота, боли в кишечнике, то необходима срочная консультация специалиста!
Терапия запора/задержки стула
Традиционным методом лечения является медикаментозная терапия. В случае спаечного процесса может потребоваться хирургическое лечение.
Отметим, что противоболевая терапия может усугубить ситуацию.
Лучевые поражения кишечника
Лучевые поражения кишечника проявляются в виде колитов – воспалительного заболевания слизистой оболочки кишечника. Колиты преимущественно развиваются у пациентов, получающих терапию на область малого таза (матка, цервикальный канал, простата, прямая кишка, мочевой пузырь).
Колиты могут возникнуть на любом этапе лечения: во время начала лучевой терапии и в течении 3 месяцев после окончания лечения. Существуют и позднеотстроченные лучевые колиты, которые возникают в течение первого года после проведенной лучевой терапии.
Симптомы
К основным симптомам лучевого поражения кишечника относят: нарушение стула, диарея, ложные позывы к дефекации, боли по ходу кишечника и боли в заднем проходе, в зависимости от зоны, куда пациент получает лучевую терапию. При достаточно выраженном воспалении появляются следующие симптомы — недержание кала и газов, диспепсия, метеоризм, рвота, тошнота, снижение массы тела на фоне диареи.
Если в начале лучевой терапии, во время нее, после нее у пациента отмечается выделение крови с каловыми массами – стоит немедленно обратиться к врачу! Он назначит необходимые обследования и лечение.
Диагностика лучевых поражений кишечника
Исследования, которые позволяют определить степень поражения и назначить терапию:
- Сбор жалоб и анамнеза
- Лабораторные исследования
- ФКС — фиброколоноскопия (применяется при позднеотсроченном колите)
- Аноскопия (применяется при ранних поражениях, позволяет оценить степень воспалительной реакции прямой кишки)
- КТ/МРТ
- Ирригоскопия
- Фистулография (применяется только при наличии свища, на определение свищевого хода, это не рутинное исследование.
Терапия
При лучевых поражениях желудочно-кишечного тракта терапия зависит от локализации патологического процесса. В основном используются:
- препараты месалазина
- глококортикостероиды
- заместительная ферментативная терапия
- антидиарейные препараты
- коррекция микробиоценоза
Срок лечения определяется специалистом. Стоит отметить, что лучевой колит невозможно вылечить за 2-3 недели, терапия должна быть длительной и систематической.
Источник
Понос (диарея) – учащенное опорожнение кишечника с выделением разжиженных и обильных испражнений. Считается, что при поносе стул бывает более 2 раз в сутки (однако нельзя не назвать поносом однократное опорожнение кишечника жидкими массами), что он значительно больше нормального количества в 200 г (для некоторых заболеваний характерен «ректальный плевок» – мизерное количество кала) и что в нем повышено содержание воды. Не следует путать понос с частым стулом, когда при неоднократной дефекации не возрастает суточная масса кала, или с недержанием кала, когда не изменяется ни количество, ни консистенция.
У онкологических больных понос может быть обусловлен:
- поражением кишечника опухолевыми узлами;
- последствиями удаления части кишечника с опухолью (синдром короткой кишки), когда уменьшается всасывающая поверхность и сокращается время прохождения пищи;
- осложнениями химиотерапии, когда гибнут клетки слизистой оболочки;
- повреждением кишечника вследствие лучевой терапии, обычно при дозе свыше 40 Грей (продолжительность его редко превышает 3 недели после завершения курса);
- выделением нейроэндокринными опухолями биологически-активных веществ (карциноидный синдром); наряду с поносом больных беспокоят приливы, бронхоспазм, цианоз, поражения кожи;
- погрешностями питания;
- инфекцией, паразитами кишечника, патогенными грибами и пр. (в подобных случаях присутствуют характерные общие симптомы);
- почечной недостаточностью (уремия) при раке почки;
- заболеваниями других органов (гастрогенный, панкреатогенный,
гепатогенный, метаболический); - приемом слабительных средств.
Кишечник всасывает огромное количество жидкости: с пищей мы получаем около 2 литров жидкости, вырабатываем 1 литр слюны, 6 литров желчи, желудочного и панкреатического сока; выделяем же с калом около 100 мл. Понос возникает в случае нарушения нормального соотношения между всасыванием жидкости в кишечнике и ее секрецией при ускоренном продвижении содержимого по кишечнику.
Механизмы поносов сложны, при разных патологических состояниях могут преобладать разные патогенетические факторы. Одним из механизмов является ускоренное продвижение пищевой кашицы под влиянием усиленного сокращения кишечника или, наоборот, при ослаблении перистальтики. Другой механизм – нарушение всасывания жидкости измененной слизистой кишечника. Третий механизм – выделение в просвет кишечника воспалительного секрета, раздражающего рецепторы, что приводит и к усилению перистальтики, и к нарушению всасывания.
Поносы подразделяются на острые и хронические. Хроническим понос считается, если беспокоит более 2-х недель или рецидивирует. Этиологию (причину) поноса поможет выяснить наблюдающий врач.
Лечение направлено на устранение причины поноса и восстановление водно-электролитного баланса. Если причину устранить невозможно (опухоль, короткая кишечная трубка, последствия химиотерапии или лучевого воздействия), то ограничиваются симптоматической терапией, в частности, назначают противодиарейные средства (лоперамид/ имодиум после каждого акта дефекации). При некоторых инфекциях эти средства принимать не следует, так как они замедляют перистальтику кишечника, приводя к застою кишечного содержимого и патологической флоры.
При нейроэндокринных опухолях применяется специфическое средство, подавляющее секрецию соматостатина. Оно может помочь и при синдроме короткой кишки.
В ряде случаев следует назначать антимикробные препараты даже при неинфекционной природе поноса и провести полноценный курс, не ограничиваясь 1-2 днями. Иначе создается риск «приучить» неубитую патогенную флору к лекарству, на которое она при повторном его применении не будет реагировать.
При любом поносе следует больше пить: чай, дубящие отвары, вяжущие соки и кисели. С приемами пищи лучше повременить. Если нет сил терпеть голод, лучше всего съесть рисовую кашу на воде с сухарями.
Источник
Симптомы лучевого энтерита могут возникнуть довольно рано, в период проведения лучевой терапии; иногда вскоре после лечения, но их развитие возможно и через несколько месяцев и даже лет по его окончании. Рано могут наблюдаться тошнота, рвота, расстройство стула в виде поноса или запора. Вовлечение в патологический процесс толстой кишки обусловлено тенезмами, появлением слизи и алой крови в фекалиях в результате образования изъязвлений в слизистой оболочке нижнего отрезка кишечника (10% случаев), преобладанием вначале поноса, затем запора в связи с ранним возникновением стриктур толстой или прямой кишки. Преобладание в клинической картине признаков поражения тонкой кишки на ранней стадии характеризуется схваткообразными болями в животе, тошнотой, усилением перистальтики, водянистым стулом, вздутием, урчанием, переливанием. Иногда эти симптомы довольно быстро исчезают, но в ряде случаев остаются в течение продолжительного времени либо возобновляются через несколько месяцев после облучения. Лучевая диарея развивается главным образом в связи с уменьшением реабсорбции желчных кислот поврежденной слизистой оболочкой подвздошной кишки, что ингибирует реабсорбцию воды толстой кишкой. Реактивное воспаление слизистой оболочки тонкой кишки сопровождается расстройством мембранного пищеварения, дисбактериозом. Истощение и нарушение созревания абсорбтивных клеток ворсинок приводит к уменьшению активности ферментов «щеточной» каймы. Дыхательный тест позволяет обнаружить нарушение всасывания лактозы, D-ксилозы, гликохолатов, витамина B12. Возможно умеренное расстройство абсорбции жира, чаще в остром периоде. Однако описано и бессимптомное течение заболевания даже при значительных повреждениях слизистой оболочки кишки.
Отсутствие острых, ранних признаков поражения кишечника не гарантирует от появления поздних, индуцированных облучением его изменений. Латентный период, т.е. интервал между временем облучения и появлением признаков поражения кишечника, варьирует в весьма больших пределах – от 3 мес до 31 года. Частота поздних кишечных проявлений лучевой терапии составляет примерно 10%. В этом периоде наиболее характерным симптомом лучевого энтерита являются коликообразные боли в животе, обусловленные частичной тонкокишечной непроходимостью, которая иногда переходит в полную непроходимость. Могут наблюдаться тошнота, рвота, признаки нарушения всасывания различной степени. Кишечная непроходимость обычно бывает вызвана локальным механическим сужением кишки, но может быть обусловлена наличием нефункционирующих ее участков, препятствующих нормальной перистальтике. Может быть одновременное вовлечение многих сегментов кишки. Клиническое обследование больного обнаруживает признаки кишечной непроходимости и пальпаторно определяемые плотные образования в брюшной полости, появление которых связано с воспалением кишки и брыжейки. Между тазовыми органами и органами брюшной полости возможно формирование свищей. В подобных случаях возникают такие симптомы, как мутные влагалищные выделения, пневматурия и быстрое появление непереваренной пищи в жидком стуле. Доказательством образования ректовагинального свища служит возникновение признаков проктита. Абсцессы обычно локализуются в малом тазе и могут привести к перитониту и сепсису. Перфорация подвздошной и толстой кишки хотя и наблюдается относительно редко, также может быть причиной острого перитонита. Изредка отмечают массивные кишечные кровотечения, обусловленные изъязвлениями подвздошной и толстой кишки.
При обширном поражении тонкой кишки на первый план в клинической картине выступают признаки синдрома нарушенного всасывания. У таких больных наряду с значительной, недавно возникшей, необъяснимой потерей массы тела о нарушении кишечной абсорбции свидетельствуют такие тесты, как определение жира в фекалиях, всасывание витамина B12, дыхательная проба на желчные кислоты, всасывание D-ксилозы. Нарушение абсорбции желчных кислот способствует как диарее, так и стеаторее.
[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12], [13], [14], [15], [16], [17], [18]
Источник