Кишечная инфекция острый инфаркт
Кишечная инфекция и инфаркт миокарда. Дифференциация инфекций с инфарктом миокардаТрудности дифференциальной диагностики инфаркта миокарда и острых кишечных инфекций неоспоримы. Они связаны с нередко возникающим при инфаркте миокарда абдоминальным синдромом, с одной стороны, и изменениями на ЭКГ при тяжелом течении острых кишечных инфекций, с другой, выражающимися депрессией сегмента ST и отрицательным зубцом Т. Указанные изменения являются следствием интоксикации, гипоксии, водно-электролитных и микроциркуляторных нарушений при острых кишечных инфекциях. Сложность диагностики еще более усугубляется, когда инфаркт миокарда осложняется кардиогенным, а острая кишечная инфекция инфекционно-токсическим шоком (ИТШ). По мнению В.Х.Василенко и М.Ю.Мелиховой (1959), абдоминальный синдром при инфаркте миокарда может быть единственным эквивалентом боли в области сердца. По данным авторов, у 50 % больных с инфарктом миокарда наблюдаются легкие диспепсические расстройства и У 1/3 — однократная или повторная рвота. У 63 наблюдаемых нами больных с инфарктом миокарда отмечались боль в эпигастрии (82,5 %), тошнота (88,8 %), рвота (80,9 %), жидкий стул (14,3 %). Значительные трудности диагностики были связаны с наличием резорбционно-некротического синдрома при инфаркте миокарда, характеризующемся лихорадкой, лейкоцитозом периферической крови, увеличенной СОЭ и гиперферментемией. Нами наблюдалось 90 больных, поступивших в клинику с диагнозом пищевой токсикоинфекции, у которых в стационаре был выявлен крупноочаговый инфаркт миокарда. В анамнезе лишь у 23 больных была зарегистрирована ИБС. Рвота отмечалась у 82 (91,1 %), тошнота — у 88 (97,7%), жидкий стул — у 45 больных (50%), в том числе с частотой до 5 раз в сутки — у 42 (93,4 %), 6—10 раз — у 3 больных (6,6 %). Диареей в течение 1 сут страдали 39 (86,6%), 2 сут — 6 больных (13,4%), на боль в животе жаловались 78 больных (86,6 %), в том числе она была разлитого характера у 15 (19,2 %), с локализацией в эпигастрии — у 63 больных (80,8 %).
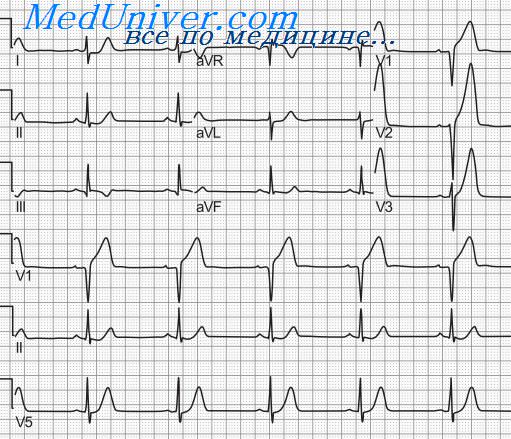
При поступлении в стационар повышенная температура тела была выявлена у 37 больных (41,1 %), у 4 она превышала 38 °С; боль в области сердца ангинозного характера наблюдалась у 82 больных (91,1 %), иррадиация ее в левую руку, лопатку и шею — у 58 (70,7 %); у 8 больных (8,9 %) боль в области сердца отсутствовала, чувство дискомфорта было незначительным. У 83 больных (92,2 %) изменения на ЭКГ соответствовали динамике указанных показателей при остром инфаркте миокарда, у 7 (7,8 %) для подтверждения диагноза потребовалось повторное электрокардиографическое исследование. Инфаркт передней стенки левого желудочка был выявлен у 16 больных (17,8 %), задней стенки — у 56 (62,2 %), иной локализации — у 18 (20 %), гемодинамические нарушения в 1-й день пребывания в стационаре зарегистрированы у 53 больных (58,9 %). В 1-е сутки количество лейкоцитов в периферической крови составляло 8,0-10,09/л – 10,0—10,09/л у 9 больных, 10,0-10,0% – 15,0-10,07/л у 28, свыше 15,0-10,09/л у 16 больных, увеличение СОЭ у 34 (37,8 %), в том числе в пределах 11—20 мм/ч у 18, свыше 20 мм/ч у 16 больных. В 1-е сутки пребывания в стационаре увеличение уровня ACT отмечалось у 5 из 12 обследованных пациентов, а гипергликемия, обусловленная повышенной секрецией катехоламинов, усиливающей гликогенолиз, и тормозящая секрецию инсулина, — у 16 из 27 пациентов, не страдавших прежде сахарным диабетом. В 1-е сутки инфаркт миокарда был диагностирован у 61 (67,8 %) из 90 больных, на 2—3-й сутки — у 26 (28,9 %) и только на секции — у 3 больных (3,3 %). Вышеизложенное подтверждает сложность диагностики заболевания. В помощь практическому врачу мы предлагаем схему дифференциальной диагностики инфаркта миокарда и пищевых токсикоинфекций. – Также рекомендуем “Инфаркт в разгар кишечной инфекции. Пневмония и кишечные инфекции” Оглавление темы “Дифференциация кишечных инфекций в практике врача”: |
Источник
Инфаркт в разгар кишечной инфекции. Пневмония и кишечные инфекции
Диагностика наиболее затруднена при распознавании инфаркта миокарда, развивающегося в разгар острой кишечной инфекции. Нами наблюдалось развитие инфаркта миокарда у 155 больных с пищевыми токсикоинфекциями, при этом ИБС отмечалась в анамнезе у 128 из них (82,6 %). Старше 60 лет было 96 пациентов (61,9 %).
По нашим наблюдениям, инфаркт миокарда, развившийся при острых кишечных инфекциях, имел некоторые особенности:
• острая кишечная инфекция возникала раньше инфаркта миокарда, чаще всего на 2—4 дня;
• чем тяжелее было течение острой кишечной инфекции, тем больше была вероятность развития инфаркта миокарда;
• инфаркт миокарда чаще всего развивается на фоне нарушенной гемодинамики, изменений водно-солевого обмена и кислотно-основного состояния (КОС);
• начало развития инфаркта миокарда бывает, как правило, “завуалированным”;
• боль локализовалась не только и не столько в области сердца, сколько в эпи- и мезогастрии;
• диарея, малохарактерная для “чистого” инфаркта миокарда, в этих случаях бывает отчетливо выраженной и не имеет тенденции к прекращению;
• диагностическую значимость приобретала динамика электрокардиографической картины и гиперферментемии (ACT, ЛДГ, КФК);
• диагностическую значимость теряли следующие показатели: лейкоцитоз крови; уровень гематокрита; выделение патогенных или условно-патогенных бактерий из испражнений больных.
Пневмония и кишечные инфекции
Значительные трудности возникают при проведении дифференциального диагноза между пищевыми токсикоинфекциями (сальмонеллезами) и крупозной пневмонией. Гипердиагностика пищевых токсикоинфекций может быть причиной тяжелых диагностических ошибок (например, остается нераспознанной крупозная пневмония).
Сложность диагностики обусловлена тем, что у больных крупозной пневмоний может развиться “абдоминальный синдром”, проявления которого имеют общие симптомы с сальмонеллезом. Кроме того, при крупозной пневмонии могут возникать осложнения (ИТШ), затрудняющие установление правильного диагноза.
Еще большая диагностическая трудность появляется тогда, когда крупозная пневмония осложняется коматозным состоянием с развитием отека мозга, проявления которого становятся доминирующими и оттесняют иные клинические симптомы на второй план.
Нами наблюдались 56 больных, направленных в стационар с диагнозом пищевой токсикоинфекции, у которых была выявлена также пневмония (лобарная — у 11, очаговая — у 45). Кроме того, у 7 пациентов с крупозной пневмонией наблюдался летальный исход. Абдоминальный синдром (рвота, боль в эпигастральной области, кашицеобразный или жидкий стул) зарегистрирован у всех 63 больных. Вместе с тем у подавляющего большинства наблюдавшихся больных (85,7 %) отсутствовала или была крайне слабо выражена симптоматика, характерная для пневмонии.
О возможности возникновения абдоминального синдрома при пневмониях сообщали Н.С.Молчанов и В В.Ставская (1971). Вместе с тем Е.Я.Северова и соавт. (1978) отмечали, что в последние годы острые пневмонии зачастую протекали без выраженных характерных перкуторных и аускультативных признаков и выявлялись преимущественно рентгенологически. Это вполне согласуется с мнением о том, что при крупозной пневмонии характерные аускультативные данные довольно долго не выявляются, так как уплотнение легочной ткани сравнительно поздно достигает периферических участков легких.
По данным М.К.Пермяковой и Т.Н.Бук (1978), острая пневмония не распознавалась на догоспитальном этапе (15,6 %) и в приемных отделениях больниц (10 %). Еще в большей мере это относится к пневмониям у лиц пожилого и старческого возраста.
У некоторых больных с пищевыми токсикоинфекциями (сальмонеллезами) развиваются пневмонии. Исходя из клинико-патогенетических особенностей последних, целесообразно выделить:
1) пневмонии в сочетании с пищевыми токсикоинфекциями (сальмонеллезами), т.е. микст-инфекцию;
2) пневмонии, развивающиеся у больных с септикопиемическим вариантом генерализованной формы сальмонеллеза;
3) пневмонии, возникающие у больных с острыми кишечными инфекциями, осложнеными инфекционно-токсическим шоком; 4) застойные ли гипостатические пневмонии у тяжелобольных.
В некоторых случаях проникновение микробов, вызывающих пневмонию, происходит из окружающей среды (“госпитальная инфекция”). Нами наблюдались 125 больных с пищевыми токсикоинфекциями, у которых клиническое течение заболевания осложнилось пневмонией: у 17 из них (11,2 %) пневмония возникла при ИТШ, у 135 (88,8 %) носила гипостатический характер. При ИТШ преобладал двусторонний воспалительный процесс в легких, при гипостатической пневмонии он локализовался преимущественно (75 %) в задних отделах легких.
У подавляющего большинства лиц пожилого и старческого возраста симптоматика пневмонии была значительно беднее, чем у лиц зрелого возраста, что существенно затрудняло диагностику. Частота развития гипостатической пневмонии коррелировала с тяжестью течения основного заболевания и возрастом больных.
– Также рекомендуем “Кишечные инфекции и гипертоническая болезнь. Обострение гипертонической болезни”
Оглавление темы “Дифференциация кишечных инфекций в практике врача”:
1. Кишечный трихомониаз. Кишечный лямблиоз
2. Балантидиаз и его проявления. Амебиаз в практике врача
3. Гименолепидоз. Трихоцефалез и его диагностика
4. Аскаридоз. Кишечный шистосомоз Мансона
5. Кишечная инфекция и инфаркт миокарда. Дифференциация инфекций с инфарктом миокарда
6. Инфаркт в разгар кишечной инфекции. Пневмония и кишечные инфекции
7. Кишечные инфекции и гипертоническая болезнь. Обострение гипертонической болезни
8. Неспецифический язвенный колит и кишечные инфекции. Дифференциация НЯК
9. Сахарный диабет и кишечные инфекции. Идиопатический кетоз в инфекционных болезнях
10. Хронический алкоголизм и кишечные инфекции. Абстинентный синдром в виде кишечной патологии
Источник
Инфаркт миокарда с клиникой кишечной инфекции. Гипертонический криз и токсикоинфекция
При дифференциальной диагностике пищевой токсикоинфекции следует иметь в виду ряд неинфекционных заболеваний, протекающих со сходной клинической симптоматикой. Особое место среди таких болезней занимает инфаркт миокарда (ИМ). Ответственность этого диагноза очевидна и возрастает еще от того, что такая важнейшая лечебная процедура при пищевой токсикоинфекции, как промывание желудка, больным инфарктом миокарда абсолютно противопоказана.
Необходимость дифференциального диагноза пищевой токсикоинфекции и инфаркта миокарда возникает в связи с возможностью его так называемого «гастралгического варианта». При этой форме инфаркта миокарда наблюдаются рвота, боль в подложечной области, особенностью которой являются иррадиация вверх и частое сочетание с интенсивной болью за грудиной, сопровождающейся чувством страха смерти (С В. Шестаков).

Тогда же, т.е. значительно позднее, чем при пищевой токсикоинфекции, появляется лейкоцитоз. При инфаркте миокарда позывы на рвоту более редки и, как правило, возникают при нормальном стуле Живот обычно безболезненный. В противоположность пищевой токсикоинфекциям при инфаркте миокарда урчание кишечника отсутствует. Печень увеличивается позднее и только при развитии недостаточности кровообращения. Селезенка не увеличивается.
Решающее значение имеют ЭКГ-исследования, выявляющие изменения, характерныедля инфаркта миокарда.
В первые часы заболевания диагноз пищевой токсикоинфекции нередко ставят при гипертоническом кризе и особенно при субарахноидальном кровоизлиянии. У больных с субарахноидальным кровоизлиянием наряду с резчаишей головной болью появляется рвота, что дает основание заподозрить пищевую токсикоинфекцию и ошибочно направить больного в инфекционный стационар. Отличительными симптомами субарахноидального кровоизлияния являются внезапное начало заболевания, ощущение удара и прилива тепла к голове.
Возможна кратковременная потеря сознания. Постепенно прогрессируют менингеальный синдром и другие симптомы поражения центральной нервной системы. Температура повышается позднее. Лицо больных часто гиперемировано. Живот безболезнен. Артериальное давление может быть повышено. В анамнезе у больных обычно имеются гипертоническая болезнь, атеросклероз сосудов головного мозга. Провоцирующими факторами могут быть травмы, физическое перенапряжение, перегревание на солнце. При люмбальной пункции удается получить кровянистый ликвор с признаками ксантохромии после его центрифугирования или отстаивания, что является абсолютным подтверждением диагноза субарахноидального кровоизлияния.
– Также рекомендуем “Острый живот и кишечные инфекции. Основные причины диареи”
Оглавление темы “Современное выявление острой кишечной инфекции”:
1. Диагноз острой кишечной инфекции. Пищевая токсикоинфекция
2. Дифференциация пищевой токсикоинфекции (ПТИ). Дифференцировка острой дизентерии
3. Формы пищевой токсикоинфекции. Причины пищевой токсикоинфекции
4. Редкие формы токсикоинфекций. Соматическая патология с клиникой токсикоинфекции
5. Кишечный сепсис. Дифференциация ботулизма и пищевой токсикоинфекции
6. Дифференциация вирусных поражений и пищевых токсикоинфекций. Пищевые интоксикации – отравления
7. Диагностика острой кишечной инфекции. Выявление причины кишечной инфекции
8. Инфаркт миокарда с клиникой кишечной инфекции. Гипертонический криз и токсикоинфекция
9. Острый живот и кишечные инфекции. Основные причины диареи
10. Наследственные причины диареи. Синдромы сопровождающиеся диареей
Источник
Причины инфаркта при кишечных инфекциях. Инфекционно-токсический шокПроводилось изучение причин развития инфаркта миокарда у больных с пищевыми токсикоинфекциями. По нашим наблюдениям, он выявлялся у 0,4 % больных с острыми кишечными инфекциями. В то же время, согласно статистическим данным, он встречался у лиц, не страдавших этими инфекциями, в 4 раза реже. У всех наблюдавшихся больных инфаркт миокарда возник в остром периоде кишечной инфекции. Факторами, способствующими его развитию, по нашему мнению, являлись гиповолемия, гемодинамические нарушения, повышенная вязкость крови, метаболический ацидоз, электролитные нарушения, диссеминированная внутрисосудистая коагуляция. В анамнезе у 88,5 % указанных больных отмечалась ИБС. У лиц, страдающих хроническим алкоголизмом, возникновение острой кишечной инфекции, как правило, приводило к прекращению или значительному уменьшению приема алкоголя, в связи с чем развивался абстинентный синдром, который у части больных эволюционировал в металкогольный психоз. Причиной развития абстинентного синдрома у больных хроническим алкоголизмом в условиях прекращения приема алкоголя является нормализация распада катехоламинов при сохраняющемся усиленном их синтезе, что приводит к существенному повышению содержания дофамина в мозге. Таким образом, острые кишечные инфекции, в том числе пищевые токсикоинфекции, являются факторами риска возникновения некоторых острых хирургических заболеваний органов брюшной полости (аппендицит, холецистит, панкреатит), а также обострения некоторых хронических заболеваний (гипертоническая болезнь, ИБС, НЦД, желчнокаменная болезнь, спаечная болезнь брюшной полости, сахарный диабет, хронический пиелонефрит, хронический алкоголизм). Инфекционно-токсический шокИнфекционно-токсический шок (ИТШ) является наиболее тяжелым осложнением острых кишечных инфекций и главной причиной неблагоприятного исхода заболевания.
Гиповолемический вариант ИТШ развивается при острых кишечных инфекциях на фоне обезвоживания III—IV степени (по В.И.Покровскому). Обезвоживание носит изотонический характер. При этом возникает патологический каскад, обусловливающий клиническую симптоматику потеря изотонической жидкости и электролитов приводит к уменьшению объема плазмы и интерстициальной жидкости, нарушениям микроциркуляции, гипоксии, ацидозу, полиорганной недостаточности, прежде всего к поражению почек. Наиболее часто ИТШ с выраженным обезвоживанием наблюдается при тяжелом течении холеры, но может возникать и при пищевых токсикоинфекциях, сальмонеллезах и эшерихиозах. ИТШ без выраженного обезвоживания с преобладанием токсикоза чаще всего наблюдается при тяжелом течении сальмонеллеза, дизентерии и пищевых токсикоинфекций. Он представляет собой сложный патологический процесс, возникающий в результате действия экстремального фактора, связанного с прорывом инфекта в кровь, что вызывает наряду с повреждением органов и тканей чрезмерное и неадекватное напряжение неспецифических механизмов адаптации. При этом наблюдаются сдвиги гомеостаза до уровня, несовместимого с жизнью из-за развития гипоксии, ограничения перфузии тканей и глубокие расстройства обменных процессов, отчетливо прослеживаются следующие изменения: Необходимо иметь в виду, что ИТШ развивается далеко не всегда при тяжелом течении острой кишечной инфекции. Основным условием его развития является генерализация инфекции. По мнению В.И.Покровского (1978), для генерализации инфекции необходимы определенный преморбидный фон, генотипические и фенотипические особенности организма, дефекты иммунного гомеостаза и адаптационно-компенсаторного синдрома защиты организма. Возникновению ИТШ способствует антибиотикотерапия препаратами бактерицидного действия, вызывающая массовую гибель бактерий и приводящая к освобождению большого количества эндотоксинов. Летальность при ИТШ высокая и, по данным ряда авторов , достигает 70-90 %. Существуют и иные точки зрения на патогенез ИТШ. Так, по мнению Н К Пермякова и соавт. (1987), ИТШ вероятнее всего развивается вследствие общерезорбтивного действия токсинов, чем генерализации инфекции Морфологическими критериями шока Н.К.Пермяков (1989) считает: 1) некротически-гнилостные изменения в первичном очаге; 2) преимущественно грамотрицательную флору; 3) апоплексию коры надпочечников; 4) некроз гипофиза; 5) кортикальный некроз почек; 6) фибринолиз; 7) появление петехиальной сыпи; 8) наличие ареактивной селезенки. Однако при инфекциях, протекающих с отчетливым общерезорбтивным действием токсинов ботулизма и столбняка, ИТШ не развивается. – Также рекомендуем “Критерии инфекционно-токсического шока. Степени ИТШ” Оглавление темы “Осложнения кишечной инфекции”: |
Источник