Кишечная непроходимость и каловый перитонит
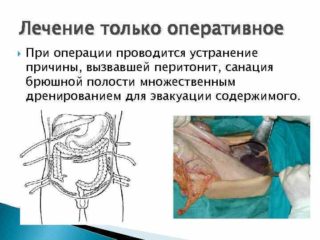
Нарушения моторной функции тонкой кишки при перитоните и кишечной непроходимости многие исследователи рассматривают как биологически оправданную рефлекторную защитную реакцию, первопричиной которой служит нервно-рефлекторное тормозное воздействие, возникающее вследствие раздражения интерорецепторов по типу висцеро-висцеральных рефлексов [50]. Начальный механизм этой реакции связан с нарушением нейрогуморальной регуляции моторики кишечника в виде дисбаланса между влиянием симпатической и парасимпатической нервных систем. Под воздействием усиленного выброса катехоламинов происходит деполяризация мембран клеток гладкомышечных волокон кишечной стенки с последующей их трансминерализацией. Снижается активность холинергических систем. Повышается чувствительность нервных центров к афферентной импульсации. Активация калликреинкининовой системы и избыточное накопление гистамина, брадикинина, протеолитических ферментов и других биологически активных веществ подавляет функцию энтерорецепторов, водителей ритма сокращений и пропульсивную активность кишечника. Резкое сокращение продукции серотонина энтерохромаффинными клетками подслизистого слоя кишечника тормозит передачу нервного импульса от синапса к гладкой мышце кишки. Потери электролитов и прежде всего калия усиливают и закрепляют первоначальный эффект патологических рефлексов. Вследствие увеличения содержания внутриклеточного натрия и уменьшения количества калия происходит деполяризация мембраны клетки, что снижает реактивность гладкой мускулатуры и нервного аппарата кишечной стенки, подавляя моторику кишки.
Таким образом, угнетение двигательной активности, прекращение эвакуации содержимого, скопление в просвете тонкой кишки больших объемов жидкости и газов служат пусковыми механизмами пареза кишечника. По мере прогрессирования гнойно-воспалительного процесса в брюшной полости или нарастания кишечной непроходимости в силу вступают новые патологические механизмы, которые способствуют поддержанию и прогрессированию пареза и формируют синдром энтеральной недостаточности. Ведущим из них является нарастающая гипоксия.
Гипоксия кишечной стенки при перитоните и кишечной непроходимости носит смешанный и многокомпонентный характер. Патогенетическую основу ее составляют глубокие расстройства внешнего дыхания, гемодинамики, микроциркуляции и метаболизма.
Легкие по мере прогрессирования перитонита и кишечной непроходимости становятся одним из первых органов, которые подвергаются повреждению. Происходит разрушение сурфактантной системы, коллапс альвеол, развиваются интерстициальныи отек и диффузные ателектазы, уменьшается дыхательная поверхность легких. В результате перерастяжения кишечника содержимым и газами повышается внутрибрюшное давление, ограничивается экскурсия диафрагмы, что также способствует сокращению дыхательной емкости легких. Развиваются синдром острой дыхательной недостаточности и артериальная гипоксемия.
Секвестрация крови в потерявших тонус внутриорганных сосудах, снижение венозного возврата и падение ударного объема сердца в результате воздействия микробного фактора и эндотоксинов на миокард, баро- и хеморецепторы вен приводят к гипокинетическому состоянию центральной гемодинамики. В свою очередь прогрессирующее снижение объема циркулирующей крови и ее компонентов (плазменного и глобулярного объемов), массивная диффузия жидкости в брюшную полость, просвет желудка и кишечника ведут к стойкой гиповолемии. Развивается диспротеинемия. Происходит снижение в крови уровней АТФ, креатинфосфата, сахара, гликогена и, как следствие, возникает дефицит энергетических ресурсов организма.
Изменение характера органного кровотока в виде замедления его скорости, открытия артериоло-венулярных шунтов и выпадения из кровообращения части микрососудистой сети, ухудшения реологических свойств крови (увеличение вязкости, уменьшение текучести, агрегация форменных элементов, склонность к внутрисосудистому свертыванию), перивазальные изменения в виде отека тканей, лейкоцитарной инфильтрации и микрогеморрагии способствуют глубоким нарушениям микроциркуляции в кишечной стенке.
Гемоциркуляторные расстройства ухудшаются по мере повышения внутри-полостного кишечного давления. На основании изучения интрамурального кровотока установлено, что критическое давление в просвете кишки составляет 30 мм рт. ст. При повышении давления до 40-60 мм рт. ст. почти вся кровь минует интрамуральную капиллярную сеть и шунтируется в венозное русло.
Нарушения регионарного; кровообращения и микроциркуляции ведут к недостаточной доставке кислорода и энергетических веществ к тканям стенки кишки, в результате чего развиваются вторичная тканевая гипоксия и глубокие нарушения метаболических процессов. Снижается активность дыхательных ферментов клетки, уменьшается образование макроэргов. Активизируются распад тканевых липидов, катаболизм белков, дезаминирование и переаминирование аминокислот.
Происходят активация перекисного окисления липидов, нарушение функций клеточных мембран, митохондрий и лизосом. Инактивируются ферментные системы клетки. Вследствие нарастающей циркуляторной гипоксии кишечной стенки постепенно утрачивается возможность передачи импульсов по интрамуральному нервному аппарату, а мышечные клетки в результате глубоких метаболических расстройств становятся неспособными воспринимать импульсы к сокращению. При этом структурные изменения обнаруживаются не только в интрамуральном нервном аппарате, но и в солнечном сплетении – экстрамуральном аппарате.
С развитием пареза и задержкой пассажа кишечного содержимого происходят интенсивный рост и изменение микрофлоры тонкой кишки.
В нормальных условиях двенадцатиперстная, тощая и проксимальная часть подвздошной кишки содержат относительно немногочисленную микрофлору, состоящую в основном из грамположительных факультативных микроорганизмов. Последние представлены чаще всего стрептококками, анаэробными лактобациллами, дифтероидами и грибами. Их общая концентрация обычно не превышает 10000 микроорганизмов в 1 мл кишечного содержимого. В дистальной части подвздошной кишки примерно у 60 % здоровых людей обнаруживаются в существенных концентрациях грамотрицательные микроорганизмы, такие как аэробные колиформные бактерии, анаэробные бактероиды, бифидо- и фузобактерии, клостридии, количество которых начинает превышать грамположительные виды.
Наряду с нормальной кислотностью желудочного сока высокоэффективным механизмом защиты против избыточной колонизации тонкой кишки служит мигрирующий моторный комплекс [378].
Под синдромом избыточной колонизации (СИК) понимают патологическую колонизацию тонкой кишки более стабильными и более разнообразными популяциями, схожими по качественному составу с микрофлорой толстой кишки и фекалий. На фоне острой кишечной непроходимости (независимо от ее этиологии) СИК развивается у 100 % больных, при этом отмечается увеличение концентрации аэробов и анаэробов. Синдром избыточной колонизации в классическом варианте с развитием ярких клинических симптомов энтеральнои недостаточности (стойкая потеря массы тела, постоянные диарея и анемия) сопутствует хроническому нарушению пассажа по тонкой кишке (спаечная болезнь, болезнь Крона, органические формы дуоденостаза).
Благоприятные условия для избыточной колонизации создают любые оперативные вмешательства с формированием длинных приводящих или отключенных петель тонкой кишки.
Клинически синдром избыточной колонизации тонкой кишки протекает в форме энтеральнои недостаточности, проявляющейся мальабсорбцией, которая может касаться одного или нескольких веществ: белков, углеводов, жиров, воды, электролитов, витаминов или желчных кислот.
Мальабсорбция при СИК не является результатом действия каких-либо патогенных микробов. Патологически разросшаяся микрофлора действует в просвете кишечника путем конкурентной метаболизации пищевых субстратов и секрета кишки, нарушая таким образом процессы полостного пищеварения и переваривания пищевых веществ за счет ферментов, адсорбированных в слизистых наложениях. Кроме того, имеются данные о поражении микробами щеточной каймы и гликокаликса энтероцитов, в результате чего нарушаются процессы мембранного пищеварения и всасывания.
Нарушение всасывания белков при СИК возникает вследствие разрушения пищевых белков, функциональных расстройств слизистой оболочки со значительным уменьшением всасывания аминокислот, а также из-за энтеропатии с потерей белков.
Мальабсорбция углеводов при СИК также относится к многофакторным процессам, включающим внутриполостной бактериальный катаболизм и нарушение всасывания. В аспиратах из тонкой кишки больных с СИК обнаружен высокий уровень летучих жирных кислот – продуктов бактериальной ферментации углеводов. Доказано, что некоторые виды бактерий, особенно В. fragilis, С. perfringens и S.faecalis, содержат протеазы, способные удалять мальтазу из щеточной каймы, а некоторые виды бактероидов образуют протеазы, разрушающие дисахаридазы щеточной каймы энтероцитов человека [378].
Наиболее частое проявление СИК тонкой кишки – мальабсорбция жиров, которая клинически проявляется стеатореей. В тяжелых случаях СИК с фекалиями выделяется больше жиров, чем поступает с пищей. Наиболее важным механизмом этого расстройства является нарушение метаболизма желчных кислот. При наличии способных к деконъюгации бактерий концентрация связанных желчных солей снижается, что приводит к недостаточному образованию мицелл, мальабсорбции жиров и стеаторее.
Одним из клинических проявлений СИК является макроцитарная анемия, возникающая из-за мальабсорбции витамина В12. Нарушение метаболизма жирных кислот может приводить к нарушению всасывания жирорастворимых витаминов A, D, К.
Таким образом, СИК тонкой кишки развивается значительно чаще, чем диагностируется, так как в большинстве случаев он протекает кратковременно и на субклиническом уровне. В широкой клинической практике вероятность развития СИК очень высока при следующих состояниях: в ранние сроки после травматичных операций на органах брюшной полости, особенно в условиях пареза кишечника; на фоне послеоперационной гипо- или ахлоргидрии, развивающейся после резекции желудка, ваготомии, гастрэктомии; при длительном голодании у больных со стенозом выходного отдела желудка и двенадцатиперстной кишки; при обширных ожогах, сепсисе и инфекционных заболеваниях желудочно-кишечного тракта. При сочетании перечисленных патологических состояний, при кишечной непроходимости и разлитом перитоните, независимо от их этиологии, СИК тонкой кишки развивается во всех случаях. Это обстоятельство значительно усугубляет и без того имеющиеся нарушения полостного пищеварения, переваривания в слоях слизи, мембранного пищеварения и всасывания, которые в свою очередь способствуют прогрессированию СИК.
Утрачивается антагонистическая активность по отношению к патогенным микроорганизмам. Усиленное их размножение и активное функционирование нарушают транспорт электролитов и усиливают секрецию в просвет кишки. Избыточная колонизация тонкой кишки микрофлорой толстокишечного типа приводит к ослаблению противомикробной защиты на фоне снижения барьерных функций эпителия, лимфатической и ретикулоэндотелиальной систем. Происходит адгезия микробов к кишечному эпителию с последующим внедрением в энтероциты, под базальную мембрану и собственную пластинку. Эндотоксины энтеробактерий, поступая в кровь и лимфу, оказывают нейро- и капилляротоксическое действие. В результате застоя содержимого в просвете кишки создаются благоприятные условия для активизации гнилостных и бродильных процессов. Происходит избыточное образование высокотоксичных веществ: индола, скатола, кадаверина и др. Повреждающим эффектом на кишечную стенку обладают и образующиеся в процессе микробного метаболизма аммиак и сероводород. Посредством гидролитических ферментов кишечных бактерий происходит замена собственного пищеварения симбионтным и интенсивное образование биологически активных среднемолекулярных пептидов. Их низкомолекулярные фракции, поступая в кровь и лимфу, усиливают расширение микрососудов и проницаемость капиллярной стенки, угнетают сократительную способность мышечного аппарата кишечника.
Нарушение микроциркуляции и непосредственное воздействие микробов и токсических веществ на слизистую оболочку приводят к нарушению барьерной функции тонкой кишки и проникновению бактерий и токсинов не только в кровоток, но и в полость брюшины. Кишечник становится основным источником эндогенной интоксикации и токсемии. Развивается состояние, которое может быть охарактеризовано как универсальная энтеральная недостаточность, разрешить которую возможно лишь путем патогенетического лечения. Одним из важных элементов такого лечения является декомпрессия тонкой кишки, длительное ее дренирование с проведением детоксикационной и корригирующей интестинальной терапии, в том числе полноценного энтерального зондового питания.
A. Kypыгинa, Ю. Cтoйкo, C. Бaгнeнкo
Перитонит и кишечная непроходимость и другие материалы по хирургической гастроэнтерологии.
Читайте также в этом разделе:
- Дренирование тонкой кишки
- Вся информация по этому вопросу
Источник
Каловым перитонитом называют патологию, при которой в брюшную полость попадают фрагменты кала и вызывают в ней острый воспалительный процесс. Он быстро прогрессирует и вызывает множество опасных для организма человека состояний. Заболевание требует незамедлительного эффективного лечения. Подробная схема терапии описана в Международной классификации болезней 10-го пересмотра. Код по МКБ калового перитонита — K65.0. При несвоевременной медицинской помощи смертность от недуга очень высока.
Этиология заболевания
 Поражение серозной оболочки брюшины — сложное заболевание. Оно вызывает нарушение сразу нескольких функций полости: защитной, обменной и экссудативной. При развитии калового перитонита происходит воспаление соседних участков и их отек, отравление кишечника токсическими веществами, обезвоживание и отравление всего организма.
Поражение серозной оболочки брюшины — сложное заболевание. Оно вызывает нарушение сразу нескольких функций полости: защитной, обменной и экссудативной. При развитии калового перитонита происходит воспаление соседних участков и их отек, отравление кишечника токсическими веществами, обезвоживание и отравление всего организма.
Причины калового перитонита:
- нарушение целостности кишечника;
- длительный инфекционный процесс в ЖКТ;
- дивертикулез;
- ущемление грыжи;
- кишечная непроходимость.
К бактериям, вызывающим инфицирование пищеварительного тракта, относят:
- синегнойную палочку;
- энтеробактерии;
- кишечную палочку;
- стафилококк и др.
Располагающими к формированию перитонита факторами являются также хронические патологии ЖКТ (гастрит, энтерит, колит), воспалительные заболевания поджелудочной железы и печени. В некоторых случаях попадание каловых масс в брюшную полость может быть последствием механической травмы живота, влекущей за собой разрыв тканей кишечника.
Классификация
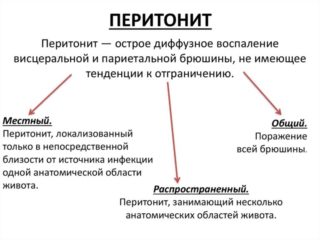
Данный вид перитонита — вторичное гнойное воспаление в брюшной полости. В зависимости от степени распространения принято выделять:
- местный;
- диффузный;
- разлитой.
В первом случае страдает только небольшой участок тканей. При диффузном перитоните воспаление поражает от 2 до 5 областей, а при тотальном — охватывает всю брюшную полость.
Клиническая картина калового перитонита
 Формирование воспаления происходит стремительно. Болезнь развивается в несколько стадий: от реактивной до терминальной. Лучше всего она поддается лечению в срединной фазе — реактивной. На терминальной организм уже перестает бороться с инфекцией и многие органы не могут полноценно выполнять свои функции даже при поддерживающей терапии.
Формирование воспаления происходит стремительно. Болезнь развивается в несколько стадий: от реактивной до терминальной. Лучше всего она поддается лечению в срединной фазе — реактивной. На терминальной организм уже перестает бороться с инфекцией и многие органы не могут полноценно выполнять свои функции даже при поддерживающей терапии.
В числе симптомов разлитого и местного калового перитонита выделяют:
- острые кинжальные боли в местах локализации;
- постепенное распространение болевого синдрома на всю стенку брюшины;
- бледная кожа с синюшным или серым оттенком;
- липкий пот;
- субфебрильная температура;
- выраженная слабость, сонливость.
Перистальтика при перитоните нарушается, живот вздувается, появляется тошнота и рвота. При пальпации передняя брюшная стенка напряжена. У больного наблюдается учащенный пульс, низкое артериальное давление, одышка. Он пытается лечь на бок и притянуть ноги к животу, чтобы снизить дискомфорт.
На терминальной стадии калового перитонита черты лица заостряются, язык покрывается темным налетом. Болевые ощущения затихают, пульс становится нитевидным.
У детей признаками калового перитонита являются постоянный плач, отказ от груди, напряжение брюшной стенки, температура, примеси крови в стуле. У пожилых пациентов, напротив, напряжение брюшной стенки наблюдается лишь в 34% случаев, а от болей страдают только половина пациентов. Симптоматика очень скудная, почти отсутствует.
Диагностика
 Болезнь относится к группе состояний под общим названием «острый живот». Чтобы поставить точный диагноз, проводится глубокая пальпация. При наличии патологии возникают специфические симптомы:
Болезнь относится к группе состояний под общим названием «острый живот». Чтобы поставить точный диагноз, проводится глубокая пальпация. При наличии патологии возникают специфические симптомы:
- Щепкина-Блюмберга;
- Берштейна;
- Менделя.
Они сопровождаются значительным напряжением мышц передней стенки живота. Положительный результат говорит о наличии перитонита у больных. Перкуссия живота и прослушивание брюшной полости обнаруживают притупление звука и резкое снижение или исчезновение кишечных шумов.
Ректальное или вагинальное исследование с помощью лапароскопа косвенно помогает предположить перитонит.
Если клинические проявления болезни стерты, может понадобиться более подробный аппаратный анализ:
- УЗИ;
- рентген;
- компьютерная томография;
- МРТ кишечника.
Применение перечисленных методов диагностики позволяет обнаружить выпотную жидкость, свободные газы, ограничение движения диафрагмы и другие признаки болезни.
Все обследования должны быть проведены гастроэнтерологом в неотложном порядке, если состояние пациента критично. При неточных показаниях брюшная стенка будет вскрыта оперативным путем для обследования.
Методы терапии
 Каловые перитониты требуют многоэтапной хирургической санации и комплексного медикаментозного лечения. Все мероприятия проводятся в условиях стационара.
Каловые перитониты требуют многоэтапной хирургической санации и комплексного медикаментозного лечения. Все мероприятия проводятся в условиях стационара.
Операция при этом заболевании носит экстренный характер и состоит из нескольких этапов:
- Введение наркоза больному.
- Поиск источника заражения.
- Удаление воспалительного очага.
- Восстановление целостности кишечника.
- Очищение и санация брюшной полости.
Современная медицина рекомендует использовать для лечения калового перитонита плазмофорез, экстракорпоральную детоксикацию, энтеросорбацию, гемодиализ.
Дальнейшая терапия состоит из курса антибиотиков широкого спектра действия, обезболивающих, сорбентов, успокоительных. Учитывается, что микрофлора имеет резистентный характер и плохо поддается массивной антибактериальной терапии. Длительное время пациенты соблюдают диету. Их меню состоит из пищи, приготовленной отварным способом или на пару. Исключаются овощи, повышающие газообразование, сладости и прочие раздражающие кишечник продукты. По мере восстановления функции кишечника рацион пополняется новыми блюдами.
Возможные осложнения и последствия
Осложнения калового перитонита:
- множественные абсцессы;
- сепсис;
- кишечная непроходимость;
- спаечная болезнь;
- образование кишечных фистул;
- увеличение давления в брюшной полости.
Крайней степенью негативных последствий является летальный исход.
Профилактические меры и прогноз
Предотвратить воспалительное заболевание можно, своевременно обратившись к врачу по поводу хронических болезней желудочно-кишечного тракта. Необходимо пройти полный курс лечения и не пренебрегать правилами здорового образа жизни. Особенно важно сбалансировать рацион, питьевой режим и отказаться от губительных привычек.
При каловом перитоните летальность составляет 20-40%. Важную роль играет своевременное лечение со стороны специалиста по гастроэнтерологии. При местном перитоните шансы на излечение выше, чем у диффузных форм. Последние, по статистике, в большинстве случаев приводят к смерти.
Детский каловый перитонит заканчивается летальным исходом у 78% пациентов. Это связано с тем, что патология протекает агрессивнее, в отличие от взрослого организма. Ситуация также осложняется невозможность доктора собрать полный анамнез. Больной ребенок не в состоянии своевременно показать и рассказать, что и где у него болит.
Наивысшую летальность имеют пациенты пожилой возрастной группы. Показатель связан с отсутствием симптомов и невозможностью определить патологию до начала необратимых процессов в организме.
Источник