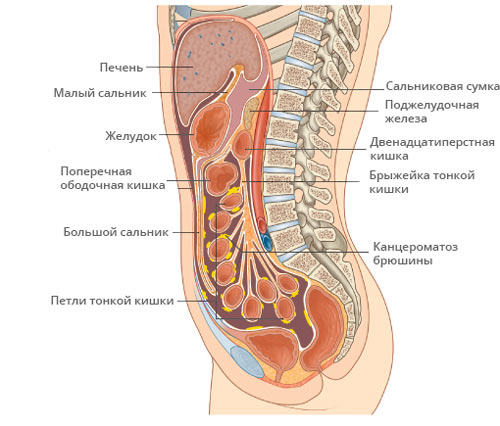
Кишечная непроходимость при канцероматозе
Здравствуйте, Марк Азриельевич!
1. Диагноз – ноябрь 2008 г. – рак желудка (перстневидно-клеточный), тотальное поражение (T3N0M0). Операция (после 2-х курсов неадъювантной химиотерапии): гастрэктомия, спленэктомия, лимфодиссекция Д2.
6 марта 2012 – выполнена подвесная трансверзостомия по поводу острой толстокишечной непроходимости.
23 апреля 2012 – выполнена диагностическая лапаротомия. Интрооперационно выявлен канцероматоз брюшины. Множественные увеличенные лимфоузлы в брыжейке тонкого кишечника. Взята биопсия (мтс узел), результат еще не пришел.
2. Общий анализ крови (26.04.12): эритроциты – 5.42 млн., гемоглобин – 170 г/л, тромбоциты – 286 тыс., лейкоциты – 14.4 тыс., лим. – 12.3%, ГРА – 82.6%, МИД – 5.1%, СОЭ – 25 мм/ч.
Общий анализ мочи (26.04.12): цвет – св.желтый, прозрачность – неполная, относительная плотность – м/м, реакция – кислая, белок – 0.36 г/л, глюкоза – отр., лейкоциты – 50-55 в поле зрения, эритроциты – нет.
Биохимический анализ крови от 26.04.12 г.: общий белок – 65 г/л, мочевина – 7.4 ммоль/л, креатинин – 124 мкмоль/л, натрий – 137 нм/л, калий – 4.9 нм/л, билирубин – 13 мкмоль/л, алат – 15, асат – 30, амилаза – 110 ед/л, глюкоза – 5.4 ммоль/л.
Группа крови: А(II), Rh – положит., KELL – отриц.
Ro легких, 16.04.12 – легочные поля прозрачны, корни легких – структурны, диафрагма – подвижна, синусы свободные.
Ro брюшной полости, 16.04.12 – свободного газа и уровней жидкости не выявлено.
Ro брюшной полости, 20.04.12 (контроль пассажа бария через 12 ч.) – барий в тонкой и частично в правых отделах ободочной кишки. Уровней жидкости нет.
КТ органов брюшной полости, 19.04.12 – контуры органов плохо контурируются из-за скопления жидкости, повышенной плотности мезентериального жира (отек брыжейки с асцитом). Лимфоузлы брюшной полости и забрюшинного пространства не увеличены. В просвете толстой кишки значительное количество калового содержимого и следы контрастного препарата. Петли тонкой кишки резко расширены до 44 мм, стенки и складки ут олщены до 4.3 мм. Пневматизация петель толстой кишки не нарушена. Заключение – признаки частичной тонкокишечной непроходимости, отека брыжейки и асцита. Данных за объемное образование органов брюшной полости и брюшины нет. Гепатомегалия. Хронический холецистит.
УЗИ органов брюшной полости, 18.04.12 – поджелудочная железа не увеличена, однородная, средней эхогенности. Билиарная сеть не расширена. Холедох 5 мм. Желчный пузырь 5.3 х 1.5 см, стенки 2 мм, в просвете неоднородное содержимое. Селезенка удалена. Во всех отделах брюшной полости петли кишечника расширены с жидкостным компонентом, вялой перистальтикой. Между петлями тонкие жидкостные полоски. В мезогастрии слева измененный участок кишечника.
ЭГДС, 19.04.12 – пищевод свободно проходим. Слизистая его н/3 мелкопятнистая с участками гиперемии. Пищеводно-кишечный анастомоз свободно проходим. Слизистая кишок без особенностей. Большое количество жидкости в отводящей кишке.
Тонкокишечная непроходимость.
3. 37 лет, рост 176, вес – 55 кг (15 апреля), в сознании, адекватен, встает мочиться самостоятельно. Псориаз. Аллергия не наблюдалась.
4. Боли нет.
5. Постоянная «рвота» (самостоятельно встает, наклоняется над раковиной – желчь с кишечными соками практически свободно вытекает). При этом ничего не ест, практически не пьет. Сначала намеренно «сливает» желчь, потом грамм 100 чая или молока пьет, минут 30 пытается «держать» в себе, рвет.
Очень обессилен – встает только до туалета (мочится раза 2 в день), до раковины в палате. Даже по телефону разговаривает с трудом.
6. Обезболивание не требуется.
7. Поскольку не ест, не пьет – в день: натрия хлорид (500 мл), глюкоза (500 мл), глюкоза (500 мл) + аминоплазмаль (500 мл). По какой-то причине три дня не назначали аминоплазмаль. Буквально за день муж «потух». Как только продолжили капать – практически сразу оживился. 2 раза в день колят антибиотики (?), вечером снотворное (?). Все равно полноценного сна не получается – от приступа рвоты просыпается. Пободрствует немного, устает, подремет… и так целый цень.
8. Место проживания – Москва.
27 апреля с Вами по телефону разговаривала по поводу перевода мужа из больницы к Вам в отделение. Муж не хочет (врачи – вселяют надежду, что кишечник заработает). Говорит, что очень голоден, ел бы и ел, а не «проваливается»…
Можно ли мужу дополнительно, для бОльших сил, какие-нибудь комплексы аминокислот? Каких? Возможно, есть какие-нибудь препараты, препятствующие образованию желчи, кишечных соков (чтоб не рвало)? Нужно ли что-либо для уменьшения интоксикации организма?
Как еще можно улучшить качество жизни человеку?
Спасибо.
Источник
анонимно
Здравствуйте, уважаемая Елена Сергеевна!
Моя родственница 72 лет в августе 2013 года перенесла операцию.Рак матки 3 стадии. Прошла 4 курса химиотерапии амбулаторно.
3 января 2014 года – последняя химиотерапия.
Еле дошла домой. С этого момента состояние ее начало ухудшаться. Плохо работал кишечник. 18 января 2014 года ей стало совсем плохо. Отсутствие стула. Тошнота. Каловая рвота.
Вызвали скорую. Но мою родственницу не пустили дальше приемного покоя. Сказали мест нет. Это было в субботу. Сделали
капельницу. В понедельник отправили в хоспис с диагнозом канцероматоз брюшины. Каловая рвота – симптом кишечной непроходимости. В больнице не стали делать срочную операцию. Сказали – бесполезно. Ваше мнение Можно ли делать операцию
по устранению кишечной непроходимости с канцероматозом брюшины. Как ее лечить? Подскажите, пожалуйста, врача в Москве. Галина.
хирург-онколог, детский хирург
Доброго времени суток.
Постараюсь интерпретировать данные, которые вы приложили.
3 стадия, согласно стадированию бывает различная. Для этого необходимы онкологические индексы TNM. При 3 стадии заболевания ( из 4- х возможных) высоко вероятен риск метастазирования опухоли. Согласно стандартам лечения онкологических пациентов выполняется операция + системная химиотерапия.
В каком лечебном учереждении вам проводилость оперативное лечение? Причин возникновения клиники кишечной непроходимости две.
1. спаечная кишечная непроходимость ( но учитывая проведенную операцию в августе 2013г. для спаечной непроходимости уже все сроки ушли. 2. Канцероматоз брюшины. Если основная причина кишечной непроходимости канцероматоз, то постоновка вопроса о проведении оперативного лечения сложна. Канцероматоз представляет собой поражение париетальной и висцеральной брюшины ( т.е стено брюшной полости и всех состояющиъ структур брюшной полости клетками опухоли . Обычно это имптантационные или гематогенные метастазы. В итоге происходит как бы ” склеивание” всех структур брюшной полости между собой, менастазы прорастают ткани сливаясь между собой. В ходе этого процесса получается неразделимы конгломерат состояший из органов , в первую очередь из тонкой и ободочной кишки.
Опреация при канцероматозе заключается в ” выведении кишки на живот” т.е стомы. если все “склеино” то не возможно вывести данные стомы без определенных проблем. Единственное что смущает меня в вашем письме- это появление “каловой рвоты”( т.е темная зловонная рвота с калоым запахом. Ранее в августе( в плане дообследования) вам проводилась фиброколаноскопия ( исследование ободочной кишки) на предмет исключени я патологии толстой кишки.
Истинная каловая рвота возникает , когда имеется припятствие в восходящем , поперечном отделе кишки.
В плане дообследования выполнялось ли : рентген обзорный снимок брюшной полости или компьютерная томография ( МСКТ ) брюшной полости, для определения канцероматоз ли это, так же возможно выявить уровень препятствия для каловых масс и возможную опухоль в ободочной кишке.
В настояшее время необходимо установить назогастральный зонд ( трубка установленная через нос) для того чтобы излишки по ней выходили из желудка. Питаться только жидками морсами и больонами, а возможно только внутривенным питанием.
Данных не достаточно для определения, что вызвало кишечную непроходимость / нарушение пассажа по кишке. ( не определена причина) конечно , ссылаться на канцероматоз проце всего, т.к человек пролечен по поводу рака. Обратитесь на консультацию в РОНЦ ( российский онкологический центр)- ведь отказать в консультации онкологическом убольному они не имеют права.
Всего вам доброго. С уважением Елена Сергеевна
Консультация врача онколога на тему «Кишечная непроходимость» дается исключительно в справочных целях. По итогам полученной консультации, пожалуйста, обратитесь к врачу, в том числе для выявления возможных противопоказаний.
Источник
Канцероматоз брюшины — опухолевое поражение листков слизистой оболочки, покрывающей органы и внутреннюю стенку живота. Преимущественно обусловлен разрастанием метастазов рака в брюшной полости, иногда возможно развитие первичного злокачественного процесса — мезотелиомы в самой брюшине.
Метастатическое поражение правильнее называть «карциноматоз», поскольку карцинома — синоним рака. Аналогично метастазы саркомы в брюшину именуют «саркоматоз».
Частое, но не обязательное проявление перитонеального канцероматоза, — выработка асцитической жидкости. С асцитом или без, но поражение брюшины злокачественным процессом всегда угрожает жизни больного и требует очень непростого лечения.

Причины канцероматоза брюшины
Не всякая оторвавшаяся от материнской раковой опухоли клетка способна стать метастазом, в кровеносном русле погибает львиная доля циркулирующих злокачественных клеток. Для обретения способности стать метастазом раковая клетка должна измениться внутренне — научиться вырабатывать вещества, позволяющие самостоятельно жить и внедриться в другом месте, подавляя нормальные клетки.
Оторвавшиеся от узла клетки мигрируют на большие расстояния, раздвигая нормальные клетки, имплантируются в брюшную слизистую, способны даже внедряться внутрь других клеток. После закрепления на местности, начинается размножение и образование целой клеточной колонии.
Кроме переноса метастатических клеток по крови и лимфе, распространение идёт и внутри полости живота — трансцеломически. Не совсем ясно почему злокачественные клетки задерживаются в брюшине, предполагается благотворное действие микроклимата. Большинство метастазов находят в местах с более спокойной обстановкой и слабой перистальтикой органов, или там, где активно всасывается внутрибрюшная жидкость.
Часто клетки «разбрасываются» во время операции и при лапароскопическом вмешательстве вероятность обсеменения вдвое ниже, чем при классической хирургии. Во время операции обязательно проводится профилактика раковой диссеминации путём неоднократной обработки специальными растворами, но самый эффективный способ очищения от диссеминатов — внутриполостная химиотерапия на фоне гипертермии (HIPEC).
При каких заболеваниях развивается
Перитонеальный канцероматоз диагностируют у каждого третьего пациента с новообразованием желудочно-кишечного тракта. Метастазы по брюшине характерны для карцином желудка и поджелудочной железы — поражается до 40% пациентов. При раке кишечника канцероматоз обнаруживают только у десятой части больных. Максимально высокий процент обусловлен злокачественными процессами яичников — на момент выявления болезни две из трёх пациенток уже имеют опухолевые узлы на брюшине.
Вероятность канцероматоза зависит от степени агрессивности раковых клеток и величины первичной опухоли, так при тотальном инфильтративном раке желудка его выявляют чаще, чем при локальном процессе, не разрушившем наружную серозную оболочку органа.
Тем не менее, ни при одном из злокачественных процессов любой локализации, будь то рак молочной железы или простаты, лёгкого или носоглотки, не исключается внутрибрюшинное метастазирование. Посмертно канцероматозные изменения выявляют у каждого третьего, погибшего от прогрессирования заболевания.
Для сарком такая локализация метастазов нетипична, саркоматоз брюшины констатируется едва ли у трёх из сотни больных. В редчайших случаях совершенно доброкачественные по гистологии муцинозные аденома аппендикса и цистаденома яичников тоже способны привести к обсеменению брюшины с выработкой гелеобразного секрета.
У одного из миллиона, и много чаще это будет женщина, выявляют муцинозную аденому аппендикса или муцинозную цистаденому яичников, в последующем часто приводящие к обсеменению брюшины. Распространение аденомуцинозных клеток в полости живота с выработкой гелеобразного секрета именуют уже «псевдомиксома», зачастую при в этой стадии заболевания не удаётся определить первоисточник опухоли.
Диагностика канцероматоза брюшины
Не представляет трудности выявление опухолевого поражения брюшины при асците, в отсутствии выработки патологического секрета диагностика опирается на визуализацию — УЗИ и КТ с контрастированием.
При УЗИ на внутреннем листке, прилежащем к мышцам брюшной стенки, в норме очень тонком и незаметном, можно увидеть напластования толщиной в несколько сантиметров, практически не прослеживаются только мелкие узелки.
КТ с контрастным усилением много информативнее УЗИ, способно выявить сантиметровые образования. Наиболее точный диагностический метод — лапароскопия. Это обследование обязательно при карциноме желудка, при раке яичников предпочтительна операция — диагностика и лечение одновременно.
При лапароскопии или пункции получают асцитическую жидкость для исследования и определения первоисточника злокачественного процесса. Из экссудата выделяют осадок, который изучают под микроскопом и проводят специфические реакции — ПЦР и ИГХ.
ПЭТ на этапе первичной диагностики не всегда информативна, поскольку далеко не все злокачественные клетки легкого, печени, почек способны накапливать изотопы.
Вне всяких сомнений, самый оптимальный метод диагностики — получение кусочка опухолевой ткани для исследования. Биопсия не целесообразна при известном источнике метастазов и после недавнего лечения первичного рака.
Стадии канцероматоза брюшной полости
Стадирование перитонеального канцероматоза нельзя назвать точным, все классификации приблизительны в определении объёма повреждений и не уточняют локализацию узлов. Зачастую, стадирование даёт общее представление о прогнозе эффективности лечебных мероприятий, нежели информирует о настоящем состоянии внутри полости живота.
Разработанная японскими специалистами градация опухолевого распространения по трём степеням, учитывает общий объём поражения, без числа и размеров очагов:
- P1 — ограниченное;
- P2 — разделённые нормальной тканью очаги;
- P3 — множество узлов.
Во время операции хирурги определяют индекс перитонеального канцероматоза (РСI), измеряя узелки в 13 регионах полости, общая сумма баллов влияет на тактику лечения, в первую очередь, на возможность удаления брюшины — перитонэктомию и целесообразность внутриполостной химиотерапии. При некоторых злокачественных процессах прибегают к сложным формулам расчёта РСI.
Наибольшее представление о размерах ракового повреждения даёт стадирование по степеням:
- 0 — в полости чисто,
- I — в одной анатомической зоне узелки до 5 мм,
- II — множественные узелки до 5 мм,
- III — локальное поражение 0.5–2 см,
- IV — 2-х сантиметровые узелки.
Течение канцероматоза определяется не столько размером метастатического узла, сколь клеточной потенцией к прогрессии и выработке асцитической жидкости, общей площадью опухолевой трансформации и клиническими проявлениями.
Симптомы канцероматоза брюшной полости
Перитонеальный канцероматоз небольшой протяжённости может не проявлять себя симптомами, особенно в отсутствии выработки асцитической жидкости. С другой стороны, жидкость может продуцироваться и при отсутствии видимых метастазов. Как правило, симптоматика неспецифична, и в разном наборе могут отмечаться:
- меняющие локализацию болезненные ощущения, а чаще — непонятный дискомфорт в полости живота;
- нарастающая слабость до утраты работоспособности;
- потеря веса при стабильном диетическом режиме;
- прогрессирующее снижение аппетита;
- функциональные нарушения со стороны органов ЖКТ.
Дальнейшее нарастание раковых повреждений сопровождается опухолевой интоксикацией, сдавление желудка опухолевыми узлами осложняется тошнотой и рвотой, кишечника — запорами и поносами с усугублением частичной непроходимости. Распад крупных узлов может вызывать боли и повышение температуры.
Асцит нарушает процесс дыхания и вызывает сердечную недостаточность с постоянными отёками, а частая эвакуация патологической жидкости приводит к белковой недостаточности.
Как лечат канцероматоз брюшины
Ни один из современных методов лечения канцероматоза не гарантирует радикального удаления опухоли, не способен излечить, но может улучшить состояние и существенно продлить жизнь.
Хирургическое лечение канцероматоза технически сложное для оперирующей бригады и трудно переносимое пациентом, поскольку предполагает удаление первичного рака, увеличенных лимфатических узлов, сальниковых сумок и всех видимых опухолевых образований вместе с брюшиной.
Перитонэктомия — многоэтапное вмешательство, включающее удаление нескольких органов и отделов брюшной полости. В результате операции пациент может остаться без селезёнки, желчного пузыря, части кишечника, матки с придатками.
Стандарт терапии канцероматоза — химиотерапия системная и локальная — внутрибрюшинная после удаления асцита или через лапаропорт, установленный во время операции.
Эффективность лекарственной терапии невысокая, за исключением случаев первичного рака яичников. Таргетные и иммуно-онкологические препараты только изучаются в клинических испытаниях.
Какие методики терапии дают лучший результат
Наиболее высокий эффект демонстрирует комбинация трёх методов лечения рака:
- Операция с максимально возможным удалением злокачественных новообразований — циторедукция.
- Локальная внутрибрюшинная гипертермия.
- Внутриполостное введение химиопрепаратов.
Использование во время хирургического вмешательства интраперитонеальной гипертермической химиотерапии (ИГХТ или HIPEC) позволяет максимально долго поддерживать очень высокую концентрацию цитостатика непосредственно в зоне поражения и усилить лекарственное воздействие нагреванием тканей. При весьма скромных исторических результатах хирургического вмешательства устойчивой к цитостатикам псевдомиксомы только HIPEC открывает пациентам перспективу на долгую жизнь.
Технология ИГХТ такова: в течение полутора часов внутрь брюшной полости под давлением подаётся нагретый химиопрепарат в дозе, существенно превышающей максимально разрешённую для внутривенного введения. За счёт локального использования изменяется спектр токсических реакций, исключается опасное для жизни повреждение кроветворения, но возможна боль в животе и временное нарушение функционирования органов ЖКТ.
Интраоперационная фотодинамическая терапия (ФДТ), когда на выявленные с помощью фотосенсибилизатора очаги опухоли воздействуют лазером, уступает HIPEC по результативности, поскольку лазером невозможно проникнуть во все «закоулки» брюшной полости. Тем не менее, целесообразно использование фотодинамической терапии при крупных и немногочисленных раковых узлах.
Прогноз при канцероматозном поражении
На течение процесса влияет объём поражения на момент начала терапии, степень злокачественности опухоли, в свою очередь определяющая чувствительность к химиотерапии. Основополагающее влияние оказывает талант и опыт хирурга, и несомненно, правильность выбора лечебной тактики.
Однозначно революционные результаты в клинических испытаниях показала только HIPEC. После интраоперационной гипертермической ХТ пятилетняя выживаемость при канцероматозе рака желудка выросла максимально до 20%, все прочие методы исключали столь долгое дожитие. При раке толстой кишки с метастазами по брюшине каждый третий пациент прожил более 5 лет, при карциноме слепой кишки и аппендикса — шестеро из десяти вступили во вторую пятилетку жизни.
Список литературы
- Давыдов М.И., Тер-Ованесов М.Д., Буйденок Ю.В. с соавторами/ Гипертермическая интраоперационная интраперитонеальная химиотерапия при раке желудка: существует ли реальная возможность изменить прогноз? // Вестник РОНЦ им. Н. Н. Блохина РАМН; 2010 Т. 21; № 1
- Степанов И.В., Падеров Ю.М., Афанасьев С.Г./ Перитонеальный канцероматоз// Сибирский онкологический журнал; 2014; № 5
- Akiyama H., Yamaoka H., Tanaka K., et al./ Continuous hyperthermic peritoneal perfusion for peritoneal dissemination of gastric cancer // Hepatogastroenterology; 1998.
- Bozzetti F., Bonfanti G., Morabito A., et al/ A multifactorial approach for the prognosis of patients with carcinoma of the stomach after curative resection // Surg. Gynecol. Obstet.; 1986.
- Cotte E., Passot G., Gilly F.N., Glehen O. /Selection of patients and staging of peritoneal surface malignancies // World J. Gastrointest. Oncol.; 2010; Vol. 2.
- Chua T.C., Moran B.J., Sugarbaker P.H., et al. /Early- and longterm outcome data of patients with pseudomyxoma peritonei from appendiceal origin treated by a strategy of cytoreductive surgery and hyperthermic intraperitoneal chemotherapy// J. Clin Oncol 2012.
- Deraco M., Santoro N., Carraro O., Inglese M.G., et al./ Peritoneal carcinomatosis: feature of dissemination. A review // Tumori; 1999.
- Lansom J., Alzahrani N., Liauw W., Morris D.L. /Cytoreductive Surgery and Hyperthermic Intraperitoneal Chemotherapy for Pseudomyxoma Peritonei and Appendix Tumours // Indian J Surg Oncol. 2016 Jun.
- Sugarbaker P.H./ Overview of peritoneal carcinomatosis // Cancerologia; 2008.
Источник