Кишечная непроходимость с асцитом
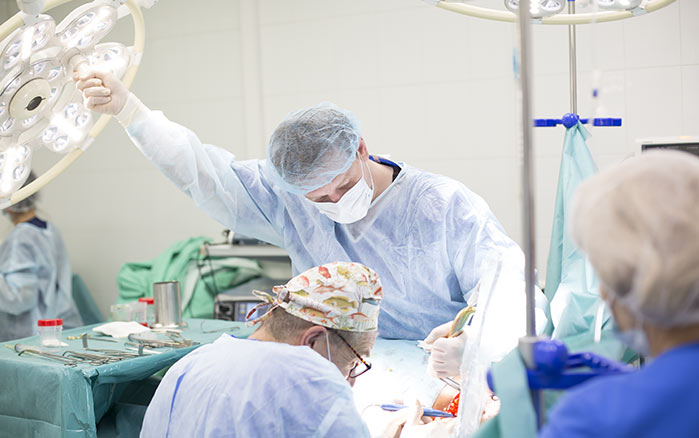
Своевременная диагностика и лечение острой кишечной непроходимости, в том числе профилактика непроходимости путем эндоскопической установки стентов, позволяет сохранить высокое качество жизни у пациентов с онкологическими заболеваниями органов брюшной полости, а в ряде случаев и спасти жизнь.
Что такое острая кишечная непроходимость?
Острая кишечная непроходимость – грозное, опасное для жизни осложнение многих заболеваний желудочно-кишечного тракта, в том числе опухолей собственно кишечника, а также опухолей других органов брюшной полости и забрюшинного пространства.
Несмотря на успехи медицины, при неоказании своевременной медицинской помощи в первые 4-6 часов развития от острой кишечной непроходимости гибнет до 90% больных.
Пациентам с раком толстой и тонкой кишки, особенно на поздних стадиях заболевания, при наличии массивных метастазов в области ворот печени, важно знать первые признаки развития острой кишечной непроходимости, чтобы своевременно обратиться за медицинской помощью в лечебное учреждение.
Суть острой кишечной непроходимости состоит в быстром прекращении нормального физиологического прохождения (пассажа) пищи по пищеварительному тракту.
Кишечная непроходимость бывает полной или частичной. При частичной непроходимости пассаж пищи резко ограничен. Так, например, при стенозе (сдавлении) опухолевым конгломератом толстой кишки ее диаметр может уменьшиться до 1-3 мм. В результате через такое отверстие может проходить только небольшое количество пищи. Диагностируется такое поражение при проведении гастроскопии или колоноскопии, в зависимости от места развития сужения кишки.
Для прогноза лечения и исхода этого острого осложнения онкологического заболевания крайне важно знать, произошло ли нарушение пассажа пищи до или после связки Трейца, образованной складкой брюшины, подвешивающей двенадцатиперстную кишку. Соответственно поэтому выделяют высокую (тонкокишечную) и низкую (толстокишечную) непроходимость.

Также прогноз лечения острой кишечной непроходимости определяется наличием или отсутствием механического препятствия. Если нет препятствия пассажу пищи в виде полного сдавления кишечной трубки, кишечная непроходимость называется динамической, которая в свою очередь бывает паралитической или спастической.
При наличии механического препятствия на пути пищи (чаще опухоли, отека прилежащих тканей, обусловленных опухолью, или спайки, в том числе возникшей вследствие ранее проведенных операций хирургического лечения рака), такая кишечная непроходимость называется механической (синоним — обтурационной).
При сдавлении брыжейки (складки брюшины, поддерживающей кишку, в которой проходят сосуды и нервы) кишечная непроходимость называется странгуляционной.
При динамической кишечной непроходимости назначают консервативное лечение в условиях хирургического стационара. При механической и странгуляционной кишечной непроходимости лечение только хирургическое.
Почему развивается острая кишечная непроходимость?
Среди факторов, предрасполагающих к механической кишечной непроходимости, наиболее часто встречаются:
- Спаечный процесс в брюшной полости (как следствие взаимодействия между опухолью и окружающими тканями, и как осложнение после операций по удалению первичного очага опухоли).
- Индивидуальные особенности строения кишечника (долихосигма, подвижная слепая кишка, дополнительные карманы и складки брюшины),
- Грыжи передней брюшной стенки и внутренние грыжи.
Механическая (обтурационная) кишечная непроходимость может возникнуть также вследствие сдавления кишечника опухолью извне или сужения просвета кишечника в результате воспаления. Важно знать, что механическая кишечная непродоходимость может развиться не только при опухолях кишечника, но и при раках других локализаций, например, раке почки, раке печени, раке мочевого пузыря, раке матки.
Паралитическая непроходимость может быть результатом травмы, перитонита, существенных нарушений обмена веществ, например, при низком уровне калия в крови. У онкологических больных паралитическая кишечная непроходимость может быть обусловлена декомпенсацией функции печени и почек, нарушением углеводного обмена при наличии таких сопутствующих заболеваний, как сахарный диабет и ряде других состояний.
Спастическая кишечная непроходимость развивается при поражениях головного или спинного мозга, отравления солями тяжёлых металлов (например, свинцом) и некоторых других состояниях.
Признаки кишечной непроходимости
Ранний и обязательный симптом острой кишечной непроходимости — боль в животе. Боль может возникнуть внезапно без каких-либо предвестников, быть «схваткообразной», обычно она не зависит от приёма пищи. Приступы боли при острой кишечной непроходимости первое время повторяются примерно через равные промежутки времени и связаны с физиологическим волнообразным движением кишечника — перистальтикой. Спустя некоторое время боль в животе может стать постоянной.
При странгуляционной непроходимости боль сразу постоянная, с периодами усиления во время волны перистальтики. При этом стихание болей нужно расценивать как сигнал тревоги, поскольку говорит о прекращении перистальтической деятельности кишечника и возникновении пареза (паралича) кишечника.
При паралитической кишечной непроходимости боли в животе чаще тупые распирающие.
Симптомы разнятся в зависимости от высоты нарушения проходимости пищи – в области пищевода, желудка, двенадцатиперстной кишки или толстого кишечника. Задержка стула, включая его отсутствие с течение нескольких часов, отсутствие отхождения газов — это ранние симптомы низкой кишечной непроходимости.
При расположении механического сдавления, пареза или сужения в области верхних отделов кишечника, преимущественно в начале заболевания, при частичной проходимости кишечной трубки, под влиянием лечебных мероприятий, у пациента может быть стул за счёт опорожнения кишечника, расположенного ниже препятствия. Часто наблюдается тошнота и рвота, иногда многократная, неукротимая, усиливающаяся с нарастанием интоксикации.
Иногда отмечаются кровянистые выделения из заднего прохода.
При внимательном осмотре можно заметить существенное вздутие и выраженную асимметрию живота, видимую на глаз перистальтику кишок, которая затем постепенно угасает – «шум вначале, тишина в конце».
Общая интоксикация, слабость, снижение аппетита, апатия — эти симптомы наблюдаются у большинства больных с постепенным прогрессированием кишечной непроходимости от частичной до полной.
Чем опасна кишечная непроходимость?
Кишечная непроходимость приводит к обезвоживанию организма, выраженным сдвигам водно-электролитного и кислотно-щелочного баланса организма. В основе лежит нарушение поступления пищи, ее переваривания и всасывания, а также прекращения секреции желудочного и кишечного соков в просвет желудочно-кишечного тракта.
Поскольку ткани и клетки организма чувствительны к малейшим изменениям в химическом постоянстве внутренней среды, то такие сдвиги вызывают дисфункцию практически всех органов и систем. Наряду с жидкостью и электролитами при кишечной недостаточности за счёт голодания, рвоты, образования воспалительного экссудата теряется значительное количество белков (до 300 г/сут), особенно альбумина, играющего важную роль в гомеостазе. Наличие метастазов в области печени, которые угнетают белково-синтетическую функцию печени, дополнительно уменьшает уровень белка в крови, снижает онкотическое давление плазмы крови, что вызывает развитие стойких отеков.
Общая интоксикация организма при постепенном развитии кишечной непроходимости дополнительно ухудшается тем фактом, что в содержимом приводящего отдела кишечника начинаются процессы разложения и гниения, в содержимом просвета кишечника начинает размножаться патогенная микрофлора, накапливаются токсические продукты. При этом физиологические барьеры, в норме препятствующие всасыванию токсинов из кишечника, не работают и значительная часть токсических продуктов поступает в кровоток, усугубляя общую интоксикацию организма. В стенке кишки начинает развивается омертвение (некроз), итогом которого является гнойный перитонит из-за излития кишечного содержимого в брюшинную полость. При этом токсичные продукты распада тканей, микробные токсины, тяжелые метаболические сдвиги могут привести к сепсису и полиорганной недостаточности и гибели пациента.

Что необходимо предпринять, чтобы спасти человека при кишечной непроходимости?
Развитие кишечной непроходимости – показание к срочной госпитализации в хирургический стационар, где безотлагательно производится:
- рентгенография брюшной полости,
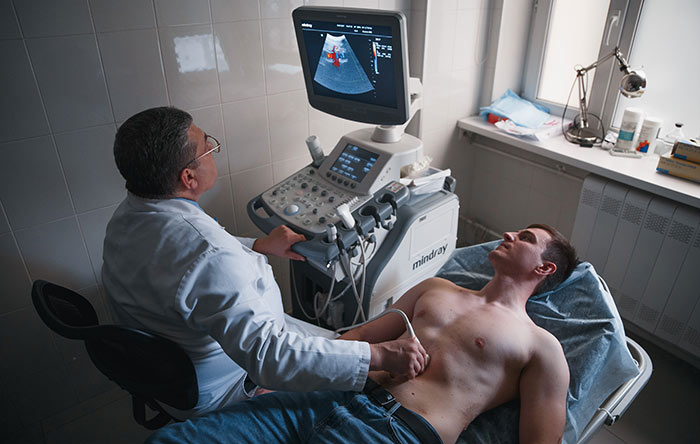
- ультразвуковое исследование органов брюшной полости
- ирригография — рентгенологическое исследование с контрастной бариевой взвесью, вводимой в кишечник с помощью клизмы.
В нашей клинике мы часто используем жидкий контраст для лучшего контурирования кишечника и во избежание попадания бария в брюшинную полость во время последующей операции. При подтверждении диагноза и/или наличии выраженных клинических симптомов перитонита после очень короткой предоперационной подготовки проводится экстренное хирургическое вмешательство.
В отсутствие симптомов раздражения брюшины (перитонита) некоторое время (до суток) под наблюдением хирурга проводится консервативная терапия:
- регидратация,
- введение белковых растворов, электролитов,
- введение антибиотиков,
- освобождение верхних отделов пищеварительного тракта путем зондового промывания желудка,
- промывание кишечника,
- обезболивание и пр.
При отсутствии эффекта от консервативного лечения требуется выполнить операцию в плановом порядке. При возможности удалить причину непроходимости проводится диагностическая лапаротомия с резекцией кишечника. Во время операции обязательно проводится ревизия брюшной полости для уточнения причины развития острой кишечной непроходимости и определения общего объема операции.

При обнаружении во время ревизии органов брюшной полости спаек, заворота, узлов петель, инвагинаций, производится их устранение. По возможности выполняется циторедуктивная операция по удалению первичного опухолевого очага, вызвавшего развитие острой кишечной непроходимости.
По существующим правилам удаление кишки при непроходимости должно проводиться на определенном расстоянии выше и ниже места непроходимости (обтурации). Если диаметр соединяемых отрезков ненамного отличается, выполняют анастомоз «конец в конец», при значительном различии диаметров приводящего и отводящего участков анастомоза – «бок в бок». В нашей клинике мы используем как классические методики ручного шва для формирования аностозов, так и современные сшивающие аппараты типа степлеров.
При тяжелом общем состоянии больного или невозможности формирования первичного анастомоза по другим причинам, например, из-за далеко зашедшего опухолевого процесса, формирования «опухолевого панциря», большой протяженности участка резецируемого кишечника, скопления большого объема жидкости в брюшной полости (асцита), на передней брюшной стенке формируется отверстие – колостома, в которую выводятся приводящий и отводящий отрезки кишки – «двухствольная стома».
В зависимости от участка кишки, из которого производится формирование колостомы данное оперативное вмешательство имеет различное наименование:
- наложение илеостомы – при выведении тонкой кишки,
- цекостома – слепой,
- асцендо-, десцендо- и трансверзостомы – соответственно восходящей, поперечный и нисходящий участки поперечноободочной кишки,
- при сигмостомии – из сигмовидной кишки.
При операции на сигмовидной кишке, называемой «операцией Гартмана» отводящий отрезок толстой кишки всегда ушивается наглухо и погружается в брюшную полость.
Всегда ли необходимо выведение стомы во время операции по поводу кишечной непроходимости?
Помимо наложения стомы, альтернативным способом восстановления прохождения пищи по кишечнику является создание обходного межкишечного анастомоза. Операции называются по названию соединяемых отделов кишечника, например:
- Операция на правых отделах толстого кишечника называется наложением обходного илеотрансверзоанастомоза.
- Наложение анастомоза между начальным отделом тонкой и конечным отделом тощей кишок называется наложением обходного илеоеюноанастоза.
Каждое из этих вмешательств может быть временным, производимым для подготовки больного к последующим этапам или окончательным при невозможности проведения радикальной операции.
Основной задачей, решаемой во время хирургического лечения острой кишечной непроходимости, является спасение жизни пациента от угрозы прорыва кишечного содержимого в брюшинную полость с развитием острого перитонита и смертью пациента.
Что происходит с выведенной стомой?
В течение 2-3-х недель после выполненной операции по поводу острой кишечной непроходимости при условии улучшении общего состояния, ликвидации последствий интоксикации организма может быть выполнена повторная операция по восстановлению естественного пассажа пищи. В таких случаях выполняется наложение кишечного анастомоза, который погружается внутрь брюшной полости.
В остальных случаях к колостоме присоединяется калоприемник для сбора кишечного содержимого. Современные разновидности калоприемников позволяют поддерживать приемлемое качество жизни даже при их использовании в течение нескольких месяцев.
Возможно ли помочь больному без операции?
Часто в тяжелых случаях и при неоперабельных опухолях у больных в тяжелом состоянии с частичной кишечной непроходимостью декомпрессия желудочно-кишечного тракта достигается путем эндоскопической установкой стента в толстую кишку. В этом случае хирургическая операция выполняется через естественный просвет кишечника – под контролем колоноскопа в просвет толстой кишки per rectum вводится первоначально баллон, расширяющий суженный (стенозированный) участок, а затем устанавливается стент.
Своевременная профилактическая установка стента в просвет кишечника позволяет продлить жизнь и существенно повысить ее качество за счет уменьшения интоксикации, а также избежать вероятного оперативного вмешательства у больных при 4 стадии ракового процесса. Аналогичным образом может выполняться стентирование участков двенадцатиперстной кишки.
Мы устанавливаем стенты в толстый кишечник у больных раковым поражением кишечника и с высоким классом анестезиологического риска из-за наличия сопутствующих заболеваний, в том числе ишемической болезни сердца, сахарного диабета и ряда других. Это позволит длительно поддерживать проходимость кишечника и избежать оперативного вмешательства.
Источник
Бактериальная асцитная жидкостная инфекция
Бактериальная асцитная жидкостная инфекция попадает в брюшную полость из просвета кишечника (путем транслокации из-за повышенной проницаемости стенок) при отсутствии первичных внутрибрюшных очагов инфекции (острый холецистит, аппендицит, перфорация кишечника и др.). Это состояние встречается исключительно у пациентов с циррозом печени. Большинство случаев вызывается аэробными G (-) палочками (Escherichia coli, Klebsiella pneumoniae) и G (+) бактериями (энтерококки, стрептококки).
Клинические проявления местных симптомов перитонита включают боль в животе (1/2 пациента), боль в животе при пальпации, рвоту, диарею, паралитическую непроходимость кишечника. Также присутствуют системные признаки воспаления: лихорадка (2/3 пациентов), гипотермия, озноб, тахикардия, тахипноэ, печеночная недостаточность, прогрессирующая печеночная энцефалопатия, артериальная гипотензия, почечная недостаточность, желудочно-кишечное кровотечение.
Боль в животе при пальпации
Диарея
У 7-30% пациентов нет клинических признаков. Цитология асцита показывает ≥500 лейк / л и ≥250 нейтро / мкл. Установлено, что рост асцитных бактерий в посевах составляет всего 40%, но отрицательный результат посева не исключает инфекцию.
Бактериальную асцитную жидкостную инфекцию следует отличать от вторичного бактериального перитонита (вследствие острого воспаления или перфорации органов брюшной полости). Для асцита характерны: локальная боль в животе, очень высокое количество нейтрофилов, высокое содержание белка (> 10 г / л), повышенный уровень глюкозы (> 2,8 ммоль / л) и уровни лактатдегидрогеназы. В асцитной жидкой культуре растет поливалентная инфекция. При подозрении на вторичный перитонит необходима компьютерная томография брюшной полости.
Патологию лечат внутривенными цефалоспоринами III поколения (цефотаксим, пиперациллин с тазобактамом) в течение 5-7 дней. Совместные инфузии 1–1,5 г/кг альбумина снижают частоту и смертность от гепаторенального синдрома. После первого случая выживаемость составляет 30-50% в первый год, 25-30%. – на второй год. Основные меры профилактики представлены в таблице 5.
Таблица 5. Первичная и вторичная профилактика бактериальной асцитной жидкостной инфекции в соответствии с рекомендациями EASL
| Острое желудочно-кишечное кровотечение | 400 мг норфлоксацина 2 р./день. 7 дн. перорально; 1 г/сут. цефтриаксон внутривенно 7 дней. |
Первичная профилактика:
| 400 мг/сут. норфлоксацин перорально. |
| Вторичная профилактика | 400 мг / сут. норфлоксацин; 750 мг еженедельно, ципрофлоксацин; 480-960 мг бисептола 5 дней в неделю. |
Злокачественный (карциноматозный) асцит
Более длительная выживаемость у женщин с репродуктивными опухолями.
Основные методы лечения злокачественного асцита — ограничение натрия, диуретики, парацентез большого объема, формирование перитовенического шунта (Денверский шунт), из которых парацентез является наиболее часто используемым и эффективным.
Асцит нефрогенного происхождения
У пациентов, находящихся на длительном гемодиализе, жидкость может начать накапливаться в брюшной полости без какой-либо другой причины. Частота асцита, связанного с гемодиализом, неизвестна, но это относительно редкое состояние.
Патогенез асцита нефрогенного происхождения до конца не выяснен. Предполагается, что возможными механизмами являются хроническая перегрузка объемом в сочетании с застоем в печени и повышенным гидростатическим давлением в венах печени, изменения проницаемости перитонеальной мембраны у пациентов, ранее проходивших перитонеальный диализ, и нарушение лимфатической перитонеальной резорбции. Другие способствующие факторы включают гипоальбуминемию, застойную сердечную недостаточность и гиперпаратиреоз.
Хилиотический асцит
Хилиотический асцит — это жидкость молочной консистенции, которая накапливается в брюшине и развивается из-за лимфатического дренажа при кишечном расстройстве, вызванном травматическим повреждением или непроходимостью (доброкачественной или злокачественной). Это довольно редкое заболевание, которое встречается примерно у 1 из 20000 пролеченных пациентов с диагнозом асцит.
Хотя новых эпидемиологических исследований не проводилось, наблюдается рост числа случаев хилиотического асцита. Это было связано с увеличением продолжительности жизни при раке, с увеличением числа более сложных операций и процедур на брюшной полости, сердце и грудной клетке.
Две трети всех случаев составляют онкологические заболевания (лимфома, лимфангиоматоз, карциноиды, саркома Капоши, опухоли груди и яичников, опухоли поджелудочной железы) и цирроз печени.
Другие возможные причины включают:
- повреждение лимфатической системы после операции (аневризмы брюшной полости, удаление забрюшинных лимфатических узлов, фундопликация Ниссена, панкреатодуоденэктомия, использование перитонеального диализного катетера);
- тупая травма живота;
- инфекции (туберкулез);
- воспалительные заболевания;
- панкреатит и другие.
Туберкулез
Хилиотический асцит выявляется примерно в 0,5–1% случаев у пациентов с циррозом печени без онкологического заболевания.
Диагностика асцита выявляет повышенное количество лимфоцитов, уровни триглицеридов >2,26 ммоль/л, SAAG s >11 г/л, атипичные клетки, уровень α-амилазы> 40 Ед/л (при остром панкреатите). При обнаружении хилиотического асцита пациенту также следует пройти обследование на туберкулез. Лабораторные анализы крови проводятся для выяснения причины асцита.
Компьютерная томография брюшной полости полезна при выявлении патологических внутрибрюшных лимфатических узлов и их производных, поражения грудного протока. Магнитно-резонансная лимфография, лимфангиография и лимфосцинтиграфия могут быть выполнены для обнаружения измененных, поврежденных забрюшинных лимфатических узлов, свищей и других поражений лимфатического дренажа.
Лечение асцита при хилиозе зависит от причины. При отсутствии ответа на лечение основного заболевания рекомендуется диета с высоким содержанием белка и низким содержанием жира с триглицеридами со средней длиной цепи, чтобы избежать длинноцепочечных триглицеридов и свободных жирных кислот. Однако этот метод не подходит для пациентов с запущенным циррозом печени. При запущенном циррозе печени применяется стандартное лечение асцита, выполняется парацентез и принимается решение TIPS.
Несколько небольших исследований описали преимущества орлистата, соматостатина и октреотида в борьбе с накоплением хилозирующего асцита.
Хирургическое лечение может помочь пациентам, у которых асцит развивается из-за послеоперационных осложнений, онкологического заболевания или врожденных состояний.
Геморрагический асцит
Это скопление кровянистой жидкости в брюшной полости, когда количество эритроцитов превышает 50000/мкл. Количество эритроцитов менее 1000/мкл. Асцит приобретает розовый цвет в присутствии эритроцитов в концентрации около 10000/мкл.
Основные причины геморрагического асцита:
- цирроз печени – 19%;
- онкологические заболевания – 20%, из них около 50% – гепатоцеллюлярная карцинома;
- системных заболеваний (саркоидоз, васкулит);
- сердечной недостаточности;
- травм у пациентов с циррозом — разрыв селезенки, биопсия печени, формирование TIPS;
- лапароскопия;
- травматическое повреждение сосудов во время парацентеза.
Цирроз печени
Для уточнения диагноза проводится УЗИ брюшной полости или компьютерная томография. Пациенты, у которых после парацентеза развивается геморрагический асцит, должны находиться под тщательным наблюдением путем повторных лабораторных тестов. Не требуется специального лечения для пациентов с циррозом печени, у которых диагностирован спонтанный геморрагический асцит при отсутствии гепатоцеллюлярной карциномы. При гепатоцеллюлярной карциноме может быть выполнена эмболизация поврежденного сосуда.
Асцит поджелудочной железы
Асцит поджелудочной железы — это скопление большого количества жидкости поджелудочной железы в брюшной полости, обычно из-за повреждения протока поджелудочной железы у пациентов с хроническим алкогольным панкреатитом.
Это асцит непортового происхождения (SAAG> 11 г / л), в основном серогеморрагический, с выраженным повышением α-амилазы (> 1000 Ед / л), сывороточного и асцитного жидкостного индекса амилазы, равного 6.
Для правильного диагноза требуется компьютерная томография брюшной полости и таза, эндоскопическая ретроградная панкреатография (ЭРХПГ) или магнитно-резонансная панкреатография.
Около трети пациентов подходит эффективное стандартное консервативное лечение панкреатита — голодная диета, инфузионная терапия, анальгетики. При отсутствии ответа некоторым пациентам рекомендуется введение октреотида 50 мг/день подкожно 2 недели в сочетании с диуретиками.
В случае стойкого асцита и повреждения протока поджелудочной железы рассматривается возможность применения ЭРХПГ и стентирования протока поджелудочной железы.
Вывод
Асцит может быть следствием многих заболеваний. Важно определить первопричину накопления асцита, вылечить основное заболевание и назначить симптоматическое лечение асцита в зависимости от его степени.
Продолжение статьи
- Асцит: первопричины, классификация — часть 1.
- Асцит: лечение асцита от легкой, умеренной (I-II) степени. Лечение асцита высокой степени (III) – часть 2.
- Асцит: бактериальная асцитная жидкостная инфекция, злокачественный, хилиотический, нефрогенный, геморрагический, поджелудочный — часть 3.
Вывод
Асцит может быть следствием многих заболеваний. Важно определить первопричину накопления асцита, вылечить основное заболевание и назначить симптоматическое лечение асцита в зависимости от его степени.
Источники: Руньон Б.А. Обследование взрослых с асцитом. В: Линдор К.Д., 2020. Анджели П., Бернарди М., Вильянуэва С. и др. Руководство EASL по клинической практике для ведения пациентов с декомпенсированным циррозом печени. 2018. Тандон П., Гарсия-Цао Г. Бактериальные инфекции, сепсис и полиорганная недостаточность при циррозе печени. Semin Liver Dis. 2008; Сангисетти С.Л. Злокачественный асцит: обзор факторов прогноза, патофизиологии и терапевтических мер. World J Gastrointest Surg. 2012; Ginès P, Angeli P, Lenz K, Al E. Клинические практические рекомендации EASL по ведению асцита, спонтанного бактериального перитонита и гепаторенального синдрома при циррозе; 2010. Арройо В., Жинес П., Гербес А.Л. и др. Определение и диагностические критерии рефрактерного асцита и гепаторенального синдрома при циррозе печени. Гепатология. 1996; Мур К.П., Айтал Г.П. Рекомендации по ведению асцита при циррозе печени. Кишечник. 2006; Бенмассауд А., Фриман С.К., Роккарина Д. и др. Лечение асцита у взрослых с декомпенсированным циррозом печени: сетевой метаанализ. Кокрановская база данных Syst Rev. 2020; Цочацис Э.А., Гербес АЛ. Диагностика и лечение асцита. J Hepatol. 2017; Эльферт А.А., Або Али Л., Солиман С. и др. Рандомизированное плацебо-контролируемое исследование баклофена при лечении мышечных спазмов у пациентов с циррозом печени. Eur J Gastroenterol Hepatol. 2016; Паш И., Билодо М. Тяжелое кровотечение после абдоминального парацентеза по поводу асцита у пациентов с заболеванием печени. Алимент Pharmacol Ther. 2005; Лин Ч., Ши Ф.Й., Ма МХМ, Чанг В.С., Ян Ч.В., Ко PCI. Должна ли склонность к кровотечению сдерживать абдоминальный парацентез? Dig Liver Dis. 2005; Бернарди М., Карачени П., Навицкис Р.Дж., Уилкс М.М. Инфузия альбумина пациентам, перенесшим парацентез большого объема: метаанализ рандомизированных исследований. Гепатология. Асцит — поддержка рака Macmillan. 2020 г. Элиа С., Граупера И., Баррето Р. и др. Тяжелое острое повреждение почек, связанное с нестероидными противовоспалительными препаратами при циррозе: исследование случай-контроль. J Hepatol. 2015; Гевара М., Фернандес-Эспаррах Г., Алессандрия С. и др. Влияние контрастных веществ на функцию почек у пациентов с циррозом печени: проспективное исследование. Гепатология. 2004; Нарахара Ю., Канадзава Х., Фукуда Т. и др. Трансъюгулярный внутрипеченочный портосистемный шунт в сравнении с парацентезом плюс альбумин у пациентов с рефрактерным асцитом с хорошей функцией печени и почек: проспективное рандомизированное исследование. J Gastroenterol. 2011.
Поделиться ссылкой:
Источник