Кишечные заболевания у недоношенных детей
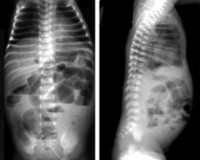
Заболевание вызывается, сальмонеллами, стафилококками, энтеровирусами, ассоциацией вирусов и бактерий и другими микробами. Заболевают чаще недоношенные и ослабленные дети, в особенности при нарушениях санитарно-гигиенического режима.
Клиническая картина. Кишечные инфекции могут протекать в форме гастрита, гастроэнтерита, энтероколита и колита.
Инкубационный период длится от некоторого количества часов до 5-8 суток. По тяжести течения различают 3 формы заболевания: легкую (стертая форма), характеризующуюся плоской кривой веса на протяжении 1-3 суток и кратковременным жидким стулом (до 5-7 раз в сутки); среднетяжелую и тяжелую формы с острым началом, нарастанием явлений токсикоза и эксикоза и неуклонным понижением веса. Ребенок резко истощен, кожа и слизистые оболочки сухие, возникает землистый оттенок кожных покровов, черты лица заостряются, огромной родничок западает. Температурная реакция бывает нечасто. Живот вздут, учащаются срыгивания, возникает рвота, нередко с примесью желчи. Стул 12-15 раз в сутки, жидкий, жидкий,с гнилостным запахом, порой с примесью зелени или имеет оранжевую окраску. В моче единичные красные кровяные клетки и цилиндры. В крови лейкоцитоз, время от времени нейтрофилез со сдвигом лейкоцитарной формулы влево. Для тяжелой формы характерны более выраженные нарушения водно-солевого обмена с последующим расстройством гемодинамики, развитием гипоксии, ацидоза и нарушением всех видов внутриклеточных обменных процессов.
В последние несколько лет участились вспышки внутрибольничной клебсиеллезной инфекции у новорожденных. Особенностью клебсиеллезного энтероколита является холероподобное течение, быстрое развитие эксикоза.
Прогноз. Серьезный, однако при своевременном лечении благоприятный.
Лечение. На весь период назначают водную паузу на протяжении 12-18 часов. В этот же период проводят дезинтоксикационную и регидратационную терапию по возможности с учетом степени и вида обезвоживания (вододефицитное, соледефицитное, изотоническое); коррекцию нарушения КОС. Для пероральной регидратации вероятно применение регидрона, отваров трав (ромашка, зверобой). При тяжелых инфекциях с неукротимой рвотой на 1-2 сут вероятно проведение полного парентерального питания, после частичного парентерального.
Для инфузионной терапии применяют раствор Рингера, 5-10 % раствор глюкозы, плазму (сухую и нативную), кровозамещающие жидкости. Расчет жидкости проводят с учетом возраста и веса ребенка (см. Диспепсические расстройства у новорожденных). С целью дезинтоксикации, десенсибилизации и удержания жидкости в сосудистом русле назначают гидрокортизон в дозе 2-3 мг/кг в сутки (половину суточной дозы возможноввести внутривенно капельно). Последующее проведение гормональной терапии продолжают коротким курсом (5-7 суток) по убывающей схеме.
После водной диеты назначают сцеженное грудное молоко по 5-10 миллилитра 10 раз в сутки, каждый день увеличивая дозу (недостающее число молока дополняют жидкостью).
Антимикробные препараты назначают с учетом чувствительности выделенной флоры. До получения посева вероятно внутримышечное (в тяжелых ситуациях внутривенное) введение антибиотиков широкого спектра действия: цепоринов, аминогликозидов — в возрастных дозах. Меньше лучше применение ампициллина и ампиокса. При клебсиеллезной, синегной или протейнойной инфекции неплохие результаты дает сочетанное использование одного из указанных антибиотиков (парентерально) и полимиксина-М (перорально), и поли- или моновалентных фагов: антиклебсиеллезного, антипротейного, колипротейного и т. д. (перорально и в клизмах).
Тяжелые формы стафилококковых энтероколитов требуют комбинированного лечения антибиотиками направленного действия: полусинтетические пенициллины (оксациллин, метициллин) в возрастной дозе. При стафилококковой этиологии заболевания показаны противостафилококковая плазма и гамма-глобулин.
Требуется рекомендация бифидумбактерина по 5 доз 3 раза в сутки на протяжении целого времени лечения антибиотиками (время введения таких 2-х препаратов не должно совпадать). Назначают витаминотерапию. При потребности проводят тоже симптоматическую терапию (сердечные средства, ингаляции кислорода и пр.). Возможно применять обволакивающие и вяжущие средства типа «Смекта» (взвесь ракушечника), спазмолитики (но-шпа).
Предупреждение. Строжайшее соблюдение санитарно-гигиенического режима в отделениях для новорожденных. В случае возникновения у ребенка признаков кишечной инфекции необходима его изоляция и индивидуальное, асептическое обслуживание. При огромной вспышке эпидемического диареи нужно закрыть отделение и произвести тщательную его дезинфекцию.
Источник
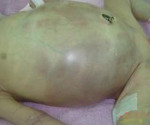
Некротический энтероколит новорожденных (НЭК) – это неспецифическое заболевание воспалительного характера, которое вызывается инфекционными агентами на фоне повреждения слизистой оболочки кишечника или ее функциональной незрелости. Симптомы включают соматические реакции и абдоминальные проявления. При длительном течении наблюдаются признаки перфорации кишечника и клиника перитонита. Диагностика НЭК сводится к физикальному обследованию, оценке симптомов по шкале Walsh и Kliegman и рентгенографии. Лечение зависит от стадии заболевания, может быть как консервативным, так и хирургическим.
Общие сведения
Некротический энтероколит новорожденных или «болезнь выживших недоношенных» – это гетерогенная патология, которая характеризуется развитием язв и некрозов стенки кишечника с дальнейшей перфорацией. Более 90% больных детей – недоношенные, с массой тела до 1500г. Общая заболеваемость составляет 0,5-3 на 1000 новорожденных. Прогноз, как правило, неясен, т. к. для НЭК характерно резкое ухудшение состояния на фоне мнимого благополучия. Часто требуется хирургическое вмешательство. Летальность в зависимости от формы колеблется от 25 до 55%. Даже после успешного проведения операции показатель смертности составляет свыше 60%. При условии выживания ребенка наблюдается тяжелый период реабилитации, остается высокий риск послеоперационных осложнений.

Некротический энтероколит новорожденных
Причины НЭК новорожденных
Некротический энтероколит новорожденных – полиэтиологическое заболевание. Основными патогенетическими факторами являются гипоксия и ишемия в перинатальном периоде, нерациональное питание новорожденного и заселение кишечника аномальными микроорганизмами. К способствующим факторам относятся преждевременные роды, эклампсия, травмы ЦНС при родах, иммунодефицитные состояния у ребенка, аномалии развития кишечника, отягощенный семейный анамнез.
Ишемия кишечника может быть обусловлена внутриутробной асфиксией плода, при которой наблюдается централизация кровообращения, постановкой катетера в пупочную артерию, влекущей за собой спазм артерий и их тромбоэмболию, явлением «сгущения крови» и артериальной гипотензией, при которых нарушается ток крови и поступление питательных веществ. К алиментарным причинам развития некротического энтероколита новорожденных относят питание ребенка искусственными смесями и их резкую смену, использование гипертонических растворов, повреждающих слизистую оболочку кишечника, врожденную непереносимость молока, непосредственную инвазию патогенных агентов через ЖКТ. Наиболее часто причиной НЭК становятся Kl. pneumonia, E. coli, клостридии, стафилококки, стрептококки и грибы рода Candida.
Классификация НЭК новорожденных
По скорости развития выделяют следующие формы некротического энтероколита новорожденных:
- Молниеносная. Перфорация стенки кишечника возникает на протяжении 36-48 часов после проявления первых симптомов – незначительного нарушения общего состояния ребенка. Характерна для доношенных детей с аномалиями развития ЖКТ (гастрошизис), гемолитической анемией, травмами ЦНС.
- Острая. Дебют характеризуется абдоминальными симптомами. Как правило, спустя 8-16 часов присоединяются соматические проявления, резко ухудшается общее состояние ребенка. Без соответствующего лечения НЭК быстро переходит в 3 стадию. Наблюдается у детей с массой тела при рождении свыше 1500 г.
- Подострая. Первичные абдоминальные проявления имеют перемежающийся характер, возникают поэтапно. Соматические расстройства развиваются медленно. Для этой формы характерно рецидивирующее течение. Обычно возникает у глубоко недоношенных детей с массой тела менее 1500 г.
В зависимости от массивности поражения различают следующие варианты НЭК:
- Локальный. Патологические изменения наблюдаются на ограниченном отрезке кишечника.
- Полисегментарный. Характерно поражение сразу нескольких участков.
- Паннекроз или тотальный. В патологический процесс втягивается весь кишечник.
Симптомы и осложнения НЭК новорожденных
Некротический энтероколит новорожденных может возникать в первые 24 часа после родов (ранняя форма) или после 1 месяца жизни (поздняя форма), средний возраст детей на момент появления симптомов – 1-2 недели. Все проявления данной патологии можно разделить на 3 группы: соматические, абдоминальные, генерализованные. Первыми, как правило, появляются абдоминальные симптомы, которые почти сразу дополняются соматическими. Генерализованные проявления НЭК отмечаются при прогрессировании заболевания и возникновении перфорации кишечника, что, в зависимости от формы, может происходить через 1-3 дня.
В группу соматических симптомов входят патологические реакции организма на развитие НЭК: приступы апноэ, респираторный дистресс, олигурия, ухудшение микроциркуляции (позитивный симптом «белого пятна»). К абдоминальным признакам НЭК относятся симптомы раздражения брюшной полости и дисфункция ЖКТ: потеря аппетита, метеоризм, рвота желчью и кровью, отсутствие перистальтических шумов, мелена, асцит, покраснение кожи, отечность подкожной жировой клетчатки и резкое напряжение мышц передней брюшной стенки. Нарушения в организме ребенка, возникшие в результате прогрессирования некротического энтероколита новорожденных, объединяют в группу генерализованных проявлений. Сюда входят гипертермия, переходящая в гипотермию, артериальная гипотония, бледность и диффузный цианоз, выраженная вялость и сонливость, ДВС-синдром, дыхательная и сердечно-сосудистая недостаточность.
Большинство осложнений некротического энтероколита новорожденных, как правило, развиваются после проведенного хирургического лечения. Наиболее часто после оперативного вмешательства возникает кишечный свищ, синдром «укороченной кишки», хроническая диарея, демпинг-синдром, обезвоживание, синдром мальабсорбции, стриктура толстого кишечника, абсцесс, задержка физического развития. Также при НЭК могут встречаться патологические состояния, вызванные полным парентеральным питанием: дефицит витамина D (рахит), поражение печени (гепатит) и костей (деминерализация).
Диагностика НЭК новорожденных
Диагностика некротического энтероколита новорожденных включает в себя сбор анамнеза, клиническое, лабораторное и инструментальное обследование. Анамнестические данные могут помочь педиатру и детскому хирургу установить возможную этиологию, проследить за динамикой заболевания. При объективном осмотре выявляются присутствующие на данный момент клинические симптомы – абдоминальные, соматические и генерализованные проявления. Специфических лабораторных тестов для подтверждения НЭК не существует. Информативными являются следующие данные, полученные при проведении лабораторных исследований: лейкоцитоз со сдвигом формулы влево, лейкопения и тромбоцитопения в ОАК, ацидоз и гипоксемия при определении газового состава крови, гиперкалиемия и гипонатриемия в электролитном спектре, диспротеинемия и выявления С-реактивного протеина в белковом спектре, обнаружение крови в кале при пробе Грегерсена. С целью выявления инфекционного возбудителя проводится бактериальный посев, ИФА и ПЦР.
Ведущую роль в диагностике некротического энтероколита новорожденных играют инструментальные методы: рентгенография, УЗИ, КТ и МРТ. Они дают возможность визуализировать отек стенок кишечного тракта, плюс-ткань, наличие воздуха в брюшной полости, в просвете портальной или печеночной вен, а также отсутствие перистальтики на серии последовательных снимков. В педиатрии для подтверждения диагноза «некротический энтероколит новорожденных» и определения стадии заболевания применяется шкала Walsh и Kliegman. При использовании данной шкалы учитываются присутствующие у ребенка соматические симптомы, проявления со стороны желудочно-кишечного тракта и рентгенологические признаки. В зависимости от количества и выраженности проявлений выделяют подозреваемый НЭК (1а и 2а ст.), явный НЭК (2а и 2б ст.), прогрессирующий НЭК (3а и 3б ст.). Это имеет существенное значение при выборе тактики лечения.
Дифференциальная диагностика некротического энтероколита новорожденных проводится с такими патологиями как неонатальный сепсис, пневмония, пневмоперитонеум, кишечная непроходимость различного генеза, аппендицит новорожденного, бактериальный перитонит и спонтанная перфорация кишечника.
Лечение НЭК новорожденных
Тактика лечения некротического энтероколита новорожденных зависит от тяжести состояния ребенка и стадии заболевания. Детям с 1а, 1б и 2а стадиями показана консервативная терапия. С момента постановки диагноза отменяется энтеральное питание и проводится постановка назо- или орогастрального зонда с целью декомпрессии. Ребенок переводится на полное парентеральное питание (TPN) в соответствии с клиническими протоколами. Параллельно назначаются антибактериальные препараты из групп пенициллинов (ампициллин) и аминогликозидов II поколения (гентамицин) в комбинации с медикаментами, действующими на анаэробную микрофлору (метронидазол). При неэффективности выбранной антибиотикотерапии применяют цефалоспорины III-IV поколения (цефтриаксон) в сочетании с аминогликозидами III поколения (амикацин). Таким детям рекомендованы пробиотики и эубиотики для нормализации кишечной микрофлоры. Также проводят СВЧ-терапию, вводят иммуномодуляторы и гамма-глобулины.
Детям с 2б, 3а и 3б стадиями показано хирургическое вмешательство. Объем операции зависит от распространенности поражения кишечника. Как правило, проводится экономная резекция пораженного участка с формированием энтеростомы или колостомы. При локальных формах НЭК возможно наложение анастомоза по типу «конец в конец». После операции назначается инфузионная терапия и медикаментозное лечение, аналогичное более ранним стадиям.
Прогноз и профилактика НЭК новорожденных
Исход НЭК зависит от тяжести общего состояния ребенка и стадии заболевания. Так как данные показатели почти всегда отличаются нестабильностью, прогноз считается сомнительным даже на фоне полноценного лечения. Профилактика некротического энтероколита новорожденных включает в себя антенатальную охрану здоровья плода, рациональное ведение беременности, грудное вскармливание в физиологических объемах. Согласно некоторым исследованиям, риск развития заболевания снижается при использовании эубиотиков, пробиотиков и IgA у детей из группы риска. При высоком риске преждевременных родов применяют глюкокортикостероиды с целью профилактики РДС.
Источник
Многие недоношенные дети очень стойкие и удивляют своими способностями преодолевать значительные трудности. Также они очень уязвимы к инфекциям и сложностям, связанным с незрелостью органов. Вы можете ожидать, что Ваш ребенок прогрессирует за несколько дней, а он может, наоборот, регрессировать.
Каждая неделя недоношенности увеличивает риски того, что ребенок будет иметь проблемы со здоровьем. Дети, достигшие возраста 32 недель перед рождением, с намного меньшей вероятностью будут иметь усложнения, чем дети, рожденные раньше этого срока.
Наиболее распространенные осложнения, которые возникают из-за незрелости органов и иммунной системы, такие:
Низкое кровяное давление.
Низкий уровень сахара в крови.
Анемия.
Асфиктическая пневмония новорожденных.
Хроническое заболевание легких. (ранее известное как бронхопульмональная дисплазия).
Некротизирующий энтероколит.
Открытый артериальный проток.
Инфекции (в том числе сепсис).
Ретинопатия недоношенных.
Кровоизлияние в мозг, которое часто приводит к церебральному параличу или умственной отсталости.
Паховая грыжа.
Любой ребенок, рожденный до 37 полных гестационных недель, подвержен повышенному риску возникновения медицинских осложнений.
Дети, рожденные на 32 неделе или позже, наименее подвержены риску возникновения осложнений.
С каждой дополнительно неделей до 32-й, риск сильно увеличивается.
Дети, рожденные на 23-26 неделе, очень сильно недоразвиты и подвержены большому риску смерти или нарушений. Родители таких детей будут поставлены перед принятием непростых жизненноважных решений.
Низкое кровяное давление
Недоношенный ребенок может иметь низкое давление (гипотонию) после рождения. Некоторые причины этого: инфекция, кровопотеря и потеря жидкости.
Если давление немного понижено, это просто требует наблюдения. Если необходимо лечение, могут использовать нижеприведенные методы:
Медикаменты для увеличения давления.
Внутривенная жидкость (жидкость, введенная через вену).
Переливание крови, если низкое давление связано с кровопотерей.
Низкий уровень сахара в крови недоношенных новорожденных (гипогликемия)
Из-за того, что недоношенным новорожденным необходимо много энергии и у них мало энергии в запасе (гликоген), они предрасположены к низкому уровню сахара в крови.
Детей с низким уровнем сахара кормят внутривенно глюкозой, чаще дают кушать ртом, или используют оба способа. Как только ребенок наладит свой график кормлений ртом, уровень сахара вырастает до нормальной отметки.
Анемия недоношенных новорожденных
Анемия – это недостаточность кровяных телец. В то время как кровяные тельца переносят кислород по телу, анемия может отбирать необходимый кислород у организма. Низкий уровень кислорода у недоношенных новорожденных может привести к медицинским осложнениям или усугубить их.
Распространенные причины анемии у недоношенных детей:
Потеря крови из-за постоянных заборов крови на анализы.
Неспособность вырабатывать красные кровяные тельца, что приводит к «анемии недоношенных». К определенному моменту организм ребенка будет зрелым, чтобы вырабатывать кровяные тельца, анемия ослабится.
Мягкая форма анемии не требует лечения. Более серьезная форма анемии требует лечения с помощью переливания крови или медикаментов, которые улучшают способность организма вырабатывать красные кровяные тельца.
Асфиктическая пневмония (АП)
Асфиктическая пневмония (АП) новорожденных, которую еще называют гиалиново-мембранной болезнью новорожденных – это серьезное состояние, которое чаще всего возникает у детей, которые родились до того, как развились их легкие. Легкие полностью не надуваются или не функционируют нормально, что делает дыхание сложным или невозможным без медицинского вмешательства.
АП возникает, когда легкие ослабевают, чтобы вырабатывать ПАВ, субстанцию, которая помогает легким быть надутыми. Обычно легкие начинают вырабатывать ПАВ ближе к рождению. Дети, рожденные до того, как легкие смогут вырабатывать эту субстанцию, нуждаются в кислородной терапии или в вентиляционной машине, чтобы помочь им дышать. Обычно состояние легких улучшается после медикаментозной формы ПАВ, которая поступает в легкие через трубочку.
Хроническое заболевание легких
Хроническое заболевание легких, или бронхопульмональная дисплазия – это состояние, которое создает проблему с дыханием у новорожденных, особенно у тех, кто был рожден слишком рано. Легкие не могут захватить воздух или быть ослабленными, наполненными жидкостью или слизью.
Ребенок с хроническим заболеванием легких может хрюкать и дышать с присвистом, дышать слишком быстро и расширять ноздри. У ребенка также может натягиваться кожа между или над ребрами, когда ребенок вдыхает, также ребенок может быстро уставать во время кормления. Кожа новорожденного может выглядеть серой, бледной или быть в пятнах. Эти симптомы могут появиться через 3 дня после рождения.
Не существует теста для определения хронического заболевания легких. Врач сначала может заподозрить ее, если ребенок имеет проблемы с дыханием и нуждается в дополнительном кислороде на протяжении какого-то периода времени.
Лечение зависит от того, насколько серьезное состояние. Оно обычно включает в себя кислородную терапию и иногда использование вентилятора, также как и медикаменты и диетотерапия.
Открытый артериальный проток
Проток открытый артериальный – это кровеносный сосуд плода, который соединяет легочную артерию, которая переносит кровь к легким, и аорту, которая переносит кровь по телу так, что кровотечение обходит легкие. Обычно этот сосуд закрывается после рождения; когда он не закрывается, это называется открытым артериальным протоком.
Открытый артериальный проток позволяет обогащенной кислородом крови течь с аорты обратно в легочную артерию и в легкие вместо того, чтобы распространяться по всему телу. Из-за кровь предназначенной для возвращение в легкие, левая сторона сердца должна работать сильнее, чтобы получить достаточно крови для тела. Это может увеличить и ослабить сердце.
Хоть у некоторых детей нет симптомов открытого артериального протока, это отклонение часто может стать причиной различных симптомов, таких как плохое питание и короткость дыхания. В конечном счете, если проток не закроется, у ребенка может развиться инфекция внутреннего клапана сердца (инфекционный эндокардит) или сердечную недостаточность. Серьезность симптомов и то, разовьются ли симптомы, зависит от того, сколько крови перетекает через проток.
Лечение открытого артериального протока может состоять из медикаментов или операции. Операцию обычно не делают, пока ребенку не исполнится как минимум 6 месяцев, если не развились серьезные проблемы до этого срока.
Ретинопатия недоношенных
Ретинопатия недоношенных (РН) – это проблема, касающаяся глаз недоношенного ребенка, особенно тех, кто родился до 28 недели беременности. Поскольку незрелая сетчатка продолжает развиваться после рождения, аномальные кровеносные сосуды могут вырасти вокруг краев глаз; в тяжелых случаях, сетчатка отслаивается от глаза.
Причины РН плохо изучены. Из-за того, что слишком большое или маленькое количество кислорода может усугубить РН, кислородная терапия для недоношенных детей применяется очень аккуратно.
Ретинопатия недоношенных может быть в мягкой форме и может пройти сама. Мягкая форма РН может стать причиной косоглазия (смещенные глаза), близорукости или и того, и другого. В более тяжелых случаях необходима операция, чтобы предотвратить ухудшение зрения или слепоту.
Дети с РН или те, у кого есть риск РН, нуждаются в частых проверках офтальмологом (специалистом по глазам). Многие дети с РН становятся близорукими к 2 годам.
Кровоизлияние в мозг у недоношенных детей
На протяжении первой недели жизни после рождения у некоторых детей случается кровоизлияние в мозг, лечения для которого еще не нашли. Кровоизлияние часто носит мягкий характер (ранжируется как І или ІІ степень), и приводит к незаметным повреждениям мозга. Если излияние ІІІ степени, это повышает риск развития гидроцефалии (накопление чрезмерной спинномозговой жидкости в мозгу), повреждения мозга или и того, и другого. Излияние IV степени – это сильное кровоизлияние, которое может привести к повреждению мозга, которое заметно на изображении.
Чем более незрелый мозг, тем более хрупкие мозговые кровеносные сосуды и тем более они чувствительны к изменению давления крови. Под самым большим риском возникновения кровоизлияния сильно недоношенные дети. У приблизительно 80% новорожденных, рожденных на 23-24 неделях, развилось такое состояние, очень редко – среди новорожденных около 35 недели.1
Несмотря на гестационный возраст новорожденного, риск кровоизлияния в мозг значительно уменьшается после 72 часов жизни и совсем незначителен после 7 дней жизни. Сильно недоношенным детям часто делают ультразвук головы (черепной ультразвук) на 3-7 дне жизни, чтобы проверить на предмет кровоизлияния. Тех, у кого проявляются симптомы кровоизлияния, проверяют регулярно.
Превентивные меры, которые могут уменьшить риск кровоизлияния в мозг, такие:
Кортистероидное лечение, проводимое матери перед родами. Это лечение обычно проводится, чтобы помочь легким плода развиться перед преждевременными родами. Считается, что это также помогает сделать кровеносные сосуды менее уязвимыми при кровотечении.
Индометацин, который дается новорожденному после рождения. Это негормональное противовоспалительное средство (НПС) сжимает кровеносные сосуды мозга (вазоконстрикция), что помогает контролировать внезапные изменения в кровяном давлении мозга.
Гидроцефалия
Гидроцефалия, или «вода в мозгу», – это накопление излишней спинномозговой жидкости (СМЖ) в мозгу. Давление излишней жидкости может привести к повреждению мозга, если это не лечить.
Обычно СМЖ течет через камеры мозга, называемые желудочками, потом вокруг мозга и спинного мозга, обеспечивая питательными веществами и образуя что-то вроде защитной подушки. Гидроцефалия возникает из-за нарушения равновесия между выработкой мозгом СМЖ и возможностью тела его распространять и впитывать.
Гидроцефалия чаще всего встречается после рождения и обычно становится незаметной до достижения ребенком 9 месяцев. Реже гидроцефалия развивается после серьезного заболевания (такого как менингит) или повреждения головы.
Лечение обычно включает в себя осушивание жидкостей в мозге с помощью трубки, которая называется шунт.
После лечения дети с гидроцефалией могут не сталкиваться с долгосрочными проблемами. Некоторые могут иметь лишь незначительные проблемы, такие как трудности в обучении. Гидроцефалия может быть пожизненной или стать причиной сложных отклонений, если ее не лечить.
Задержка умственного развития
Задержка умственного развития означает уровень интеллекта ниже среднего. Диагноз «Задержка умственного развития» базируется на тестах уровня интеллекта (IQ) и на других тестах.
Задержка умственного развития поделена на категории в соответствии с баллами IQ:
Мягкая задержка (IQ = 50-70): мягкая задержка умственного развития может не быть очевидной.
Дети с мягкой формой задержки обычно учатся играть, разговаривать и уделать другие ежедневные дела, но медленнее, чем дети без задержки в развитии.
Они могут научиться читать, писать и освоить базовую математику.
Повзрослев, они обычно могут жить независимо и самостоятельно обеспечить себя всем необходимым.
Умеренная задержка (IQ = 35-55): такие дети развиваются значительно медленнее, чем здоровые дети.
Обычно они не развиваются дальше, чем уровень 2-го класса. Тем не менее, они могут выполнять стандартные задания и могут разговаривать простыми предложениями.
Повзрослев, они могут выполнять хорошо контролируемую работу и могут жить в группах. Также они могут жить отдельно.
Тяжелая задержка (IQ = 20-35): таким детям сложно научиться самообслуживанию, такому как поесть.
Они развивают очень мало, у них слабые коммуникативные навыки, но могут понимать и реагировать на то, что говорят другие.
Они обычно могут делать тоже, что и 2-3-хлетний ребенок, например, кушать, пользоваться ванной, одеваться.
Повзрослев, они не могут жить отдельно.
Паховая грыжа
Паховая грыжа возникает тогда, когда маленький кусок кишки выступает из-за пахового канала – пересекает или открывается через мышцы брюшной стенки – в пах. Выпуклость обычно содержит в себе внутреннюю ткань живота, также как и жировую ткань внутри живота или петлю кишечника.
Есть два вида паховой грыжи:
Прямая паховая грыжа возникает, когда слабая ткань развивается в нижних брюшных мышцах. Обычно причина грыжи неизвестна, но считается, что это поднятие тяжестей, растяжение, или результат тучности, беременности или частых запоров.
Непрямая паховая грыжа возникает, когда паховый канал не закрылся до рождения. Грыжа может возникнуть в мужской мошонке или в складках кожи, если открыть влагалище женщины. Это самые распространенные виды паховой грыжи, и они могут возникнуть при рождении или позже. Непрямая грыжа больше распространена среди мужчин.
Симптомы паховой грыжи могут проявиться постепенно или внезапно и могут включать в себя выпуклость в паху или в мошонке, дискомфорт, боль или чувство тяжести. Другие симптомы могут развиваться, если ткань в паху ущемлена или если кровоснабжение к зажатым тканям ограничено.
Паховая грыжа может требовать операционного вмешательства. В некоторых случаях, маленькие и безболезненные грыжи не требуют лечения.
Некротизирующий энтероколит
Некротизирующий энтероколит – это инфекция и воспаление внутренней стенки кишечника, которое поражает некоторых новорожденных, обычно рожденных раньше срока. Заболевание может протекать в мягкой и сильной форме, которая приводит к непроходимости кишечника и отмиранию тканей, может угрожать жизни.
Симптомами у новорожденных могут быть: вздутый или сильно мягкий живот, плохой аппетит или рвота, незначительный или сильный запор, темный, черный стул или стул с кровью. У новорожденного может быть низкая или нестабильная температура тела, ребенок может быть вялым и апатичным.
Считается, что некротизирующий энтероколит возникает из-за комбинации нескольких факторов, в том числе преждевременные роды и незрелая иммунная и пищеварительная системы.
Некротизирующий энтероколит требует специального ухода в больнице. Новорожденных кормят внутривенно, чтобы дать кишечнику время вылечиться, также применяют антибиотики, чтобы предотвратить или вылечить инфекцию. Иногда необходима операция.
Источник