Лактозодефективные кишечные палочки что это

Таблица 1. Качественный и количественный состав основной микрофлоры толстого кишечника у здоровых людей (Кое/г Фекалий)
(Отраслевой стандарт 91500.11.0004-2003 “Протокол ведения больных. Дисбактериоз кишечника” – УТВЕРЖДЕНО приказом Минздрава России от 09.06.2003 г. N 231)
| Виды микроорганизмов | Возраст, годы | ||
| < 1 | 1-60 | > 60 | |
| Бифидобактерии | 1010 – 1011 | 109 – 1010 | 108 – 109 |
| Лактобактерии | 106 – 107 | 107 – 108 | 106 – 107 |
| Бактероиды | 107 – 108 | 109 – 1010 | 1010 – 1011 |
| Энтерококки | 105 – 107 | 105 – 108 | 106 – 107 |
| Фузобактерии | < 106 | 108 – 109 | 108 – 109 |
| Эубактерии | 106 – 107 | 109 – 1010 | 109 – 1010 |
| Пептострептококки | < 105 | 109 – 1010 | 1010 |
| Клостридии | <= 103 | <= 105 | <= 106 |
| Эшерихии (E.coli): | |||
| E.coli типичные | 107 – 108 | 107 – 108 | 107 – 108 |
| E.coli лактозонегативные | < 105 | < 105 | < 105 |
| E.coli гемолитические | |||
| Другие условнопатогенные энтеробактерии <*> | < 104 | < 104 | < 104 |
| Стафилококк золотистый | |||
| Стафилококки (сапрофитный, эпидермальный) | <= 104 | <= 104 | <= 104 |
| Дрожжеподобные грибы рода Candida | <= 103 | <= 104 | <= 104 |
| Неферментирующие бактерии <**> | <= 103 | <= 104 | <= 104 |
<*> – представителиродов Klebsiella, Enterobacter, Hafnia, Serratia, Proteus, Morganella, Providecia,
Citrobacter идр.
<**> – Pseudomonas, Acinetobacter идр.
Микроорганизмы, перечисленные в бланке анализа на дисбактериоз, можно разделить на три группы:
- молочнокислые бактерии нормальной микрофлоры – преимущественно бифидобактерии и лактобактерии,
- патогенные энтеробактерии,
- условно-патогенная флора (УПФ).
Молочнокислые бактерии
Основу нормальной микрофлоры кишечника составляют молочнокислые бактерии – бифидобактерии, лактобактерии и пропионовокислые бактерии с преобладанием бифидобактерий, которые выполняют ключевую роль в поддержании оптимального состава биоценоза и его функций. Падение количества бифидобактерий и лактобактерий ниже нормы говорит о наличии проблем в организме. Как минимум, это воспаление на слизистых оболочках и снижение иммунной защиты.
Патогенные энтеробактерии
Патогенные энтеробактерии – это бактерии, способные вызывать острые кишечные инфекции (возбудители брюшного тифа – сальмонеллы, возбудители дизентерии – шигеллы, возбудители йерсиниоза – йерсинии и др.) Их присутствие в кале – это уже не просто дисбактериоз, а показатель опасного инфекционного заболевания кишечника.
Условно-патогенная флора (УПФ)
К условно-патогенной флоре относятся лактозонегативные энтеробактерии, клостридии, различные кокки и др. Суть этих микробов отражена в названии группы: «условно-патогенные». В норме они не вызывают нарушений. Многие из них даже могут быть в определенной степени полезны организму. Но при превышении нормы и/или неэффективности иммунной защиты они могут стать причиной серьезных заболеваний. Конкурируя с полезными бактериями, условно-патогенная флора может войти в состав микробной пленки кишечника и стать причиной функциональных нарушений, воспалительных и аллергических заболеваний.
Возможно попадание условно-патогенной флоры через кишечную стенку в кровь и распространение ее по организму (транслокация), что особенно опасно для детей раннего возраста и лиц с выраженными иммунодефицитами, у которых эти микроорганизмы могут вызвать различные заболевания, в том числе, опасные для жизни.
Пояснения к таблице
Обычно количество обнаруженных бактерий в бланке анализа обозначается числом 10 в какой-либо степени: 103, 105, 106 и т. д. и аббревиатурой КОЕ/г, что означает количество живых, способных к росту бактерий в 1 г фекалий.
Аббревиатура «abs» напротив названия бактерии означает, что данный микроорганизм не был обнаружен в пределах нормы и выше ее, а значения ниже нормы (субнормальные), как несущественные, не смотрели.
Бифидобактерии
Бифидобактерии – это основа нормальной микрофлоры толстого кишечника. В норме их содержание в кишечнике должно быть у детей до года – 1010 – 1011, у взрослых – 109-1010 КОЕ/г. Заметное снижение количества бифидобактерий – главный признак наличия дисбактериоза и иммунных нарушений.
Дефицит бифидобактерий приводит к росту интоксикации, нарушению процессов углеводного обмена, всасывания и усвоения в кишечнике витаминов, кальция, железа и других микро- и макроэлементов. Без биопленки из бифидобактерий меняется структура и нарушаются функции слизистой оболочки кишечника, уменьшается количество иммунных клеток и их активность, повышается проницаемость кишечника для чужеродных агентов (токсинов, вредоносных микробов и др.). В результате значительно увеличивается токсическая нагрузка на печень и почки, повышается риск развития инфекций и воспалений, авитаминозов и различных микроэлементозов.
Лактобактерии
Лактобактерии, так же как и бифидобактерии, являются одной из главных составляющих нормальной микрофлоры человека. Норма содержания в кишечнике у детей до года – 106 – 107, у взрослых – 107-108 КОЕ/г. Значительное снижение количества лактобактерий говорит не только о дисбиотических нарушениях, но и о том, что организм находится в состоянии хронического стресса, а также о снижении противовирусной и противоаллергической защиты, нарушениях липидного обмена, обмена гистамина и т. д. Дефицит лактобактерий сильно повышает риск развития аллергических реакций, заболевания атеросклерозом, неврологических нарушений, сердечно-сосудистых заболеваний, может также стать причиной запоров, развития лактазной недостаточности.
Бактероиды
Бактероиды – условно-патогенные бактерии. Вторая по численности (после бифидобактерий) группа кишечных микроорганизмов, особенно у взрослых (норма – до 1010 КОЕ/г), у детей до года – 107-108. При содержании в пределах нормы они выполняют много полезных для организма функций. Но при нарушении баланса в кишечном микроценозе или при превышении нормы бактероиды могут приводить к многообразным инфекционно-септическим осложнениям. При избыточном росте бактероиды могут подавлять рост кишечной палочки, конкурируя с ней за кислород. Бесконтрольный рост бактероидов и проявление ими агрессивных свойств ограничивают основные компоненты защитной флоры – бифидобактерии, лактобациллы и пропионовокислые бактерии.
Энтерококки
Энтерококки – наиболее часто встречающиеся в кишечнике здоровых людей условно-патогенные микроорганизмы. Норма содержания для детей до года – 105-107, для взрослых – 105-108 (до 25% от общего количества кокковых форм). Некоторые специалисты считают их безобидными. На деле же многие энтерококки способны вызывать воспалительные заболевания кишечника, почек, мочевого пузыря, репродуктивных органов не только при превышении ими допустимого количества (при содержании более 107), но и в количестве, соответствующем верхней границе нормы (106-107), особенно у людей со сниженным иммунитетом.
Фузобактерии
Фузобактерии – условно-патогенные бактерии, основные места обитания которых в человеческом организме – толстая кишка и респираторный тракт. В полости рта у взрослого человека содержится 102-104 КОЕ/г фузобактерий. Допустимое количество в кишечнике у детей до года < 106, у взрослых – 108 – 109.
Некоторые виды фузобактерий при иммунодефицитах могут вызывать вторичные гангренозные и гнойно-гангренозные процессы. При ангине, герпетическом стоматите, гипотрофии у детей, при иммунодефицитных состояниях возможно развитие фузоспирохетоза – некротического воспалительного процесса на миндалинах, слизистой оболочки полости рта.
Эубактерии (лат. Eubacterium)
Относятся к основной резидентной микрофлоре как тонкой, так и толстой кишки человека и составляют значительную часть от всех населяющих желудочно-кишечный тракт микроорганизмов. Допустимое количество эубактерий в кале здоровых людей: у детей первого года – 106-107 КОЕ/г; у детей старше года и взрослых, включая пожилых – 109-1010 КОЕ/г.
Примерно половина видов эубактерий, обитающих в организме человека, могут участвовать в развитии воспаления ротовой полости, формировании гнойных процессов в плевре и легких, инфекционного эндокардита, артрита, инфекций мочеполовой системы, бактериального вагиноза, сепсиса, абсцессов мозга и прямой кишки, послеоперационных осложнений.
Повышенное содержание эубактерий обнаруживается в фекалиях больных полипозом толстой кишки. Эубактерии редко встречаются у детей, находящихся на грудном вскармливании, но у детей, находящихся на искусственном вскармливании могут выявляться в количестве, соответствующем норме взрослого человека.
Пептострептококки
Пептострептококкиотносятся к нормальной микрофлоре человека. Норма содержания в кале у детей до года < 105, у детей старше года и взрослых – 109 – 1010. В организме здорового человека пептострептококки обитают в кишечнике (в основном, в толстой кишке), ротовой полости, влагалище, дыхательных путях. Обычно пептострептококки являются возбудителями смешанных инфекций, проявляясь в ассоциациях с другими микроорганизмами.
Клостридии
Условно-патогенные бактерии, представители гнилостной и газообразующей флоры, количество которых зависит от состояния местного иммунитета кишечника. Основное место обитания в человеческом организме – толстая кишка. Допустимое количество клостридий у детей до года не более 103, а у взрослых – до 105 КОЕ/мг.
В комплексе с другой условно-патогенной флорой клостридии могут вызывать разжижение стула, понос, повышенное газообразование, которое наряду с тухлым запахом кала (симптомы гнилостной диспепсии) является косвенным признаком повышенной численности и активности этих бактерий. В определенных условиях они могут быть причиной некротического энтерита, вызывать пищевую токсикоинфекцию, сопровождающуюся водянистой диареей, тошнотой, коликами в животе, иногда лихорадкой.
При приеме некоторых антибиотиков клостридии могут вызывать антибиотикоассоциированную диарею или псевдомембранозный колит. Кроме проблем с кишечником, клостридии могут вызывать заболевания мочеполовых органов человека, в частности, острый простатит. Симптомы воспаления, спровоцированного клостридиями во влагалище, имеют сходство с симптомами кандидозного вагинита («молочницы»).
E.coli типичные (эшехирии, кишечная палочка типичные), т. е. с нормальной ферментативной активностью
Условно-патогенные микроорганизмы, которые вместе с бифидо- и лактобактериями относятся к группе защитной микрофлоры кишечника. Эта палочка препятствует заселению кишечной стенки чужеродными микроорганизмами, создает комфортные условия для других важных бактерий кишечника, например, поглощает кислород, являющийся ядом для бифидобактерий. Это главная «фабрика витаминов» в организме.
В норме общее содержание кишечной палочки – 107-108 КОЕ/ мг (что соответствует 300-400 млн/г). Повышенный уровень E. coli в кишечнике может стать причиной воспаления, сопровождающегося нарушениями стула и болями в животе. А ее проникновение из кишечника в другие экониши организма (мочевыводящие пути, носоглотку и т. д.) – причиной цистита, заболеваний почек и др.
Снижение этого показателя является сигналом о высоком уровне интоксикации в организме. Сильное снижение количества кишечной палочки типичной (до 105 КОЕ/ мг и ниже) – косвенный признак присутствия паразитов (например, глистов или паразитических простейших – лямблий, бластоцист, амеб и др.). Кроме паразитов, среди самых вероятных причин снижения уровня кишечной палочки существование в организме очагов хронической инфекции, повышенная аллергизация, дисфункции или заболевания различных органов, в первую очередь печени, почек, поджелудочной и щитовидной желез. Чтобы избежать ошибочного диагноза и, соответственно, неправильного лечения, рекомендуется сначала исключить паразитарное заражение.
Кишечная палочка со сниженной ферментативной активностью (E.coli лактозонегативные).
Норма содержания – не более 105 КОЕ/г. Это неполноценная разновидность кишечной палочки, которая прямой опасности обычно не представляет. Но эта палочка – «тунеядец». Она занимает место полноценной E.coli, не выполняя при этом присущих полноценной E.coli полезных функций. В результате организм недополучает необходимые ему витамины, ферменты и другие полезные вещества, синтезируемые полноценными эшерихиями, что в итоге может привести к серьезным обменным нарушениям и даже воспалительным заболеваниям. Присутствие этой палочки в количестве выше допустимой нормы – всегда признак начинающегося дисбактериоза и, наряду со снижением общего количества кишечной палочки, может быть косвенным показателем присутствия в кишечнике паразитических простейших или глистов.
E.coli гемолитическая (гемолитическая кишечная палочка)
Патогенный вариант кишечной палочки. В норме должна отсутствовать. Ее присутствие требует иммунокоррекции. Может вызывать аллергические реакции и различные кишечные проблемы, особенно у маленьких детей и лиц с ослабленным иммунитетом. Часто образует патогенные ассоциации с золотистым стафилококком, но в отличие от него практически не встречается в составе грудного молока.
Другие условно-патогенные энтеробактерии
(протеи, серрации, энеробактеры, клебсиеллы, хафнии, цитробактеры, морганеллы и др.) Большая группа лактозонегативных энтеробактерий большей или меньшей степени патогенности. Допустимое количество этих микроорганизмов менее 104 КОЕ/г. Большее количество этих бактерий является признаком дисбактериоза. Значительное превышение нормы (более 106) может приводить к воспалительным заболеваниям кишечника (проявляются нарушениями стула, болями), урогенитальной сферы и даже ЛОР-органов, особенно у детей раннего возраста и лиц с пониженным иммунитетом.
Наиболее неприятные бактерии данной группы:
- Протеи – чаще всего с ними связаны запоры, но они также могут вызывать острые кишечные инфекции, заболевания мочевыводящих путей и почек человека, в частности, острый и хронический простатит, цистит, пиелонефрит.
- Клебсиеллы – прямые антагонисты (конкуренты) лактобактерий, приводят к развитию аллергий, запоров, проявлениям лактазной недостаточности. Косвенный признак избыточного присутствия клебсиеллы – зеленый стул со слизью, кислый запах кала (симптомы бродильной диспепсии).
Стафилококк золотистый (S. aureus)
Один из наиболее неприятных представителей условно-патогенной флоры. В норме должен отсутствовать, особенно у детей. Для взрослых допустимо содержание 103 КОЕ/г.
Даже небольшие количества золотистого стафилококка могут вызвать выраженные клинические проявления (аллергические реакции, гнойничковые кожные высыпания, дисфункции кишечника), особенно у детей первых месяцев жизни. Кроме кишечника и кожных покровов, стафилококки в немалых количествах живут на слизистых оболочках носа и могут вызывать воспалительные заболевания носоглотки, отиты.
Главные условия, от которых зависит степень патогенности стафилококков и восприимчивость к ним организма, – это активность иммунной защиты организма, а также количество и активность конкурирующих со стафилококком бифидо- и лактобактерий, которые способны нейтрализовать его вредоносность. Чем больше в организме сильных, активных бифидобактерий и лактобактерий, тем меньше вреда от стафилококка (клинических проявлений может не быть, даже если его количество достигло 105 КОЕ/г). Чем больше дефицит бифидо- и лактобактерий и чем слабее иммунная защита организма, тем активнее стафилококк.
В группе риска сладкоежки и люди, имеющие слабый иммунитет. В первую очередь это дети – недоношенные, рожденные в результате проблемной беременности, кесарева сечения, лишенные естественного грудного скармливания, перенесшие антибиотическую терапию. В организм ребенка стафилококки могут попасть через материнское молоко, со слизистых и кожи мамы (тесный контакт).
Стафилококки сапрофитный, эпидермальный (S. epidermidis, S. saprophyticus)
Относится к условно-патогенной микрофлоре. При превышении нормальных значений (104 КОЕ/г или 25% от общего количества кокков) эти стафилококки способны вызывать определенные нарушения. Как правило, они выступают в роли вторичной инфекции. Кроме кишечника живут в верхних слоях кожи, на слизистых оболочках рта, носа и наружного уха. Патогенность микроорганизма усиливается при значительном снижении защитных сил организма, при длительных хронических заболеваниях, стрессах, переохлаждении, иммунодефицитных состояниях.
Дрожжеподобные грибы рода Candida
Максимально допустимое количество – до 104. Превышение этого уровня говорит о снижении иммунной защиты организма и очень низком рН в зоне обитания кандиды, а также может быть следствием применения антибиотиков и большого количества углеводов в рационе. При повышенном количестве этих грибов на фоне снижения количества нормальной флоры на слизистых оболочках ротовой полости и половых органов могут появится симптомы кандидоза, чаще называемого молочницей. Инфицирование грибами кишечника на фоне дефицита основных групп кишечных бактерий говорит о системном кандидозе, неработающем иммунитете и повышении риска развития диабета.
Неферментирующие бактерии (в некоторых бланках обозначены как «Прочие микроорганизмы»)
Pseudomonas, Acinetobacter и др. редко встречающиеся в кишечнике человека виды бактерий, самым опасным из которых является синегнойная палочка (Pseudomonas aerugenosa). Максимально допустимое количество у взрослых – не более 104. Как правило, их обнаружение в количестве выше нормы требует антибактериальной терапии и иммуннокоррекции.
Наши пробиотики:
Посмотреть все
Источник
 Автор: Трубачева Е.С., врач – клинический фармаколог
Автор: Трубачева Е.С., врач – клинический фармаколог
Этой статьей мы начинаем рассмотрение представителей микробиологического мира, с которыми чаще всего встречаем в ежедневной клинической практике, и темой сегодняшнего разговора будет кишечная палочка, она же Escherichia coli (E.coli).
Актуальность обсуждения данного микроорганизма состоит в том, что кишечная палочка – это чемпион по созданию проблем как для пациентов, так и для медицинского персонала стационаров и в амбулаторной службе. Хуже нее только клебсиелла, но о ней поговорим попозже. При этом E.coli не летает по воздуху и не имеет ножек для самостоятельного перемещения и инфицирование ею – это почти всегда «болезнь грязных рук». С патологией, вызванной этим возбудителем, пациент может прийти к любому врачу, а медицинский персонал может принести уже на своих руках кишечную палочку любому пациенту с одной лишь разницей – это будет не дикий и симпатичный зверек, убиваемый обычным амоксицилином, а вооруженная до зубов особь, умеющая очень эффективно убивать сама. То есть это один из тех врагов, которых совершенно точно надо знать в лицо.
Микробиологические аспекты
E.coli относится к типичным представителям семейства Enterobacteriaceae, являясь грамотрицательной бактерией, факультативным анаэробом в составе нормальной кишечной микрофлоры человека. Но тут же становится патогеном, выбравшись из среды нормального обитания, хотя отдельные штаммы являются патогенными и для желудочно-кишечного тракта. То есть кишечная палочка относится к кишечным комменсалам, кишечным патогенам и внекишечным патогенам, каждый из которых мы кратко разберем.
К штаммам E.coli, действующим как кишечные патогены и встречающимся чаще других, относятся:
- Штамм серотипа O157:H7 (STEC O157) или так называемый энтерогеморрагический штамм E.coli, который является причиной 90% случаев геморрагических колитов и 10% случаев гемолитико-уремического синдрома. Встречается достаточно часто, а если вы работаете в стационарах плановой помощи, то это один из обязательных анализов для принятия решения о госпитализации, так что так или иначе он на слуху. Проблема инфицирования этим возбудителем связана с употреблением плохо термически обработанной пищи и передачи штамма контактным путем от человека к человеку, проще говоря, через руки.
- Второй крайне опасный высоко-патогенный штамм кишечной палочки – O104:H4, вызвавший в Германии 2011 году эпидемию с высоким уровнем смертности среди пациентов с пищевыми токсико-инфекциями вследствие развития гемолитико-уремического синдрома. Если помните, это была очень громкая история с перекрытиями границ для испанских огурцов, потом вообще для всей плодоовощной продукции из Европы в Россию, пока искали хотя бы источник, не говоря уж о виновнике тех событий. Окончательно виновными тогда были обозначены листья салата, в поливе которых использовалась вода с признаками фекального заражения, а затем речь пошла уже о пророщенных семенах, которые так же полили фекально-зараженной водичкой. Так вышли на конкретный штамм E.coli – O104:H4, который, подвергшись санации антибиотиком, выплескивает эндотоксин, вызывающий гемолиз и острую почечную недостаточность. В итоге – массовая летальность пациентов, получавших антибиотики.
Затем тот же штамм обнаружился при вспышке ПТИ в Финляндии, но к тому времени пациентов с диареями до появления микробиологических результатов перестали лечить бактерицидными антибиотиками и ситуация была купирована в зародыше.
И третий громкий (для нашей страны) случай – это массовое заболевание питерских школьников в Грузии, где так же был выявлен этот штамм (пресс-релиз Роспотребнадзора по данному случаю лежит здесь).
- Кроме вышеперечисленных существуют энтеротоксические (вызывают «диарею путешественников»), энтероинвазивные (вызывают кровавую диарею) и энтеропатогенные (водянистая диарея у новорожденных) штаммы.
Когда кишечная палочка выступает внекишечным патогенном? Почти всегда, когда обнаруживается вне места своего нормального обитания.
- Заболевания мочевыводящий путей. Здесь E.coli является абсолютным лидером и играет ведущую роль в развитии:
- Острых циститов
- Пиелонефритов
- Абсцессов почек и
- Простатитов
Этот факт объясняется близким анатомическим расположением двух систем и огрехами в личной гигиене, что позволяет на этапе эмпирической терапии вышеперечисленных заболеваний сразу же назначать препараты, активные в отношении кишечной палочки.
- Заболевания желудочно-кишечного тракта:
- Диарея путешественников
- Интраабдоминальные абсцессы и перитониты, чаще всего носящие вторичный характер (прободение кишки в результате первичного заболевания, либо при дефектах оперативного вмешательства)
- Инфекции центральной нервной системы у очень ослабленных пациентов, результатом чего будет развитие менингитов. Встречается в основном у лиц старческого возраста и новорожденных. Кроме того, в случае внутрибольничного заражения менингит может развиться в результате плохой обработки рук медицинского персонала перед оперативным вмешательством или перевязками.
- Инфекции кровотока, а именно сепсис, как продолжение развития заболеваний мочевыводящих путей, ЖКТ и билиарного тракта вследствие метастазирования очага инфекции. Лечению поддается крайне тяжело, особенно если задействованы внутрибольничные штаммы, летальность чрезвычайно высокая.
- Инфекции кожи и мягких тканей как следствие раневых инфекций после вмешательств на органах брюшной полости.
- Внутрибольничные пневмонии, вызванные устойчивыми штаммами кишечной палочки, целиком связаны с дефектами ухода за пациентом и фактором чистоты, точнее ее отсутствия, рук медицинского персонала или ухаживающих родственников. Факт внутрибольничного заражения доказывается элементарно, что будет наглядно продемонстрировано в следующем разделе.
- Послеродовые (и не только) эндометриты. Вынуждены упомянуть и эту патологию, так как инфицирование кишечной палочкой встречается все чаще и чаще, а большой настороженности нет. Как результат, можно очень сильно промахнуться с антибактериальной терапией и, как следствие, прийти к экстирпации органа в виду неэффективности антибиотикотерапии. Натолкнуть на мысль может более позднее, чем обычно, поступление и более агрессивное, чем обычно течение. Дополнительный осмотр прианальной области так же может натолкнуть на вероятность развития именно такого инфицирования.
(часть вторая) Практические вопросы диагностики и лечения.
Когда мы можем заподозрить, что перед нами пациент с инфекцией, вызванной кишечной палочкой?
- Пациенты с диареей, приехавшие из отпуска и все-таки смогшие прийти на прием (диарея путешественников или энтеротоксигенные штаммы E.coli).
- Пациенты со всеми заболеваниями мочевыделительной системы, в том числе беременные, но строго с наличием симптоматики (не надо лечить бессимптомную бактериурию, иначе вырастите резистентные штаммы и создадите проблему и себе, и женщине, и роддому в последующем).
- В стационарах – нозокомиальные пневмонии, послеоперационные менингиты, перитониты, сепсисы и т. д., носящие вторичный характер.
Подтвердить или полностью исключить кишечную палочку из возбудителей может только микробиологическое исследование. Конечно, в современных условиях микробиология уже становится практически эксклюзивом, но мы пришли учиться, а учится надо на правильных примерах, поэтому далее будет рассмотрен ряд антибиотикограмм, выполненных автоматизированными системами тестирования. Вдруг вам повезет, и в вашем лечебном учреждении все уже есть или в ближайшее время будет, а вы уже умеете с этим всем работать?
Если вы читаете данный цикл по порядку, то в базовом разделе по микробиологии был выложен ряд антибиотикограмм некоего микроорганизма в контексте нарастания антибиотикорезистентности, и это была наша сегодняшняя героиня – кишечная палочка.
- Начнем с дикого и крайне симпатичного штамма E.coli, который живет в кишечнике и обеспечивает синтез витамина К. С ним сталкиваются доктора амбулаторной службы у пациентов с инфекциями мочевыводящих путей или в случае госпитализации у пациентов, которые не получали антибиотики около года. И именно такую чувствительность мы имеем в виду, когда назначаем эмпирическую антибиотикотерапию
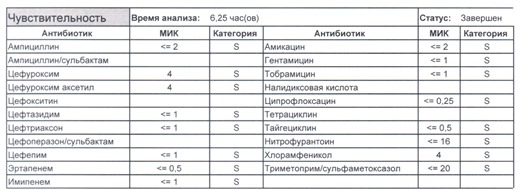
Чем лечим?
- Как видите, зверь чувствителен абсолютно ко всему, и это как раз тот случай, когда можно свободно пользоваться табличными материалами справочников или клинических рекомендаций, так как механизмы резистентности полностью отсутствуют.
- Если в ваши руки попал пациент, которого в течение последнего полугодия лечили антибиотиками пенициллинового ряда, то антибиотикограмма может выглядеть следующим образом.
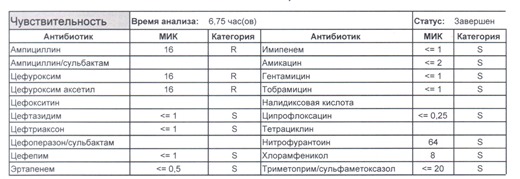
Если такая кишечная палочка окажется внекишечным патогенном, и перед вами будет беременная и ИМП (самый частый случай), то нам необходимо преодолеть резистентность к пенициллинам, то есть подавить деятельность пенициллиназ. Соответственно высокую эффективность продемонстрируют препараты с ингибиторами бета-лактамаз, чаще всего амоксициллина/клавуланат, как наиболее безопасный и эффективный. Единственное, пациентку необходимо предупредить, что в результате стимуляции рецепторов кишечника может развиться антибиотик-ассоциированная диарея.
- Отдельно хотелось бы обратить внимание на следующий штамм E.coli, как типичного обладателя бета-лактамаз расширенного спектра. И эти БЛРС чаще всего вырабатываются в результате неуемного использования цефалоспоринов третьего поколения и совершенно конкретного его представителя – цефтриаксона.
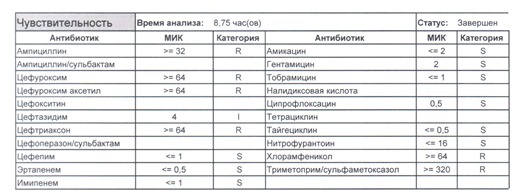
В каких ситуациях мы можем увидеть (или подумать) о таком звере:
- Пациент сам рассказывает, что получал цефтриаксон в промежутке полугодия
- Пациент был переведен из другого стационара (хотя там можно будет и следующую картинку обнаружить)
- Пациент ничего не получал, и вообще в больнице не лежал, но возбудитель попал с рук медицинского персонала, вызвав внутрибольничную инфекцию
- И самый простой случай – посев был взят в момент проведения терапии цефтриаксоном
Что делать?
- Помнить, что перед вами пациент – носитель возбудителя, который может быть перенесен и создаст серьезную опасность жизни более слабому. Поэтому и персонал, и сам пациент, должны неукоснительно соблюдать санитарные правила для недопущения переноса.
- Чем лечить? Так как ни один ингибитор бета-лактамаз тут уже не работает, БЛРС отлично их разрушают, то выбор будет невелик, и лучше, чтобы этот выбор делал специально-обученный специалист – врач-клинический фармаколог, так как в данной ситуации важную роль играют не только данные о чувствительности и резистентности, но и МПК возбудителя, например. Не говоря уже о факторе фармакодинамики и самом очаге локализации инфекции.
- Если клин. фарма нет или он не специально обученный – тогда лечим в соответствии с клиническими рекомендациями по соответствующей нозологии из раздела «препараты резерва». Не лишним будет обсудить ситуацию с врачом-бактериологом клинической лаборатории, делающей для вас посевы.
- Один из самых плохих вариантов, который вы можете увидеть
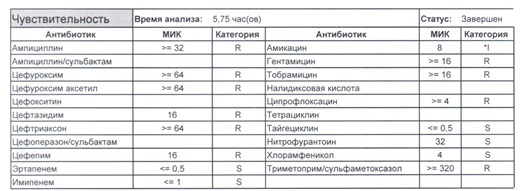
Подобный пациент не придет к вам своими ногами, его не увидит амбулаторная служба, это абсолютно стационарные больные, и если их привезут, то только из другого лечебного учреждения. Чаще всего это пациенты палат интенсивной терапии или реанимации, и такой возбудитель носит на 100% нозокомиальный характер.
Когда можем его обнаружить:
- вторичные перитониты,
- нозокомиальные пневмонии,
- пиелонефриты,
- послеоперационные менингиты,
- сепсис и т. п.
И всегда это будет ятрогенное поражение как следствие неправильной гигиены рук персонала либо обработки инструментария. Можно возразить «но как же тяжелые перитониты?». Отвечу тем, что для тяжелых перитонитов без дефектов ухода наиболее характерен штамм на третьем рисунке, так как для того, чтобы вырастить такую зверюгу, тяжелому перитониту здоровья не хватит, он от осложнений погибнуть успеет, а сама кишечная палочка ножками ходить не умеет, мы ее исключительно неправильно мытыми ручками разносим, и доказать это элементарно, так как точно такие же штаммы будут высеваться при плановых проверках эпидемиологической службы.
Что делать?
- Для эрадикации такого возбудителя нужен не просто отдельный обученный специалист и имеющая весь набор препаратов резерва аптека, но и напряженная работа эпидемиологической службы, так как подобный пациент должен быть изолирован в отдельную палату, а лучше изолятор (не подумайте, что бред – при правильной организации такие вещи вполне реальны) с проведением карантинных мероприятий, так как основная проблема появления подобного рода возбудителей в том, что они очень быстро разбегаются по всему корпусу (или стационару, если корпуса не изолированы) и обсеменяют все и вся, нанося вред другим ослабленным тяжелой болезнью пациентам и заселяя кишечники всего медицинского персонала.
- И еще одно крайне мерзкое свойство таких возбудителей – они умеют осуществлять горизонтальный перенос механизмов резистентности с другой флорой семейства Enterobacteriaceae, и даже если вы избавились от E.coli, неприятным сюрпризом может стать ее подруга клебсиелла, наносящая еще больший вред и по сути добивающая больного. Избавится полностью от этих возбудителей невозможно, для этого надо избавится от медицинского персонала как основных носителей, но контролировать можно – мероприятия подробно расписаны в действующих СанПиН 2.1.3.2630-10. Так что в случае выявления подобного возбудителя речь пойдет не только о лечении того пациента, у которого он обнаружен, но и проведения мероприятий по недопущению инфицирования всех остальных пациентов (а это, напомню, почти всегда ПИТ или ОРИТ), находящихся рядом.
- И в заключение необходимо упомянуть о панрезистентной E.coli, вооруженной полным спектром механизмов резистентности. В антибиотикограмме будут тотальные R, а МПК возбудителей пробьют все возможные потолки. К счастью для автора, она с таким зверем пока не сталкивалась, что связано с наличием работающей системы эпиднадзора, поэтому картинки не будет, хотя ее несложно представить. Такие пациенты, если кишечная палочка окажется патогеном, а не колонизатором (мало ли с чьих рук, например, в рану упала), к сожалению, почти не выживают, так как изначально являются крайне тяжелыми соматически, а кишечная палочка обычно подводит черту к их существования на бренной земле.
Что делать?
- Не допускать развития такой, не побоюсь этого слова, зверюги в ваших стационарах, а если появилась – гонять эпидемиологическую службу, чтобы избавляла руки и поверхности от такого рода заражения, что возможно только при условии наличия достаточного количества расходных материалов, перчаток и дезинфицирующих средств.
А теперь подведем небольшой итог нашего непростого разговора:
- Кишечная палочка – возбудитель очень серьезный и не следует его недооценивать. В ее типах также необходимо четко ориентироваться.
- В первую очередь о ней мы думаем при лечении инфекций мочевыводящих путей, особенно у беременных.
- Если перед нами пациент с признаками кишечной инфекции, то подход к терапии антибиотиками должен быть сугубо индивидуальным, и если состояние позволяет, то до получения микробиологии – вообще без антибиотиков. Если не позволяет – это должны быть бактериостатики.
- Мы никогда не лечим только анализ, и даже микробиологическое заключение, мы всегда лечим пациента со всем комплексом его симптомов и синдромов. Но микробиология помогает решить как дифференциально-диагностические задачи, что и позволяет отделить безусловный патоген от мирно живущего комменсала.
- Микробиологическая диагностика носит ключевое значение как для подтверждения самого возбудителя, так и для выбора необходимого антибиотика
- В случае выявления резистентных и панрезистентных возбудителей, помимо лечения самого пациента должна в полной мере задействоваться эпидемиологическая служба лечебного учреждения
Резюмируя вышесказанное, и как бы обидно это ни прозвучало, но почти всегда инфекции, вызванные кишечной палочкой, – это «болезни грязных рук» и показатель микробиологического неблагополучия. И одна из серьезных проблем медико-профилактических служб, так как при всем желании они не смогут полностью изъять источник инфицирования, так как он в прямом смысле находится во всех нас, и только соблюдение санитарных правил и санпросвет. работа могут значительно поспособствов