Неонатальная диарея у свиней
Свиноводство – бизнес для многих из нас, мы непосредственно участвуем в нем и, конечно же, наше благополучие напрямую зависит от эффективности работы нашего предприятия в целом.
Что испытывает бизнес, на который постоянно влияют негативные факторы? Естественно, становится менее рентабельным.
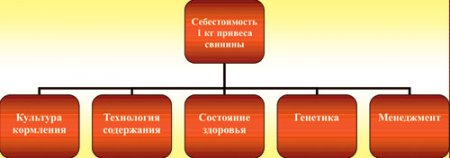
Рис.1 Ключевые моменты для получения максимальной прибыли в свиноводстве.

На рис.1 видно, что факторов, препятствующих максимальной рентабельности, множество. Но самое главное, чтобы каждый из представленных блоков деятельности контролировался, анализировался по своей сути и эффективности, дорабатывался индивидуально, в зависимости от ситуации.
Только после этого, в целом, получится результат.
Если рассмотреть ветеринарную сторону ведения свиноводства и ее участие в получении максимальной рентабельности, то можно выделить несколько основных проблемных этапов:
1. репродуктивные заболевания;
2. синдром ММА;
3. желудочно-кишечные заболевания;
4. респираторные заболевания;
5. кожные заболевания.
Все вышеперечисленные проблемы обязательно будут освещены и описаны в последующем цикле статей. Сегодня хотелось бы начать с анализа желудочно-кишечных заболеваний в свиноводстве.
Весь продуктивный период свиньи можно разделить на физиологические периоды, которые должны совпадать с фактическим нахождением животных в пределах фермы (рис. 2):
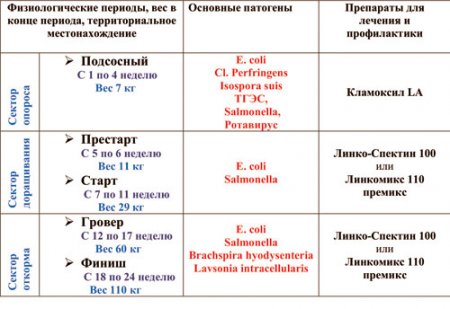
Табл. 1 Бактериальные и вирусные патогены, характерные для определенного возрастного и технологического состояния свиней.
Поросята, которые по причине желудочно-кишечных заболеваний к моменту отъема в 28 дней не успевают достигнуть 7 кг, требуют в дальнейшем дополнительных текущих затрат на корма и содержание, что в свою очередь увеличивает себестоимость 1 кг привеса.
На представленной выше таблице видно, что основными патогенами в подсосный период являются E. Coli и Cl. Perfringens. В большинстве случаев именно эти патогены становятся причиной желудочно-кишечных расстройств поросят.
Эшерихиоз (колибактериоз, колиэнтерит, колисепсис) – остропротекающая инфекционная болезнь поросят, проявляющаяся септицемией, токсемией и энтеритом.
E. coli обладает рядом факторов вирулентности:
• энтеротоксигенность – продукция энтеротоксинов, повреждающих ворсинки кишечного эпителия;
• адгезивность – синтез антигенов, с помощью которых бактерии прикрепляются к эпителиальным клеткам и реализуют свой болезнетворный потенциал;
• токсинообразование – продукция токсинов, которые и являются фактором, нарушающим осмотическое равновесие клеток и вызывающих нарушение водно-электролитного баланса.
Все эти факторы действуют комплексно, создавая инфекционный процесс.
Анаэробная энтеротоксимия свиней (клостридиоз) – остропротекающая токсико-инфекционная болезнь преимущественно новорожденных поросят, характеризующаяся геморрагически-некротическим энтеритом и токсикозом организма. Основным возбудителем анаэробной энтеротоксимии является Cl. Perfringens типа С. Гораздо реже отмечается болезнь, обусловленная типом А и В.
Заболеванию анаэробной энтеротоксимией, так же как и колибактериозом, поросята подвержены преимущественно в первые дни жизни. Болезнь часто может развиваться в первые часы после рождения и быстро получать распространение с охватом 50-80% помета. В таких случаях заболевшие поросята нередко гибнут от дегидратации в течение 1-3 суток.
Лечение вышеописанных заболеваний обычно неперспективно. Ведь даже после эффективной терапии дальнейшая продуктивность поросят падает, потому что антибиотик применяется уже после проявления клинических симптомов заболевания. В некоторых случаях помогает высокая доза per os: ампицилина, тиамулина, валмемулина, линкомицина сразу после рождения поросенка.

Если такие патогены как E. Coli и Cl. Perfringens имеют место на ферме (это подтверждено клинически, лабораторно, патологоанатомически), самой эффективной мерой профилактики данных патогенов будет применение стратегии иммунопрофилактики.
Для улучшения сохранности поросят подсосного периода и увеличения их живой массы при отъеме рекомендуется введение в технологическую схему ветеринарных обработок супоросных свиноматок вакцинации комплексной инактивированной вакциной «Литергард ЛТ-С» («Файзер»).
Препарат содержит в одной дозе пять серотипов E. Coli, Clostridium perfringens типа C и вводится свиноматкам на 75 и 100 день супоросности. Результаты производственных испытаний вакцины «Литергард ЛТ-С» в Украине привели к следующим результатам:
• отход поросят по причине заболевания патогенами E. Coli, Clostridium perfringens уменьшился на 3% (по результатам на отъеме);
• ветеринарные затраты на лечение поросят до отъема уменьшились на 46%;
• средний вес поросенка на отъеме во всех опытных группах был в среднем на 0,7 кг больше.
Таким образом, возникновение неонатальных расстройств ЖКТ самым негативным образом отражается на всем периоде выращивания поросенка и, соответственно, на экономике предприятия в целом.
Из большого набора возбудителей, наиболее характерных для новорожденных поросят, самыми актуальными есть E. Coli, Clostridium perfringens типа С. В этот конкретный период выращивания лечение диареи является не совсем экономически эффективным мероприятием. Стратегически верным есть проведение вакцинации супоросных свиноматок с целью передачи ими напряженного колострального иммунитета поросятам. Одним из самых эффективных способов сделать это в данное время является вакцина «Литергард ЛТ-С» производства компании «Файзер». Препарат вводится супоросным свиноматкам на 70 и 100 день супоросности.
В.В.Эверт, д.в.м., к.в.н.,
А.А. Шептуха, д.в.м.,
Ветеринарный департамент
Представительства компании «Файзер» в Украине
Источник
Пилип Л. В., Бякова О. В.
ФГБОУ ВПО «Вятская государственная сельскохозяйственная академия», г. Киров
Диарейные болезни неинфекционной этиологии распространены повсеместно, развиваются в первые часы жизни животного, сопровождаются тяжелыми токсическими явлениями, характеризуются высоким падежом и наносят большой экономический ущерб [2,3,6].
Около 90% новорожденных животных переболевают желудочно-кишечными болезнями и около половины всех заболеваний свиней, особенно в условиях промышленного свиноводства, составляют болезни желудочно-кишечного тракта. В структуре болезней желудочно-кишечного тракта свиней около 20% приходится на незаразные болезни. У новорожденных поросят наиболее распространена токсическая диспепсия или неонатальная диарея, у более старших возрастных групп наблюдаются катаральные гастриты, гастроэнтериты, гастроэнтероколиты. Изменения в составе фекалий довольно часто бывают первыми признаками начинающегося заболевания, и их исследование может иметь решающее значение в диагностике болезней пищеварительной системы [2,3,4].
В настоящее время проблема широкого распространения желудочно-кишечных заболеваний в свиноводстве не потеряла своей актуальности. По-прежнему желудочно-кишечные заболевания являются огромной проблемой, несмотря на огромное количество препаратов, применяемых в животноводстве [2,3,4,6].
Целью наших исследований явилось изучение функционального состояния желудочно-кишечного тракта больных неонатальной диареей поросят и после применения различных схем лечения.
Для этого у поросят контрольной и опытных групп в начале развития болезни и после клинического выздоровления были отобраны пробы фекалий и проведены копрологические исследования.
Копрологические исследования фекалий проводили в соответствии с пособием по исследованию кала и клинической оценке полученных результатов [1]. При проведении исследований учитывали следующие показатели: форма, цвет, консистенция, скрытая кровь, содержание детрита, жира и жирных кислот, слизи, лейкоцитов, эритроцитов, эпителия, яиц гельминтов, соотношение палочковидных и кокковых форм бактерий. Пробы кала брали после самостоятельной дефекации в чистую сухую тару. В течение 2 часов пробы кала доставлялись для исследований. Для микроскопического исследования готовили влажные препараты в 4 вариантах. Для приготовления нативного препарата готовили равномерную суспензию из воды и кала. В нативном препарате дифференцировали мышечные и соединительные волокна, нейтральный жир, жирные кислоты, лейкоциты, эритроциты, кишечный эпителий, слизь. Показатели учитывали по пятибальной шкале в плюсовых и минусовых единицах. Для нахождения жира и продуктов его расщепления готовили суспензию из кала и реактива Саатгофа. Для просветления и обнаружения яиц глист кал растирали с глицерином. Влажные препараты микроскопировали под малым и большим увеличением (8х10,40х10). Скрытую кровь обнаруживали с помощью бензидиновой пробы: к неразведанному калу добавляли раствор бензидина в ледяной уксусной кислоте и раствор перекиси водорода. Появление окрашивания свидетельствовало о положительной реакции.
В опытной группе № 1 (n = 10) лечение проводили антибиотиком фармазином-50 (тилозин) ежедневно, внутримышечно, в дозе 10 мг/кг в течение 3-4 дней до исчезновения клинических признаков. Препарат из группы макролидов эффективен в отношении большинства грамположительных и некоторых грамотрицательных бактериий, в том числе стафилококков, стрептококков, коринебактерий, клостридий, пастерелл, эризипелотриксов, спирохет, хламидий, трипонемы хлодизентирии и микоплазм. Препарат выводится с калом.
В опытной группе № 2 (n = 10) применяли пробиотик бифитрилак, традиционно используемый для лечения желудочно-кишечных заболеваний. В состав препарата входят: Bifidobacterium bifidum 0,5 х 109/г, Lactobacillus acidophilus 0,5 х 109/г, Bifidobacillus bulgaricus 0,5 х 109/г, Bifidobacillus fermentum 0,5 х 109/г, сорбент KMg3[AlSi3O10] до 1 г. Бифитрилак давали ежедневно, с кормом, групповым методом, в дозе 0,3 г/голову, в течение 5-7 дней до исчезновения клинических признаков.
В опытной группе № 3 (n = 10) применяли пробиотик руменофит ежедневно, индивидуально, per os, в дозе 5,0 мл до исчезновения клинических признаков.
Контрольную группу составили больные животные.
При макроскопическом исследовании определяли консистенцию, форму и цвет кала. У больных животных кал неоформленный, жидкой и мазевидной консистенции, желтого и белого цвета. У животных опытных групп, после применения пробиотиков бифитрилака и руменофита и антибиотика фармазина – 50 кал становится оформленным, плотной и кашицеобразной консистенции, светло-коричневого и серо-коричневого цвета.
При химическом исследовании у 40
Микроскопическая картина дает возможность определить переваривание трех основных элементов корма: белков, жиров и углеводов. О переваривании и усвоении жиров можно судить по количеству нейтрального жира, жирных кислот и мыл; о переваривании углеводов – по присутствию крахмала и клетчатки в кале.
Детрит составляет основной фон при микроскопии нормального кала. Это аморфная масса, состоящая из мелких, зернистых образований. Чем полнее происходит переваривание, тем больше в кале детрита. Детрит учитывается по пятибальной шкале в плюсовых единицах. У больных животных наблюдается следующая закономерность: у 80 % поросят количество детрита оценивалось на «+», у 20 % на «++». Данные показатели говорят о недостаточной переваривающей способности у больных животных вследствие быстрого прохождения каловых масс по желудочно-кишечному тракту. У животных в опытных группах переваривающая способность возрастает. Так, в опытной группе № 1 и № 2 после лечения бифитрилаком и фармазином – 50 количество детрита увеличивается, а наилучшие изменения регистрируются в опытной группе № 3 после лечения руменофитом.
Наличие непереваренной соединительной ткани в кале указывают на недостаточность переваривающей функции желудка.
При нормальном пищеварении кал не содержит нейтрального жира. Остатки жировой пищи выделяются в виде мыл солей высших жирных кислот. Небольшое количество жирных кислот, которое образуется в условиях выключения панкреатического сокоотделения, полностью усваивается кишечником, в кале жирные кислоты не образуются. Ускоренное продвижение химуса приводит к недостаточному усвоению всех пищеварительных продуктов, в том числе жира. У животных опытных групп нормализовалось (после применения руменофита и бифитрилака) и снизилось (после применения фармазина-50) содержание жирных кислот. Таким образом, применение пробиотиков и антибиотика способствовало нормализации деятельности желудочно-кишечного тракта.
Слизь состоит из бесструктурного вещества, в котором заложены различные образования: лейкоциты, клетки эпителия, эритроциты и т.д.
Слизь обнаруживаемая микроскопически, происходит из тех отделов, где каловые массы еще настолько жидки, поэтому при перистальтике она с ними перемешивается. Наличие большого количества слизи является признаком воспалительного процесса слизистой оболочки кишечника.
Единичные клетки кишечного эпителия встречаются в нормальном кале, как следствие физиологического слущения. Большое количество клеток расценивают как признак воспаления слизистой оболочки кишечника. После применения пробиотиков в опытных группах № 1 и № 3 количество эпителия значительно снизилось, а после применения антибиотика в опытной группе № 2 осталось на прежнем уровне.
Единичные лейкоциты могут обнаруживаться в нормальном кале. Увеличение числа лейкоцитов свидетельствует о воспалительном процессе. Количество лейкоцитов нормализовалось и уменьшилось во всех опытных группах. Наиболее существенные изменения происходили в опытной группе № 3, где у 100 % обследуемых животных лейкоциты не обнаруживались.
Эритроциты обнаруживаются в кале при кровотечениях. Данные исследования необходимо подтвердить химическим исследованием, так как если от момента кровотечения до выделения крови проходит значительное время или кровь выделяется из проксимальных отделов толстой кишки, то эритроциты разрушаются.
Яица гельминтов у поросят в опытных и контрольной группах отсутствуют, что исключает диарею по причине паразитарных инфекций.
При микробиологическом исследовании обнаружено, что у больных животных соотношение палочек и кокковой флоры составляет 87 к 13 %. У поросят опытных групп данное соотношение изменяется: на фоне применения антибиотика фармазина – 15 к 85 %, пробиотика бифитрилака 22 к 78 %, пробиотика руменофита 20 к 80 %.Таким образом, явно выраженный дисбаланс соотношения палочек и кокковых форм бактерий в кале у больных животных нормализуется после применения пробиотиков и антибиотика.Результаты микроскопического исследования представлены в таблице
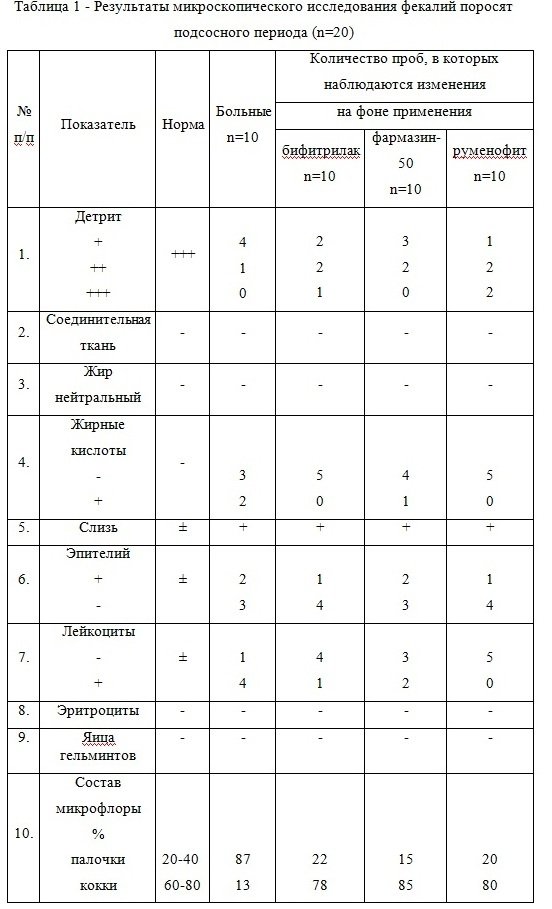
При исследовании кала больных животных выявлены следующие копрологические синдромы: недостаточность переваривания в тонком кишечнике, недостаточность переваривания в толстом кишечнике, недостаточность желчеотделения, воспаление кишечника.
Недостаточность переваривания в тонком кишечнике оценивали по полужидкой консистенции кала, фекалии были неоформленные, желтого цвета.
Недостаточность переваривания в толстом кишечнике проявлялась неоформленной, жидкой, пенистой консистенцией кала, цвет кала был желтый.
Недостаточность желчеотделения, вероятно, была физиологичной для поросят подсосного периода. Она определялась по глинистому, мазевидному, белого цвета калу, в большом количестве обнаруживались жирные кислоты.
Воспаление кишечника подтверждалось наличием большого количества лейкоцитов и эпителия, кроме того, при химическом исследовании обнаружена скрытая кровь.
После проведенного лечения животных в опытных группах отмечена тенденция к снижению и исчезновению проявления описанных синдромов, что особенно выражено в опытной группе № 3.
Таким образом, в результате применения пробиотика руменофита в дозе 5,0 мл больным неонатальной диареей поросятам подсосного периода, повышается переваривающая способность желудочно-кишечного тракта; нормализуется соотношение палочек и кокковых форм бактерий, сдвиг которого отмечается у больных животных; наблюдается тенденция к снижению и исчезновению проявления копрологических синдромов, таких как недостаточность переваривания в тонком кишечнике, недостаточность переваривания в толстом кишечнике, недостаточность желчеотделения, воспаление кишечника.
Источник
Читайте эту статью в:
Здоровье свиней
Лучшим материалом для диагностики неонатальных энтеропатогенов являются живые поросята, которых и следует отправлять для анализа.
Неонатальная диарея – одно из самых частых и распространенных расстройств, наблюдаемое на свиноводческих предприятиях всего мира. Подавляющее большинство случаев такой диареи имеют инфекционную этиологию и напрямую связаны с ненадлежащим выполнением моечных и дезинфекционных процедур в процессе повседневной работы. Общепринятым подходом является максимальное использование производственных площадей, что делает производственный график работы секции опороса чрезвычайно напряженным и в значительной мере сокращает срок сушки и выдержки помытых и продезинфицированных станков. В конечном итоге, все это ведет к тому, что накопившаяся инфекция провоцирует рецидивную диарею, которую пытаются гасить, используя самые современные моющие и/или дезинфицирующие средства. Тем не менее, вплоть до настоящего времени не придумали ничего, что в конечном итоге могло бы сравниться по эффективности с проведенными надлежащим образом мойкой и сушкой. Чаще всего инфекционными агентами, ассоциируемыми с такими ситуациями, являются энтеротоксигенная Escherichia coli (ETEC), ротавирусы А, В и С, Clostridium perfringens типа A and C, Clostridium difficile и Isospora suis. Коронавирусные инфекции, такие как вирусы трансмиссивного гастроэнтерита свиней (ТГСВ), эпизоотической диареи свиней (ЭДСВ) и дельта коронавирус – чрезвычайно патогенны сами по себе и способны вызвать проблемы даже в условиях тщательного выполнения процедур. А уж если мойка проводится недостаточно тщательно, ситуация ухудшается многократно.


Первым шагом в деле успешного диагностирования инфекционной неонатальной диареи является правильный подбор животных. Всегда выбирайте поросенка, у которого клинические симптомы диареи только-только проявились, но у которого еще не развились ни летаргия, ни обезвоживание. Правильный выбор животного в начальной стадии развития болезни может сыграть ключевую роль в том, смогут ли быть выявлены основные вирусные агенты – ротавирусы или коронавирусы. Количество вирусных частиц в энтероцитах у свежеинфицированных животных значительно выше, чем у хронически больных. У поросят, инфекция которых носит хронический характер, истончается слой эпителия верхних покровов кишечных крипт, что затрудняет обнаружение вирусного антигена и/или его РНК.
Лучшим материалом для диагностики неонатальных энтеропатогенов являются живые поросята, которых и следует отправлять для анализа. Поскольку основой диагностики является гистопатология, время, прошедшее с момента наступления смерти и автолиз – главные препятствия, затрудняющие правильную оценку гистологических симптомов и выявление инфекционных агентов, содержащихся в клетках энтеральных тканей. Так, например, через 20-30 минут после наступления смерти, под воздействием автолиза, происходит диффузионное отслоение энтероцитов с кончиков кишечных ворсинок, что делает невозможным диагностику ЕТЕС и I. suis гистологическими методами. Через два часа после наступления смерти автолиз делает всю ткань на участке от кончика кишечных ворсинок до их середины эозинофильной, а клетки – неотличимыми друг от друга. А, поскольку образцы тканей поступают в лабораторию, как правило, на следующий день после их забора, отправка на исследование только «свежих» (т.е., незафиксированных) образцов кишечных тканей значительно бы затруднила правильную гистологическую оценку или даже сделала бы ее невозможной. Таким образом, если в лабораторию для исследований вы не отправляете живых животных, обязательно следует для гистопатологии отбирать образцы кишечных тканей только что умерщвленных поросят. Фрагменты желудочно-кишечного тракта длиной 2-3 см, материал из обеих частей подвздошной кишки, 4-5 фрагментов тонкой кишки, фрагмент слепой кишки, фрагмент проксимального отдела толстой кишки и два фрагмента восходящей ободочной кишки – все это должно быть помещено в пластиковые пакеты или ведра и зафиксировано в формалине (10% раствор). Кроме этого, для гистопатологического исследования следует отобрать мезентериальные лимфоузлы и фрагменты печени. Все эти образцы будут использованы для гистопатологической оценки, а также, в некоторых случаях, для иммуногистохимических исследований (ЭДС, ТГС, ротавирус) или исследований методом цитологической гибридизации (ISH).
Вместе с образцами тканей, зафиксированных в формальнее, очень важно провести забор и отправку в лабораторию свежего материала для проведения бактериологических и вирусологических тестов, а также молекулярно-биологических исследований. Фрагменты подвздошной и тонкой кишки, а также остаток слепой и восходящей ободочной кишки, каждый длиной 10-15 см, следует упаковать в пластиковый пакет. Мезентериальные лимфатические узлы и фрагменты печени, во избежание контаминации, следует также поместить в отдельный пакет.
Эта область не предназначена для консультаций авторов по поводу своих статей, это место для открытых дискуссий между пользователями pig333.ru
Оставьте новый Комментарий
Ограниченный доступ пользователям 333. Чтобы отправить комментарий, Вам необходимо авторизироваться

Источник