Послеоперационное ведение больных острой кишечной непроходимостью

Предоперационная
подготовка
должна быть направлена на коррекцию
дисбаланса воды, улучшение центрального
и периферического кровообращения,
устранение метаболических нарушений.
Центральным звеном предоперационной
подготовки является дозированная по
объему и качественному составу
инфузионная терапия с одновременным
нейровегетативным торможением.
В
среднем подготовка к операции занимает
2—3 ч и зависит от тяжести и продолжительности
заболевания. Устанавливают катетер в
полую вену, катетер в мочевой пузырь и,
по возможности, желудочный зонд. При
шоке инфузии начинают с гетерогенных
объемозамещающих растворов типа
лекстрана-60 или диоксиэтилкрахмала.
Наряду с этими растворами рекомендуется
введение низкомолекулярных декстранов
или растворов крахмала с мол. массой
200 000. Общая доза декстранов не должна
быть больше 1,5 г/кг массы тела. После
восстановления нормальных или близких
к нормальным показателей АД, частоты
пульса, улучшения показателей ЦВД
переливают изотонические растворы,
содержащие натрий и хлор. При дефиците
белка, который нередко возникает при
опухолевой непроходимости, применяют
альбумин, протеин или плазму для
выравнивания КОД. Иногда требуются
трансфузии крови, если уровень гематокрита
исходно был снижен до 0,25 и более. Общая
доза инфузионных растворов за первые
24 ч должна составлять 2,4—3,0 л/м2
поверхности тела. Скорость введения
определяют по клинической симптоматике,
параметрам гемодинамики.
При олигурии
и тем более при анурии, на фоне
продолжающейся инфузионной терапии
целесообразно использование стимуляторов
диуреза, причем при сниженном ОЦК
предпочтение следует отдавать маннитолу.
В
острой стадии дегидратации, олигурии
или анурии, несмотря на выявленный
дефицит калия, не следует применять
растворы с калием. Калий обычно назначают
в послеоперационном периоде, когда
восстановлены показатели гемодинамики,
в основном ликвидирован дефицит жидкости
и нормализована функция почек.
Умеренные изменения КОС обычно требуют
специальной коррекции, они, как правило,
связаны с электролитным дисбалансом,
и лечение заключается в восстановлении
гидроионного равновесия.
Нередко
в ходе предоперационной подготовки
возникает необходимость регулировать
темп введения жидкости, применять
кардиотонические, антиаритмические
средства или использовать гормональные
препараты (преднизолон, гидрокортизон)
для стабилизации гемодинамики на уровне,
допускающем возможность начала
операции.
^В
послеоперационном периоде
проводят поддерживающую инфузионную
терапию в соответствии с потерями
жидкости и выявленными дефицитами. Для
возмещения гидроионных дефицитов
применяют раствор Рингера, лактасол,
поляризующие коктейли, содержащие
глюкозу, инсулин и калий. Объем плазмы
восполняют путем введения желатиноля,
альбумина, плазмы и других сред, избегая
при этом избыточной инфузионной терапии.
Назначают реополиглюкин и другие
средства с целью профилактики
тромбообразования и восстановления
микроциркуляции. К инфузионным средам
добавляют растворы, содержащие
магний, кальций, витамины (аскорбиновая
кислота, тиамин, пиридоксин). Калий
вводится только при достаточной функции
почек. Важнейшим методом профилактики
и лечения послеоперационной атонии
кишечника является восстановление
водного и электролитного баланса,
важнейшее звено которого — ликвидация
дефицита калия. Для обеспечения
достаточной перистальтики применяют
прозерин. Усиление перистальтики
можно достичь путем улучшения
мезентериального кровообращения с
помощью гиперосмолярно-гиперонкотических
растворов. Полное восстановление
жидкостных дефицитов при неосложненном
течении послеоперационного периода
происходит на 3—4-е сутки.
БИЛЕТ
6
Соседние файлы в предмете Факультетская хирургия
- #
- #
- #
- #
03.10.20171.98 Mб136Острый холецистит.pptx
- #
Источник
Комментарии
26 ноября 2007 г. Министерством здравоохранения утверждены протоколы диагностики и лечения острой кишечной непроходимости.
Острая кишечная непроходимость (ОКН) МКБ-10-К56 – синдромная категория, объединяющая осложненное течение различных по этиологии заболеваний и патологических процессов, которые формируют морфологический субстрат ОКН.
В зависимости от природы пускового механизма ОКН подразделяется на механическую и динамическую, в абсолютном большинстве – паралитическую, развивающуюся на основе пареза кишечника. Спастическая непроходимость может возникнуть при органических спинальных нарушениях.
Если острое нарушение кишечной гемоциркуляции захватывает внеорганные брыжеечные сосуды, возникает странгуляционная ОКН основными формами которой являются ущемления, завороты и узлообразования. Значительно медленнее, но с вовлечением всего приводящего отдела кишечника процесс развивается при обтурационной ОКН, особенно это касается опухолевой толстокишечной ОКН, когда просвет кишки перекрывается опухолью или иным объемным образованием. Промежуточное положение занимают смешанные формы ОКН – инвагинации и спаечная непроходимость – сочетающие странгуляционные и обтурационные компоненты. Спаечная непроходимость составляет до 70-80% всех форм ОКН.
Характер и выраженность клинических проявлений зависят от уровня ОКН. Различают тонкокишечную и толстокишечную ОКН, а в тонкокишечной – высокую и низкую.
При всех формах ОКН тяжесть расстройств имеет прямую зависимость от фактора времени, что определяет неотложный характер лечебно-диагностических мероприятий.
Диагноз или обоснованное предположение о наличии ОКН являются основанием для немедленного направления больного в хирургический стационар машиной скорой помощи в положении лежа на носилках.
ПРОТОКОЛЫ ДИАГНОСТИКИ ОКН В ОТДЕЛЕНИИ ЭКТРЕННОЙ МЕДИЦИНСКОЙ ПОМОЩИ (В ПРИЕМНОМ ОТДЕЛЕНИИ)
Всех больных, поступающих с диагнозом ОКН, делят на две группы:
– быстрое, внезапное, даже бурное начало заболевания на фоне полного благополучия;
– схваткообразные боли в животе;
– задержка стула и газов;
– неукротимая рвота;
– наличие рубцов на передней брюшной стенке;
– рентгенологические признаки (горизонтальные уровни жидкости). 1.2 Протоколы обследования в ОЭМП: 1. Главной задачей дифференциальной диагностики при наличии признаков ОКН является выделение больных со странгуляционными формами механической непроходимости, которым показано неотложное хирургическое лечение и эта категория больных после выполнения ЭКГ, консультации терапевта направляется в операционную.
2. Целенаправленно обследуются места типичного расположения грыж брюшной стенки. Обязательным является пальцевое ректальное исследование.
3. Оценивается степень обезвоживания – тургор кожи, сухость языка, наличие жажды, фиксируется интенсивность рвоты, ее частота, объем и характер рвотных масс.
4. Производится термометрия.
5. Лабораторные исследования: клинический анализ крови, общий анализ мочи, сахар крови, группа крови, резус-фактор, RW, коагулограмма, КЩС, ACT, АЛТ, ЩФ, креатинин, мочевина, средние молекулы, хемолюминисценция, глютатиопироксидаза и супероксиддисмутаза.
6. Инструментальные исследования: обзорная рентгенография брюшной полости, обзорная рентгенография груди, УЗИ органов брюшной полости, ЭКГ. ПРОТОКОЛЫ ЛЕЧЕБНО-ДИАГНОСТИЧЕСКОЙ ТАКТИКИ В ХИРУРГИЧЕСКОМ ОТДЕЛЕНИИ 1. Установленный диагноз странгуляционной ОКН служит показанием к неотложной операции после краткой предоперационной подготовки в сроки не более 2 часов после поступления больного.
2. Обязательными компонентами предоперационной подготовки наряду с гигиенической подготовкой кожи в области операционного поля являются:
– опорожнение и декомпрессия верхних отделов желудочно-кишечного тракта через желудочный зонд, который сохраняется на период вводного наркоза в операционной для предотвращения регургитации;
– опорожнение мочевого пузыря;
– превентивное парентеральное введение антибиотиков (целесообразно использование аминогликозидов II-Ш, цефалоспоринов III поколения и метронидозол 100 мл за 30-40 минут до начала операции.
3. Наличие выраженных клинических признаков общего обезвоживания и эндотоксикоза служит показанием для интенсивной предоперационной подготовки с постановкой катетера в магистральную вену и проведением инфузионной терапии (внутривенно 1,5 литра растворов кристаллоидов, реамберин 400 мл, цитофлавин 10 мл в разведении на 400 мл 5% раствора глюкозы. Антибиотики в этом случае вводятся за 30 минут до операции внутривенно.
4. При сомнениях в диагностике ОКН, а также если синдром ОКН развивается на фоне длительного существования спаечной болезни и предшествовавших по этому поводу неоднократных операций, показано сочетанное проведение:
– дифференциальной диагностики;
– консервативных лечебных мероприятий по устранению ОКН (до окончательного решения вопроса об операции);
– общесоматической инфузионной терапии, которая служит одновременно и подготовкой к возможной операции.
5. Консервативные мероприятия по устранению ОКН включают: – двухстороннюю сакроспинальную блокаду на уровне Th5 – Th7: – постоянную декомпрессию верхних отделов пищеварительного тракта через назогастральный зонд или интестинальный зонд, заведенный при помощи ФГДС; – интенсивную инфузионную терапию с введением спазмолитических или стимулирующих кишечную моторику препаратов (по показаниям); – проведение сифонных клизм.
6. Показаниями к проведению исследований с приемом контраста при непроходимости служат спаечная ОКН у больных, неоднократно подвергшихся оперативным вмешательствам, без явлений перитонита. Основанием для прекращения серии Rg-грамм является фиксация поступления контраста в толстую кишку.
7. При опухолевой толстокишечной непроходимости лечение начинается с консервативных мероприятий, цель которых – устранение острой непроходимости и создание условий для выполнения радикальной операции. К перечисленным выше консервативным мероприятиям добавляется лечебно-диагностическая эндоскопия (неотложные ректороманоскопия, фиброколоноскопия).
При отсутствии эффекта в течение 12 часов от поступления в стационар выполняется срочная операция. Рентгеноконтрастное исследование с дачей бариевой взвеси не показано. ПРОТОКОЛЫ ХИРУРГИЧЕСКОЙ ТАКТИКИ ПРИ ОСТРОЙ КИШЕЧНОЙ НЕПРОХОДИМОСТИ 1. Операция по поводу ОКН всегда выполняется под наркозом трехврачебной бригадой.
2. На этапе лапаротомии, ревизии, идентификации патоморфологического субстрата непроходимости и определения плана операции обязательно участие в операции самого опытного хирурга дежурной бригады, как правило – ответственного дежурного хирурга.
3. При любой локализации непроходимости доступ – срединная лапаротомия, при необходимости – с иссечением рубцов и осторожным рассечением спаек при входе в брюшную полость.
4. Операции по поводу ОКН предусматривают последовательное решение следующих задач:
– установление причины и уровня непроходимости;
– устранение морфологического субстрата ОКН;
– определение жизнеспособности кишки в зоне препятствия и определение показаний к ее резекции;
– установление границ резекции измененной кишки и ее выполнение;
– определение показаний и способа дренирования кишки;
– санация и дренирование брюшной полости при наличии перитонита.
5. Обнаружение зоны непроходимости непосредственно после лапаротомии не освобождает от необходимости систематической ревизии состояния тонкой и толстой кишок на всем их протяжении. Ревизии предшествует обязательная инфильтрация корня брыжейки тонкой кишки раствором местного анестетика (100-150 мл 0,25% раствора новокаина). В случае выраженного переполнения кишечных петель содержимым перед ревизией производится декомпрессия кишки с помощью гастроинтестинального зонда.
6. Устранение непроходимости представляет собой ключевой и наиболее сложный компонент вмешательства. Оно осуществляется наименее травматичным способом с четким определением конкретных показаний к использованию различных методов: рассечения спаек; резекции измененной кишки; устранения заворотов, инвагинаций, узлообразований или резекции этих образований без предварительных манипуляций на измененной кишке.
7. При определении показаний к резекции кишки используются визуальные признаки (цвет, отечность стенки, субсерозные кровоизлияния, перистальтика, пульсация и кровенаполнение пристеночных сосудов), а также динамика этих признаков после введения в брыжейку кишки теплого раствора) местного анестетика. При сомнениях в жизнеспособности кишки, особенно на большом ее протяжении допустимо отложить решение вопроса о резекции, используя запрограммированную релапаротомию или лапароскопию через 12 часов.
8. При решении вопроса о границах резекции следует отступать от видимых границ нарушения кровоснабжения кишечной стенки в сторону приводящего отдела на 35-40 см, и в сторону отводящего отдела 20-25 см. Исключение составляют резекции вблизи связки Трейца или илеоцекального угла, где допускается ограничение указанных требований при благоприятных визуальных характеристиках кишки в зоне предполагаемого пересечения. При этом обязательно используются контрольные показатели кровотечение из сосудов стенки при ее пересечении и состояния слизистой области. Возможно, также, использование трансиллюминации, ЛАКК или других объективных методов оценки кровоснабжения.
9. Показаниями к дренированию тонкой кишки служат:
– переполнение содержимым приводящих кишечных петель;
– наличие разлитого перитонита с мутным выпотом и наложениями фибрина;
– обширный спаечный процесс в брюшной полости.
10. При колоректальной опухолевой непроходимости и отсутствии признаков неоперабельности выполняются одно – или двухэтапные операции в зависимости от локализации, стадии опухолевого процесса и выраженности проявлений толстокишечной непроходимости. Выполнение неотложной правосторонней гемиколэктомии в отсутствии перитонита допустимо завершать наложением первичного илеотрансверзоанастомоза. В случае непроходимости с левосторонним расположением очага обструкции выполняется резекция ободочной кишки с удалением опухоли, которая завершается по типу операции Гартмана. Первичный анастомоз не накладывается.
11. Все операции на ободочной кишке завершаются девульсией наружного сфинктера заднего прохода.
12. Наличие разлитого перитонита требует дополнительной санации и дренирования брюшной полости в соответствии с принципами лечения острого перитонита. ПРОТОКОЛЫ ВЕДЕНИЯ ПОСЛЕОПЕРАЦИОННОГО ПЕРИОДА Энтеральное питание начинается с появлением кишечной перистальтики посредством введения в интестинальный зонд глюкозо-электролитных смесей.
Извлечение назогастроинтестинального дренирующего зонда осуществляется после восстановления устойчивой перистальтики и самостоятельного стула на 3-4 сутки. Дренирующая трубка, установленная в тонкую кишку через гастростому или ретроградно по Велчу-Житнюку, удаляется несколько позже – на 4 – 6 сутки. Зонд, введенный в кишку с каркасной целью при спаечной ОКН, удаляется на 7-8 сутки.
С целью борьбы с ишемическими и реперфузионными повреждениями тонкой кишки и печени проводится инфузионная терапия (внутривенно 2-2,5 литра растворов криталлоидов, реамберин 400 мл, цитофлавин 10,0 мл в разведении на 400 мл 0,9% раствора хлорида натрия, трентал 5,0 – 3 раза в сутки, контрикал – 50000 ед/сутки, эссенциале 10,0, аскорбиновая кислота 5% 10 мл/сутки).
Антибактериальная терапия в послеоперационном периоде должна включать либо аминогликозиды II-III, цефалоспорины III поколения и метронидозол, либо фторхинолоны II поколения и метронидозол.
Для профилактики образования острых язв ЖКТ терапия должна включать антисекреторные препараты.
Комплексная терапия должна включать гепарин либо низкомолекулярные гепарины для профилактики тромбоэмболических осложнений и нарушений микроциркуляции.
Лабораторные исследования выполняются по показаниям и перед выпиской.
Выписка при неосложненном течении послеоперационного периода производится на 10-12 сутки. Наличие функционирующего искусственного кишечного или желудочного свища при отсутствии других осложнений допускает выписку больного на амбулаторное лечение с рекомендацией повторной госпитализации для ликвидации свища в случае, если не произойдет самостоятельного его закрытия.
В случае необходимости проведения адъювантной химиотерапии и при отсутствии противопоказаний к ней у больных с опухолевой причиной ОКН, проводить ее следует не позднее 4 недель после операции.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Ба М.Р.
2
Негребов М.Г.
1, 2
Александров Л.В.
1, 2
1 Городская клиническая больница № 67 им. Л.А. Ворохобова Департамента здравоохранения г. Москвы
2 ГБОУ ВПО Первый Московский государственный медицинский университет им. И.М. Сеченова Минздрава России
Цель исследования: разработать и патогенетически обосновать оптимальную тактику ведения больных с острой тонкокишечной механической непроходимостью (ОТМН) в послеоперационном периоде. Материал и методы: проанализированы результаты лечения 68 (100%) больных с ОТМН, которым выполнена резекция нежизнеспособного участка кишки в зависимости от степени кишечной непроходимости. Выделены основная (I) группа – 40 (58,8%) больных, которым проводили отмывание тонкой кишки и энтеральное зондовое питание (ЭЗП) в раннем послеоперационном периоде, и контрольная (II) группа — 28 (41,2%) больных, которым динамическую кишечную непроходимость (ДКН) разрешали традиционными способами и осуществляли полное парентеральное питание до разрешения ДКН. Результаты: Сроки разрешения ДКН в I и II группах 30±9,8 и 46,3±13,85 ч соответственно; p
тонкая кишка
странгуляционная кишечная непроходимость
спаечная кишечная непроходимость
ущемлённая грыжа
заворот тонкой кишки
резекция кишки
синдром кишечной недостаточности
энтеральное питание
нутритивная поддержка
1. Ачкасов Е.Е., Пугаев А.В., Мельников П.В., Алекперов С.Ф., Александров Л.В, Посудневский В.И., Волков В.С., Ба М.Р. Инвагинационная тонкокишечная непроходимость, обусловленная метастазами меланомы в тонкой кишке // Хирургия. Журнал им. Н.И. Пирогова. 2013. № 1. С. 83–87.
2. Ба М.Р., Негребов М.Г., Ачкасов Е.Е., Александров Л.В., Андрейчиков А.А. Морфологические изменения тонкой кишки при острой тонкокишечной механической непроходимости. // Материалы конференции молодых ученых «Актуальные аспекты диагностики и лечения в абдоминальной хирургии», г. Москва, 26 июня 2014 г. С. 14–16.
3. Негребов М.Г., Ачкасов Е.Е., Александров Л.В., Ба М.Р. Эволюция подходов к классификационным критериям острой кишечной непроходимости // Хирургическая практика. 2013. № 1. С. 24–29.
4. Попова Т.С., Тамазашвили Т.Ш., Шестопалов А.Е. Синдром кишечной недостаточности в хирургии. М., 1991. 240 с.
5. Пугаев А.В., Ачкасов Е.Е. Обтурационная опухолевая толстокишечная непроходимость. М.: Профиль-2С, 2005. 224 с.
6. Сапин М.Р., Милюков В.Е., Антипов Е.Ю. Патогенетическое обоснование лечебной тактики при острой тонкокишечной непроходимости // Вестник хирургической гастроэнтерологии. 2008. № 1. С. 42–51.
7. Сапин М.Р., Николенко В.Н., Никитюк Д.Б., Чава С.В. Вопросы классификационных закономерностей морфогенеза желез стенок полых внутренних органов // Сеченовский вестник. 2012. № 4. С. 62–71.
8. Юдин А.Б., Демко А.Е., Чуприс В.Г. Ранняя энтеральная терапия у больных, оперированных по поводу спаечной тонкокишечной непроходимости // Военно-медицинский журнал. 2008. № 6. С. 60–61.
9. Bologna Guidelines for Diagnosis and Management of Adhesive Small Bowel Obstruction (ASBO): 2010 Evidence-Based Guidelines of the World Society of Emergency Surgery, World J Emerg Surg. 2011; 6: 5. Published online 2011 January 21. doi: 10.1186/1749-7922-6-5PMCID: PMC3037327
10. Gavin G. Lavery, Paul Glover The metabolic and nutritional response to critical illness // Current opinion in critical care. 2000. № 3. P. 145–148.
Острая тонкокишечная механической непроходимость (ОТМН) — одна из наиболее актуальных проблем среди экстренных хирургических заболеваний. Многообразие этиологических факторов, сложность патогенеза, трудности диагностики отражаются на результатах лечения [1, 3, 6, 7, 8]. Послеоперационная летальность при ОТМН составляет от 6,5 до 9,4%, что определяет научно-практическую значимость изучаемой проблемы [8, 9]. В результате анализа неблагоприятных исходов при хирургическом лечении больных с ОТМН сделаны выводы, что у наибольшего количества умерших в ранние сроки после операции имелись глубокие нарушения обмена, одной из причин которых является синдром энтеральной недостаточности [4, 8].
У больных в послеоперационном периоде происходит мощный выброс стрессовых гормонов – катехоламинов, глюкагона, обладающих выраженным катаболическим действием. Энергетические затраты увеличиваются до 50–150%, что определяет необходимость ранней энтеральной нутритивной поддержки в послеоперационном периоде [10].
Функциональные и морфологические изменения в стенке тонкой кишки на различных этапах развития ОТМН определяют важнейшие осложнения этого тяжелого заболевания и смертельные исходы [4]. Проведено много экспериментальных работ на животных, свидетельствующих о важности микроциркуляции в стенке тонкой кишки для улучшения результатов лечения ОТМН [6]. Многие авторы считают, что микроциркуляторные нарушения наступают раньше клинических и исчезают позже последних [4, 6, 8]. Для улучшения результатов лечения ОТМН существенное значение имеют проведение патогенетической терапии и скорейшее восстановление функции тонкой кишки.
Цель исследования – разработать и патогенетически обосновать оптимальную тактику послеоперационного лечения больных с ОТМН.
Материалы и методы. Клиническое исследование выполнено на 68 (100%) больных с ОТМН, осложненной некрозом кишки, на базе ГКБ № 67 им. Л.А. Ворохобова ДЗ г. Москвы в период 2009–2014 гг. Были обследованы 34 (50%) женщины и 34 (50%) мужчины. Всем больным была выполнена резекция нежизнеспособного участка тонкой кишки. Объем резекции кишки зависел от степени ОТМН на основании ранее проведенных исследований [2], при которых было установлено, что для компенсированной ОТМН оптимальным объемом резекции является 10 см в проксимальном направлении от макроскопических границ некроза и 5 см — в дистальном направлении, при субкомпенсированной ОТМН — 15 см в проксимальном направлении от макроскопических границ некроза и 10 см в дистальном. В условиях декомпенсированной ОТМН объем резекции следует увеличивать до 30 см в проксимальном направлении от макроскопических границ некроза и 15 см — в дистальном. Время с момента начала заболевания до поступления в стационар составило 4,98±3,63 ч. Наиболее частой причиной ОТМН были спайки брюшной полости – 42 (61,8%), на втором месте — ущемление грыж – 24 (35,3%), реже заворот тонкой кишки – 2 (2,9%) пациента. Сопутствующие хронические заболевания были выявлены у 46 (67,6%) пациентов (сердечно-сосудистые заболевания, болезни легких, сахарный диабет 2-го типа, хронический пиелонефрит, мочекаменная болезнь, полинейропатия).
Выделяли 3 степени компенсации кишечной непроходимости (КН): компенсированная, субкомпенсированная, декомпенсированная [5]. Степень КН определяли на основании клинической картины, обзорной рентгенографии брюшной полости в положении стоя, ультразвукового исследования (УЗИ) брюшной полости. Компенсированной считали такую КН, при которой на обзорной рентгенограмме брюшной полости выявляли пневматизацию с единичными уровнями жидкости в тонкой кишке; при УЗИ брюшной полости обнаруживали дилятацию тонкой кишки, в просвете — газ и незначительное количество жидкости, при этом толщина стенки не превышала 4 мм, а моторно-эвакуаторная функция была снижена, но сохранена. К субкомпенсированной относили КН, при которой обнаруживали множественные уровни жидкости с газом в тонкой кишке и складками Керкринга, что отражает отек стенки кишки. Данные рентгеносемиотики подтверждали УЗИ брюшной полости, при котором выявляли не только расширение просвета с жидкостным содержимым, но и отек стенки тонкой кишки (толщина стенки до 7 мм) с двойным контуром и сохраненной моторной функцией кишки в виде маятникообразных движений. Критериями декомпенсированной КН являлись множественные тонкокишечные уровни с локализацией арок во всех отделах брюшной полости; при УЗИ — резкая дилятация тонкой кишки, жидкость и газ во всех проксимальных отделах тонкой кишки, толщина ее стенки >7 мм, моторно-эвакуаторная функция отсутствует.
Операцию выполняли в первый час от поступления после предварительной подготовки – коррекции гемодинамических и водно-электролитных нарушений. Всем пациентам выполнены лапаротомия, интраоперационная декомпрессия кишечника при субкомпенсированной и декомпенсированной ОТМН с помощью зонда Эббота—Мюллера, резекция нежизнеспособного участка тонкой кишки с формированием анастомоза бок в бок двухрядным швом, санация и дренирование брюшной полости.
Для сравнения методов разрешения динамической кишечной непроходимости (ДКН) выделили две группы: основную (I) – 40 (58,8%) больных и контрольную (II) – 28 (41,2%) больных. В I группе после декомпрессии тонкой кишки и устранения ОТСН устанавливали интраоперационно-назоинтестинальный зонд (НИЗ) в тощую кишку для разрешения ДКН и проведения раннего энтерального зондового питания (ЭЗП) в послеоперационном периоде. В 1-е сутки после операции в НИЗ со скоростью 100–150 мл/мин вводили охлажденный до 14–16оС 0,9%-ный раствор NaCl в объеме 1200–1500 мл, что способствовало разрешению ДКН. Критериями разрешения ДКН и восстановления функции кишечника являлись: сокращение объема отделяемого по назогастральному зонду, положительная проба на капельное введение 300 мл подогретого до 35–37⁰С физиологического раствора в тощую кишку под контролем УЗИ, жидкий стул. После устранения ДКН проводили раннее ЭЗП сбалансированными энтеральными смесями с последующим переводом на сипинг и оральное питание.
Во II группе для коррекции водно-электролитных нарушений и белково-энергетической недостаточности до разрешения ДКН проводили полное парентеральное питание, в дальнейшем разрешали пить и переводили на оральное питание.
Статистический анализ полученных результатов проводили с применением статистического пакета StatisticaforWindows v. 7.0, StatSoftInc. При сравнении групп по качественным признакам применяли односторонний точный критерий Фишера. При сравнении по количественным признакам независимых групп применяли критерий Манна—Уитни, по количественным признакам зависимых групп – критерий Вилкоксона. Статистически значимыми считались различия при р<0,05.
Результаты исследования. Выявили, что в I группе было 18 (45%) пациентов с компенсированной, 16 (40%) — с субкомпенсированной и 6 (15%) — с декомпенсированной ОТМН, во II группе было 12 (42,9%) пациентов с компенсированной, 11 (39,2%) — с субкомпенсированной и 5 (17,9%) — с декомпенсированной ОТМН. Провели сравнительный анализ результатов лечения двух групп. При анализе трофического статуса (ТС) на протяжении всего послеоперационного периода выявлено, что к 10-м суткам после операции в I группе отмечается тенденция к повышению сывороточного альбумина, трансферрина и лимфоцитов. Во II группе увеличения этих показателей отмечено не было. В результате проведенного анализа изменений ТС у пациентов с ОТМН видно, что использование раннего отмывания тонкой кишки и коррекция белково-энергетической недостаточности ЭЗП позволяет поддержать и стабилизировать ТС в раннем послеоперационном периоде и препятствовать развитию системной воспалительной реакции (рис. 1–5).
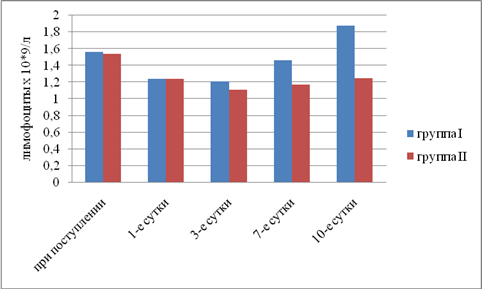
Рис. 1. Динамика изменений абсолютного числа лимфоцитов (р<0,05)
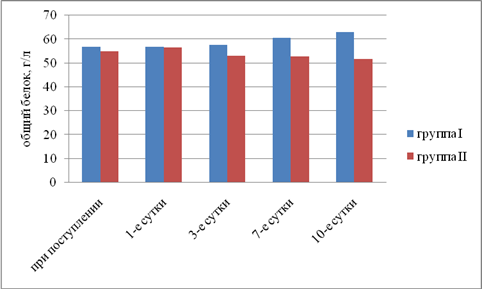
Рис. 2. Динамика изменений общего белка плазмы (р<0,05)
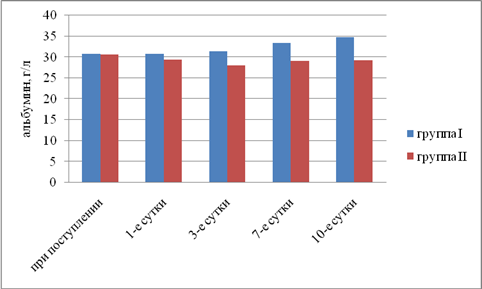
Рис. 3. Динамика изменений сывороточного альбумина (р<0,05)
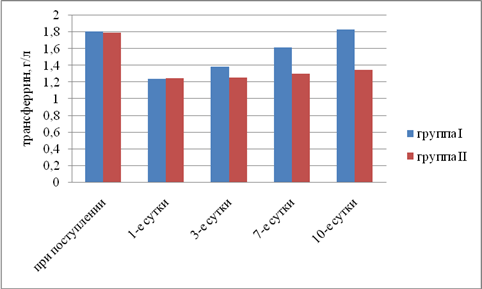
Рис. 4. Динамика изменений трансферрина (р<0,05)
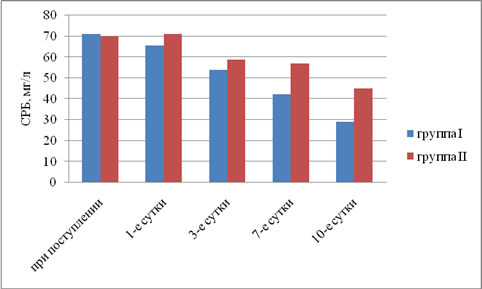
Рис. 5. Динамика изменений С-реактивного белка (р<0,05)
При сравнительном анализе результатов лечения обеих подгрупп выявлено, что во II группе, где отмывание тонкой кишки и раннее ЭЗП не применяли, выше уровень послеоперационных осложнений, больше сроки разрешения ДКН, выше уровень летальности и больше сроки госпитализации (табл. 1).
Таблица 1
Данные о результатах лечения в I и II группах
Показатель | группа I | группа II | Достоверность |
Послеоперационные осложнения | 2 (5,00%) | 9 (32,14%) | р=0,004* |
Сроки разрешения ДКН, ч | 30±9,8 | 46,3±13,85 | p<0,001** |
Сроки госпитализации, сутки | 11,2±1,73 | 14,63±2,24 | р=0,004** |
Летальность | 0 (0%) | 2 (7,14%) | р=0,166* |
Прим.: * Односторонний критерий Фишера; ** Критерий Манна—Уитни
Большую часть осложнений у пациентов II группы составляли гнойно-септические осложнения, что объясняли отсутствием адекватной коррекции белково-энергетической недостаточности в раннем послеоперационном периоде на фоне сопутствующих заболеваний. Выраженные метаболические нарушения, пожилой и старческий возраст, тяжелая хирургическая травма с выраженной катаболической реакцией, длительные сроки госпитализации явились основными причинами развития осложнений.
Заключение. Наиболее оптимальным методом разрешения ДКН в раннем послеоперационном периоде является интраоперационная декомпрессия тонкой кишки с аспирацией кишечного содержимого с последующей установкой назоинтестинального зонда для раннего отмывания тонкой кишки охлажденным до 14–16оС 0,9%-ным раствором NaCl. Отмывание тонкой кишки позволяет сократить объемы инфузионной терапии.
В условиях послеоперационной травмы организма именно кишечник становится основным источником инфекции и источником неконтролируемой транслокации микробов и их токсинов в кровь, что лежит в основе формирующейся системной воспалительной реакции и развивающейся на этом фоне полиорганной недостаточности. В связи с этим назначение больным с ОТМН ЭЗП позволяет минимизировать последствия агрессивного воздействия различных факторов на желудочно-кишечный тракт и сохранять его структурную целостность и полифункциональную активность, что является необходимым условием для более быстрого выздоровления пациента.
Раннее энтеральное питание позволяет предотвратить прогрессирование белково-энергетической недостаточности, снижает частоту послеоперационных осложнений, летальность и длительность пребывания пациентов в стационаре.
Рецензент:
Алекперов С.Ф., д.м.н., заведующий 2-м хирургическим отделением ГКБ № 67 им. Л.А. Ворохобова ДЗ, г. Москва;
Черепанин А.И., д.м.н., заместитель главного врача по хирургии Клинической больницы № 1 МЕДСИ в Отрадном, профессор кафедры госпитальной хирургии № 1 лечебного факультета Первого МГМУ им. И.М. Сеченова, г. Москва.
Библиографическая ссылка
Негребов М.Г., Александров Л.В., Ба М.Р., Негребов М.Г., Александров Л.В. ТАКТИКА ВЕДЕНИЯ ПОСЛЕОПЕРАЦИОННОГО ПЕРИОДА ПРИ ОСТРОЙ ТОНКОКИШЕЧНОЙ МЕХАНИЧЕСКОЙ НЕПРОХОДИМОСТИ // Современные проблемы науки и образования. – 2015. – № 3.;
URL: https://science-education.ru/ru/article/view?id=19679 (дата обращения: 02.11.2020).

Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник