Сепсис вызванный кишечной палочкой
 Автор: Трубачева Е.С., врач – клинический фармаколог
Автор: Трубачева Е.С., врач – клинический фармаколог
Этой статьей мы начинаем рассмотрение представителей микробиологического мира, с которыми чаще всего встречаем в ежедневной клинической практике, и темой сегодняшнего разговора будет кишечная палочка, она же Escherichia coli (E.coli).
Актуальность обсуждения данного микроорганизма состоит в том, что кишечная палочка – это чемпион по созданию проблем как для пациентов, так и для медицинского персонала стационаров и в амбулаторной службе. Хуже нее только клебсиелла, но о ней поговорим попозже. При этом E.coli не летает по воздуху и не имеет ножек для самостоятельного перемещения и инфицирование ею – это почти всегда «болезнь грязных рук». С патологией, вызванной этим возбудителем, пациент может прийти к любому врачу, а медицинский персонал может принести уже на своих руках кишечную палочку любому пациенту с одной лишь разницей – это будет не дикий и симпатичный зверек, убиваемый обычным амоксицилином, а вооруженная до зубов особь, умеющая очень эффективно убивать сама. То есть это один из тех врагов, которых совершенно точно надо знать в лицо.
Микробиологические аспекты
E.coli относится к типичным представителям семейства Enterobacteriaceae, являясь грамотрицательной бактерией, факультативным анаэробом в составе нормальной кишечной микрофлоры человека. Но тут же становится патогеном, выбравшись из среды нормального обитания, хотя отдельные штаммы являются патогенными и для желудочно-кишечного тракта. То есть кишечная палочка относится к кишечным комменсалам, кишечным патогенам и внекишечным патогенам, каждый из которых мы кратко разберем.
К штаммам E.coli, действующим как кишечные патогены и встречающимся чаще других, относятся:
- Штамм серотипа O157:H7 (STEC O157) или так называемый энтерогеморрагический штамм E.coli, который является причиной 90% случаев геморрагических колитов и 10% случаев гемолитико-уремического синдрома. Встречается достаточно часто, а если вы работаете в стационарах плановой помощи, то это один из обязательных анализов для принятия решения о госпитализации, так что так или иначе он на слуху. Проблема инфицирования этим возбудителем связана с употреблением плохо термически обработанной пищи и передачи штамма контактным путем от человека к человеку, проще говоря, через руки.
- Второй крайне опасный высоко-патогенный штамм кишечной палочки – O104:H4, вызвавший в Германии 2011 году эпидемию с высоким уровнем смертности среди пациентов с пищевыми токсико-инфекциями вследствие развития гемолитико-уремического синдрома. Если помните, это была очень громкая история с перекрытиями границ для испанских огурцов, потом вообще для всей плодоовощной продукции из Европы в Россию, пока искали хотя бы источник, не говоря уж о виновнике тех событий. Окончательно виновными тогда были обозначены листья салата, в поливе которых использовалась вода с признаками фекального заражения, а затем речь пошла уже о пророщенных семенах, которые так же полили фекально-зараженной водичкой. Так вышли на конкретный штамм E.coli – O104:H4, который, подвергшись санации антибиотиком, выплескивает эндотоксин, вызывающий гемолиз и острую почечную недостаточность. В итоге – массовая летальность пациентов, получавших антибиотики.
Затем тот же штамм обнаружился при вспышке ПТИ в Финляндии, но к тому времени пациентов с диареями до появления микробиологических результатов перестали лечить бактерицидными антибиотиками и ситуация была купирована в зародыше.
И третий громкий (для нашей страны) случай – это массовое заболевание питерских школьников в Грузии, где так же был выявлен этот штамм (пресс-релиз Роспотребнадзора по данному случаю лежит здесь).
- Кроме вышеперечисленных существуют энтеротоксические (вызывают «диарею путешественников»), энтероинвазивные (вызывают кровавую диарею) и энтеропатогенные (водянистая диарея у новорожденных) штаммы.
Когда кишечная палочка выступает внекишечным патогенном? Почти всегда, когда обнаруживается вне места своего нормального обитания.
- Заболевания мочевыводящий путей. Здесь E.coli является абсолютным лидером и играет ведущую роль в развитии:
- Острых циститов
- Пиелонефритов
- Абсцессов почек и
- Простатитов
Этот факт объясняется близким анатомическим расположением двух систем и огрехами в личной гигиене, что позволяет на этапе эмпирической терапии вышеперечисленных заболеваний сразу же назначать препараты, активные в отношении кишечной палочки.
- Заболевания желудочно-кишечного тракта:
- Диарея путешественников
- Интраабдоминальные абсцессы и перитониты, чаще всего носящие вторичный характер (прободение кишки в результате первичного заболевания, либо при дефектах оперативного вмешательства)
- Инфекции центральной нервной системы у очень ослабленных пациентов, результатом чего будет развитие менингитов. Встречается в основном у лиц старческого возраста и новорожденных. Кроме того, в случае внутрибольничного заражения менингит может развиться в результате плохой обработки рук медицинского персонала перед оперативным вмешательством или перевязками.
- Инфекции кровотока, а именно сепсис, как продолжение развития заболеваний мочевыводящих путей, ЖКТ и билиарного тракта вследствие метастазирования очага инфекции. Лечению поддается крайне тяжело, особенно если задействованы внутрибольничные штаммы, летальность чрезвычайно высокая.
- Инфекции кожи и мягких тканей как следствие раневых инфекций после вмешательств на органах брюшной полости.
- Внутрибольничные пневмонии, вызванные устойчивыми штаммами кишечной палочки, целиком связаны с дефектами ухода за пациентом и фактором чистоты, точнее ее отсутствия, рук медицинского персонала или ухаживающих родственников. Факт внутрибольничного заражения доказывается элементарно, что будет наглядно продемонстрировано в следующем разделе.
- Послеродовые (и не только) эндометриты. Вынуждены упомянуть и эту патологию, так как инфицирование кишечной палочкой встречается все чаще и чаще, а большой настороженности нет. Как результат, можно очень сильно промахнуться с антибактериальной терапией и, как следствие, прийти к экстирпации органа в виду неэффективности антибиотикотерапии. Натолкнуть на мысль может более позднее, чем обычно, поступление и более агрессивное, чем обычно течение. Дополнительный осмотр прианальной области так же может натолкнуть на вероятность развития именно такого инфицирования.
(часть вторая) Практические вопросы диагностики и лечения.
Когда мы можем заподозрить, что перед нами пациент с инфекцией, вызванной кишечной палочкой?
- Пациенты с диареей, приехавшие из отпуска и все-таки смогшие прийти на прием (диарея путешественников или энтеротоксигенные штаммы E.coli).
- Пациенты со всеми заболеваниями мочевыделительной системы, в том числе беременные, но строго с наличием симптоматики (не надо лечить бессимптомную бактериурию, иначе вырастите резистентные штаммы и создадите проблему и себе, и женщине, и роддому в последующем).
- В стационарах – нозокомиальные пневмонии, послеоперационные менингиты, перитониты, сепсисы и т. д., носящие вторичный характер.
Подтвердить или полностью исключить кишечную палочку из возбудителей может только микробиологическое исследование. Конечно, в современных условиях микробиология уже становится практически эксклюзивом, но мы пришли учиться, а учится надо на правильных примерах, поэтому далее будет рассмотрен ряд антибиотикограмм, выполненных автоматизированными системами тестирования. Вдруг вам повезет, и в вашем лечебном учреждении все уже есть или в ближайшее время будет, а вы уже умеете с этим всем работать?
Если вы читаете данный цикл по порядку, то в базовом разделе по микробиологии был выложен ряд антибиотикограмм некоего микроорганизма в контексте нарастания антибиотикорезистентности, и это была наша сегодняшняя героиня – кишечная палочка.
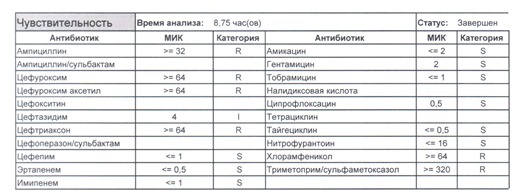
- Начнем с дикого и крайне симпатичного штамма E.coli, который живет в кишечнике и обеспечивает синтез витамина К. С ним сталкиваются доктора амбулаторной службы у пациентов с инфекциями мочевыводящих путей или в случае госпитализации у пациентов, которые не получали антибиотики около года. И именно такую чувствительность мы имеем в виду, когда назначаем эмпирическую антибиотикотерапию
Чем лечим?
- Как видите, зверь чувствителен абсолютно ко всему, и это как раз тот случай, когда можно свободно пользоваться табличными материалами справочников или клинических рекомендаций, так как механизмы резистентности полностью отсутствуют.
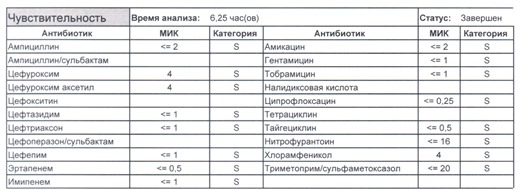
- Если в ваши руки попал пациент, которого в течение последнего полугодия лечили антибиотиками пенициллинового ряда, то антибиотикограмма может выглядеть следующим образом.
Если такая кишечная палочка окажется внекишечным патогенном, и перед вами будет беременная и ИМП (самый частый случай), то нам необходимо преодолеть резистентность к пенициллинам, то есть подавить деятельность пенициллиназ. Соответственно высокую эффективность продемонстрируют препараты с ингибиторами бета-лактамаз, чаще всего амоксициллина/клавуланат, как наиболее безопасный и эффективный. Единственное, пациентку необходимо предупредить, что в результате стимуляции рецепторов кишечника может развиться антибиотик-ассоциированная диарея.
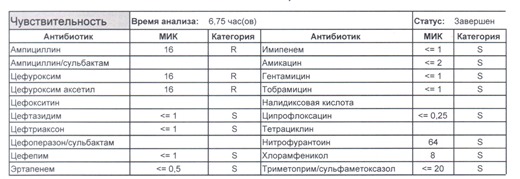
- Отдельно хотелось бы обратить внимание на следующий штамм E.coli, как типичного обладателя бета-лактамаз расширенного спектра. И эти БЛРС чаще всего вырабатываются в результате неуемного использования цефалоспоринов третьего поколения и совершенно конкретного его представителя – цефтриаксона.

В каких ситуациях мы можем увидеть (или подумать) о таком звере:
- Пациент сам рассказывает, что получал цефтриаксон в промежутке полугодия
- Пациент был переведен из другого стационара (хотя там можно будет и следующую картинку обнаружить)
- Пациент ничего не получал, и вообще в больнице не лежал, но возбудитель попал с рук медицинского персонала, вызвав внутрибольничную инфекцию
- И самый простой случай – посев был взят в момент проведения терапии цефтриаксоном
Что делать?
- Помнить, что перед вами пациент – носитель возбудителя, который может быть перенесен и создаст серьезную опасность жизни более слабому. Поэтому и персонал, и сам пациент, должны неукоснительно соблюдать санитарные правила для недопущения переноса.
- Чем лечить? Так как ни один ингибитор бета-лактамаз тут уже не работает, БЛРС отлично их разрушают, то выбор будет невелик, и лучше, чтобы этот выбор делал специально-обученный специалист – врач-клинический фармаколог, так как в данной ситуации важную роль играют не только данные о чувствительности и резистентности, но и МПК возбудителя, например. Не говоря уже о факторе фармакодинамики и самом очаге локализации инфекции.
- Если клин. фарма нет или он не специально обученный – тогда лечим в соответствии с клиническими рекомендациями по соответствующей нозологии из раздела «препараты резерва». Не лишним будет обсудить ситуацию с врачом-бактериологом клинической лаборатории, делающей для вас посевы.
- Один из самых плохих вариантов, который вы можете увидеть
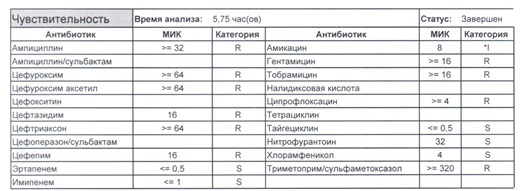
Подобный пациент не придет к вам своими ногами, его не увидит амбулаторная служба, это абсолютно стационарные больные, и если их привезут, то только из другого лечебного учреждения. Чаще всего это пациенты палат интенсивной терапии или реанимации, и такой возбудитель носит на 100% нозокомиальный характер.
Когда можем его обнаружить:
- вторичные перитониты,
- нозокомиальные пневмонии,
- пиелонефриты,
- послеоперационные менингиты,
- сепсис и т. п.
И всегда это будет ятрогенное поражение как следствие неправильной гигиены рук персонала либо обработки инструментария. Можно возразить «но как же тяжелые перитониты?». Отвечу тем, что для тяжелых перитонитов без дефектов ухода наиболее характерен штамм на третьем рисунке, так как для того, чтобы вырастить такую зверюгу, тяжелому перитониту здоровья не хватит, он от осложнений погибнуть успеет, а сама кишечная палочка ножками ходить не умеет, мы ее исключительно неправильно мытыми ручками разносим, и доказать это элементарно, так как точно такие же штаммы будут высеваться при плановых проверках эпидемиологической службы.
Что делать?
- Для эрадикации такого возбудителя нужен не просто отдельный обученный специалист и имеющая весь набор препаратов резерва аптека, но и напряженная работа эпидемиологической службы, так как подобный пациент должен быть изолирован в отдельную палату, а лучше изолятор (не подумайте, что бред – при правильной организации такие вещи вполне реальны) с проведением карантинных мероприятий, так как основная проблема появления подобного рода возбудителей в том, что они очень быстро разбегаются по всему корпусу (или стационару, если корпуса не изолированы) и обсеменяют все и вся, нанося вред другим ослабленным тяжелой болезнью пациентам и заселяя кишечники всего медицинского персонала.
- И еще одно крайне мерзкое свойство таких возбудителей – они умеют осуществлять горизонтальный перенос механизмов резистентности с другой флорой семейства Enterobacteriaceae, и даже если вы избавились от E.coli, неприятным сюрпризом может стать ее подруга клебсиелла, наносящая еще больший вред и по сути добивающая больного. Избавится полностью от этих возбудителей невозможно, для этого надо избавится от медицинского персонала как основных носителей, но контролировать можно – мероприятия подробно расписаны в действующих СанПиН 2.1.3.2630-10. Так что в случае выявления подобного возбудителя речь пойдет не только о лечении того пациента, у которого он обнаружен, но и проведения мероприятий по недопущению инфицирования всех остальных пациентов (а это, напомню, почти всегда ПИТ или ОРИТ), находящихся рядом.
- И в заключение необходимо упомянуть о панрезистентной E.coli, вооруженной полным спектром механизмов резистентности. В антибиотикограмме будут тотальные R, а МПК возбудителей пробьют все возможные потолки. К счастью для автора, она с таким зверем пока не сталкивалась, что связано с наличием работающей системы эпиднадзора, поэтому картинки не будет, хотя ее несложно представить. Такие пациенты, если кишечная палочка окажется патогеном, а не колонизатором (мало ли с чьих рук, например, в рану упала), к сожалению, почти не выживают, так как изначально являются крайне тяжелыми соматически, а кишечная палочка обычно подводит черту к их существования на бренной земле.
Что делать?
- Не допускать развития такой, не побоюсь этого слова, зверюги в ваших стационарах, а если появилась – гонять эпидемиологическую службу, чтобы избавляла руки и поверхности от такого рода заражения, что возможно только при условии наличия достаточного количества расходных материалов, перчаток и дезинфицирующих средств.
А теперь подведем небольшой итог нашего непростого разговора:
- Кишечная палочка – возбудитель очень серьезный и не следует его недооценивать. В ее типах также необходимо четко ориентироваться.
- В первую очередь о ней мы думаем при лечении инфекций мочевыводящих путей, особенно у беременных.
- Если перед нами пациент с признаками кишечной инфекции, то подход к терапии антибиотиками должен быть сугубо индивидуальным, и если состояние позволяет, то до получения микробиологии – вообще без антибиотиков. Если не позволяет – это должны быть бактериостатики.
- Мы никогда не лечим только анализ, и даже микробиологическое заключение, мы всегда лечим пациента со всем комплексом его симптомов и синдромов. Но микробиология помогает решить как дифференциально-диагностические задачи, что и позволяет отделить безусловный патоген от мирно живущего комменсала.
- Микробиологическая диагностика носит ключевое значение как для подтверждения самого возбудителя, так и для выбора необходимого антибиотика
- В случае выявления резистентных и панрезистентных возбудителей, помимо лечения самого пациента должна в полной мере задействоваться эпидемиологическая служба лечебного учреждения
Резюмируя вышесказанное, и как бы обидно это ни прозвучало, но почти всегда инфекции, вызванные кишечной палочкой, – это «болезни грязных рук» и показатель микробиологического неблагополучия. И одна из серьезных проблем медико-профилактических служб, так как при всем желании они не смогут полностью изъять источник инфицирования, так как он в прямом смысле находится во всех нас, и только соблюдение санитарных правил и санпросвет. работа могут значительно поспособствовать в сдерживании развития вышеуказанных заболеваний.
Вас может заинтересовать
Острый синусит
Острый фарингит
Студент колледжа с измененным психическим статусом
Антибиотикотерапия при эпидуральных абсцессах
Clostridium difficile
Источник
Содержание:
Сепсис — это гнойно-септическое инфекционное заболевание, поражающее кровь. Патология сопровождается распространением инфекции по всему организму и очень тяжело протекает, создавая угрозу жизни больного человека. Чаще всего возбудителями сепсиса выступают стафилококки, кишечная палочка, стрептококки, пневмококки. Сепсис зачастую развивается вследствие неблагоприятного течения гнойного воспаления мягких тканей (абсцесс, перитонит), на фоне ослабления защитных сил организма.
Что может способствовать развитию сепсиса?
- Несоблюдение правил асептики и антисептики во время обработки гнойных ран, при оперативных вмешательствах.
- Неправильный подбор лекарственных средств, ошибка с назначением дозировки антибактериальных препаратов.
- Иммунологические расстройства.
- Прогрессирование инфекционных возбудителей, устойчивых к антибиотикам.
Симптомы сепсиса
Клиническая картина при сепсисе зависит от характера возбудителя, спровоцировавшего развитие болезни. Нередко встречается сочетанная форма патологии, в основе которой лежит активное размножение сразу нескольких возбудителей.
Самым опасным по праву считают стафилококковый сепсис, который отличается высокой антибиотикоустойчивостью. Если заболевание вызывает кишечная палочка, то в очаге воспаления формируется гной. При этом область поражения не имеет четких форм.
Сепсис может иметь различные проявления. Течение болезни чаще всего бурное и стремительное, поэтому лечение необходимо начинать как можно раньше, пока не наступили необратимые для организма последствия. В последнее время выявляется сепсис со стертой симптоматикой или атипичные формы инфекционного процесса.
Основные признаки сепсиса:
- высокая температура тела;
- увеличение лейкоцитов в крови;
- учащенное сердцебиение;
- замедление образования мочи;
- нарушение работы органов кровообращения.
Септицемия и септикопиемия
Септикопиемия — это разновидность сепсиса, при которой общие симптомы болезни сочетаются с формированием характерных гнойных абсцессов в различных органах и тканях. Больные чувствуют себя очень плохо, температура тела часто повышена до 39-40°С, сознание обычно заторможено. Основными возбудителями при септикопиемии являются стафилококк и синегнойная палочка. Септикопиемия развивается менее бурно, чем септицемия. У больных септикопиемией выявляется гнойное поражение всех жизненно важных органов (сердце, печень, почки, головной мозг).
При септикопиемии зачастую быстро развивается сердечно-легочная недостаточность. Поражение мочевыделительной системы сопровождается болевым синдромом, олигурией. Если возникает гнойный менингоэнцефалит, пациенты отмечают появление сильных головных болей, помутнение сознания, возбуждение, сменяемое резкой подавленностью и заторможенностью. Гнойные очаги подлежат срочному хирургическому удалению с проведением мощной антибактериальной терапии.
Для септицемии характерен выраженный интоксикационный синдром:
- лихорадка;
- помутнение сознания;
- боли в мышцах;
- плохое самочувствие.
Инфекционный процесс протекает стремительно. Септицемия развивается преимущественно на фоне прогрессирования стрептококковой инфекции. Вследствие развития геморрагического синдрома на коже больного возникает петехиальная сыпь, выявляются кровоизлияния и во внутренних органах. Повышается сосудистая проницаемость, возникают внутренние отеки. Селезенка резко увеличена, как и лимфатические узлы. Слизистая и кожа цианотичные (синюшные).
Диагностика сепсиса
Обследование при сепсисе назначается в соответствии с формой болезни и локализацией септического очага. Могут проводиться:
- лабораторные исследования крови (наблюдается нейтрофильный лейкоцитоз со сдвигом лейкоцитарной формулы влево, снижение гемоглобина), мочи;
- УЗИ почек, печени и других органов;
- рентгенодиагностика;
- компьютерная томография;
- ЭКГ;
- бактериоскопические исследования;
- магнито-резонансная томография.
Особенности лечения сепсиса
Сепсис — это неотложное состояние, которое требует оказания неотложной реанимационной помощи. Лечение сводится к борьбе с инфекционными возбудителями и прогрессированием осложнений, которые зачастую бывают смертельно опасны для больного. Появление симптомов развития почечной недостаточности требует проведения гемофильтрации, гемодиализа, срочного восстановления гемодинамических показателей.
Если у пациента возникают признаки сердечной недостаточности, назначают вазомоторные препараты, а также средства, которые стимулируют работу сердца. Легочная недостаточность требует применения аппарата искусственной вентиляции легких. Антибиотики назначаются пациентам с сепсисом после получения достоверных результатов бактериоскопического исследования и определения чувствительности инфекционных возбудителей.
Сепсис у новорожденных детей
Сепсис в период новорожденности — очень опасное инфекционное заболевание, возбудителями которого могут выступать различные патогенные и условно патогенные микроорганизмы. В 50% случаев заражения причина кроется в прогрессировании стафилококковой инфекции, размножении гемолитического стрептококка. Чуть реже болезнь возникает вследствие активного размножения синегнойной палочки, клебсиеллы, кишечной палочки. Иногда причина развития сепсиса у новорожденных заключается в смешанной бактериальной флоре.
Входные ворота для инфекции:
- пупочная ранка;
- поврежденная кожа, слизистые оболочки;
- мочеполовые органы;
- желудочно-кишечный тракт.
Сепсис новорожденных чаще всего развивается на фоне пиодермий, отита, энтерита, кишечной инфекции, бронхита, пневмонии, фарингита.
Кто входит в группу риска по сепсису среди новорожденных? Предрасполагающие факторы и состояния:
- гипоксия плода;
- родовые травмы;
- повреждение головы и шеи во время родов;
- продолжительная искусственная вентиляция легких;
- зондовое питание ребенка;
- катетеризация вен;
- иммунные нарушения;
- ВИЧ-инфекция;
- глубокая степень недоношенности;
- тяжелые роды;
- наследственные патологии, сопровождаемые иммунореактивностью;
- конъюнктивит;
- сложные операции, проводимые в первые недели жизни ребенка.
Способствуют развитию сепсиса в раннем детском возрасте распространенные патологии беременности. Негативно отражаются на иммунитете плода венерические и мочеполовые инфекции, сифилис, ВИЧ, хронический стоматит, кандидоз, недостаток полезных веществ в рационе питания будущей матери, переутомление женщины, кислородное голодание плода вследствие анемии и нехватки железа.
Симптомы сепсиса у новорожденных
У новорожденных чаще всего развивается септицемия. Патологический процесс начинает прогрессировать на фоне длительно мокнущей пупочной ранки, гнойников на теле, выраженного стоматита, конъюнктивита. Родителей должны насторожить предвестники болезни:
- частые срыгивания;
- покраснение пупка;
- опрелости, которые не поддаются лечению;
- выделение крови, гноя, прозрачной жидкости из пупочной ранки;
- пассивность ребенка;
- недостаточная прибавка веса;
- беспокойство новорожденного.
Характерный признак сепсиса — повышение температуры тела. Может появляться гнойничковая сыпь по всему телу. Кожа приобретает характерный землистый оттенок, слизистые могут желтеть. При сепсисе наблюдается интоксикационный синдром.
Поражаются все органы ребенка, что приводит к прогрессированию опасных заболеваний и развитию следующих нарушений:
- тахикардия, брадикардия;
- увеличение количества мочи;
- геморрагический синдром;
- пневмония;
- сбои в работе надпочечников, печени, почек;
- появление хронических гнойных очагов в костной ткани, головном мозге, легких, печени;
- абсцессы;
- гнойный артрит;
- флегмоны в органах пищеварения.
При развитии молниеносной формы сепсиса возникает септический шок, который в большинстве случаев заканчивается летально. Болезнь приводит к резкому снижению температуры тела, сопровождается сильной слабостью, вялостью, повышенной кровоточивостью, отеком легких, сердечно-сосудистыми нарушениями, острой почечной недостаточностью.
Диагностика и лечение сепсиса у детей
Диагноз «сепсис новорожденных» устанавливается по клинической картине и результатам обследования. Основным методом диагностики является сдача крови на стерильность. Также проводится бактериоскопическое исследование отделяемого из пупочной ранки, берется мазок с коньюнктивы, ротоглотки, исследуется моча на микрофлору, кал на наличие дисбактериоза, проводится ПЦР-анализ. Задача специалистов, занимающихся диагностикой, дифференцировать сепсис от пневмонии, медиастенита, энтероколита, воспаления мозговых оболочек, кандиоза, энтеровирусной инфекции.
Лечение сепсиса у детей проходит с использованием реанимационного оборудования и самых современных антибактериальных препаратов. Антибиотики вводятся непосредственно в вену ребенка — так они действуют практически мгновенно и позволяют эффективно бороться с инфекционным возбудителем.
Все имеющиеся на коже гнойные абсцессы вскрывают, обрабатывая септические очаги противовоспалительными, антимикробными составами, специальными ферментами, которые повышают местный иммунитет. Для усиления иммунной активности проводят гемосорбцию, плазмаферез. Дезинтоксикационные мероприятия позволяют снизить нагрузку с почек и печени, улучшить состояние ребенка и прогноз. Больного малыша рекомендуется кормить исключительно грудным молоком, так как оно содержит антитела и помогает скорее восстановиться после болезни.
Источник