Желудочно кишечный тракт грибок
Микозы желудочно-кишечного тракта – патологические состояния, развившиеся вследствие поражения пищеварительных органов дрожжеподобными, плесневыми, диморфными грибами. Проявляются изменением вкуса, появлением налетов на видимых слизистых, диспепсией, жидким стулом, болевыми ощущениями разной локализации. Диагностируются с помощью эзофагогастродуоденоскопии, колоноскопии, электрогастрографии, микробиологического исследования биоптата, ИФА, РИФ, ПЦР. Для лечения используют антимикотики, пробиотики, иммуномодуляторы в сочетании с комплексной терапией основного заболевания, осложнившегося грибковой инфекций.
Общие сведения
Первые упоминания о специфическом поражении слизистой ротовой полости у ослабленных больных относятся к временам Гиппократа. Детальное описание орофарингеальной формы кандидозной инфекции было впервые подготовлено германским хирургом Бернгардом Лангенбеком в 1839 году. Микозы пищеварительного тракта выявляются у 8-10% пациентов, страдающих желудочно-кишечными болезнями. У 63% больных поражение ЖКТ протекает в виде кандидо-бактериальной, кандидо-герпетической, кандидо-протозойной микст-инфекции. Увеличение частоты микотических патологий связано с эпидемией ВИЧ, ростом распространенности миконосительства, заболеваний с вторичным иммунодефицитом, успехами фармакологии, предложившей эффективные иммуносупрессорные и антибактериальные средства для ранее труднокурабельных патологий.

Микозы желудочно-кишечного тракта
Причины микозов желудочно-кишечного тракта
Возбудителями микотической инфекции органов ЖКТ становятся плесневые, дрожжеподобные, диморфные грибы, в большинстве случаев являющиеся естественными комменсалами человеческого организма. 9 из 10 микозов пищеварительного тракта провоцируется Candida albicans – условно-патогенным микроорганизмом, который высеивается у 65-70% населения. Микотический процесс также может развиться в результате размножения так называемых кандид non-albicans (С. guilliermondii, С. kefyr, С. krusei, С. tropicalis и др.). Некандидозные формы микотических желудочно-кишечных болезней, вызванные возбудителями бластомикоза, гистоплазмоза, кокцидиомикоза, криптококкоза, паракокцидиомикоза, споротрихоза, возникают при диссеминации грибов из очагов на коже, в респираторном тракте, других органах. Аспергиллез пищеварительных органов, интестинальный зигомикоз диагностируются редко, обычно – при наличии тяжелой сопутствующей патологии.
Манифестации микозов часто предшествуют другие патологические состояния, способствующие патологической активации условно-патогенной флоры за счет снижения местной защитной реакции слизистой ЖКТ, угнетения иммунных сил организма. Специалисты в сфере гастроэнтерологии и микологии выделяют следующие предпосылки к развитию желудочно-кишечного микотического заболевания:
- Физиологическая иммунная недостаточность. Естественное снижение иммунитета наблюдается у беременных, связано с необходимостью поддержания гестации. Незрелость иммунной системы характерна для новорожденных, риск инфицирования возрастает при недоношенности и наличии генитального кандидоза у матери. В пожилом возрасте отмечается инволютивное угасание защитных сил.
- Патологический иммунодефицит. Несостоятельность иммунной системы лежит в основе ВИЧ-инфекции и ее клинически выраженной формы – СПИД. Нарушения иммунитета отмечаются при дисплазии тимуса, других первичных иммунодефицитах, онкогематологических и лимфопролиферативных болезнях (лейкозах, лимфогранулематозе, неходжкинских лимфомах), сахарном диабете, голодании.
- Ятрогенные факторы. Иммунная функция угнетается при использовании кортикостероидов, цитостатиков, других химиопрепаратов у пациентов, перенесших трансплантацию органа, принимающих лечение по поводу онкопатологии, ревматоидного артрита, СКВ, гломерулонефрита, других системных болезней. Развитию микозов способствует антибактериальная терапия.
- Повреждения слизистой оболочки ЖКТ. Инвазии грибов более подвержены больные, страдающие атрофическим гастритом, ахалазией кардии, бульбитом, гастроэзофагеальной рефлюксной болезнью, дисбиозом, болезнью Крона, другой желудочно-кишечной патологией. Инфицирование облегчается при ожогах, травматизации эпителия зубными протезами, твердой пищей, интубационной трубкой.
Патогенез
Механизм развития микозов желудочно-кишечного тракта основан на нарушении баланса между реактивностью организма и факторами патогенности грибов – протеолитическими ферментами инвазии (коагулазой, каталазой, козеиназой, фосфолипазой), фибриллярными белковыми комплексами, эндотоксинами. При иммунодефиците уменьшается активность интраэпителиальных лимфоцитов, В-клеток кишечника, снижается цитотоксичность Т-клеточных элементов, нарушается секреция интерферона, фагоцитоз. В результате возбудители микозов быстро обсеменяют эпителий, легко проникают через собственную пластинку слизистой, агрегируются в пейеровых бляшках.
При травмах, химических ожогах, заболеваниях пищеварительных органов, изменениях кислотности и ферментативного состава желудочного, кишечного соков ситуация усугубляется наличием участков пораженной слизистой, замедленной регенерацией эпителиальных клеток, нарушением защитной функции естественных секретов. У пациентов, принимающих антибиотики, дополнительным патогенетическим фактором становится гибель облигатных микроорганизмов (кишечной палочки, аэробных лактобацилл, анаэробных бифидобактерий), которые являются естественными антагонистами грибов и сдерживают их неконтролируемое размножение.
Классификация
При систематизации форм микотической инфекции ЖКТ учитывают вид возбудителя, локализацию и распространенность патологического процесса. С учетом этиологии различают кандидоз, являющийся самым частым видом микозов, и редкие формы грибкового поражения (аспергиллез, криптококкоз, зигомицетоз и др.). При поражении одного отдела пищеварительного тракта говорят о фокальном микозе, при массивном распространении инфекции – об инвазивном диффузном, при отсутствии признаков инвазии – о микотическом дисбиозе. Наиболее часто используют классификацию микозов по локализации поражения, в соответствии с которой выделяют:
- Орофарингеальные поражения. В структуре микотических инфекций ЖКТ занимают первое место. Обычно встречаются у новорожденных и пациентов с иммунодефицитными состояниями (СПИД, гемобластозы).
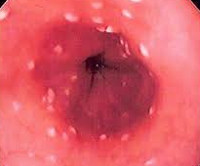
- Микотический эзофагит. Диагностируется у 1-7% больных. Чаще развивается при сниженном иммунитете. Может протекать как в поверхностной, так и в эрозивной форме с повышенной кровоточивостью.
- Микотические поражения желудка. Составляют до 5,2% микозов ЖКТ. Выявляются при гастродуоденальных язвах, хронических гастритах. В ряде случаев определяются ассоциации грибов и хеликобактера.
- Микозы кишечника. Обычно возникают на фоне микотического поражения верхних отделов пищеварительного тракта. Как правило, диагностируются у больных, получающих массивную антибиотикотерапию.
- Микотическая инфекция гепатобилиарной системы. Осложняет дискинезию желчных путей, холестаз, холецистолитиаз, лямблиоз. Диагностируется редко, в том числе из-за низкой настороженности.
Симптомы микозов ЖКТ
Клиническая картина заболевания различна в зависимости от распространенности поражения. При орофарингеальной локализации микоза у пациента возникают боли во время приема пищи, неприятный привкус во рту, на слизистой оболочке щек и языка появляются белые налеты. Поражение пищевода и желудка характеризуется болью при глотании, дисфагией, изжогой, отрыжкой, тошнотой и рвотой, дискомфортом в эпигастральной области, снижением аппетита. При прогрессировании заболевания в процесс вовлекаются нижележащие отделы желудочно-кишечного тракта, что клинически проявляется диареей с примесями слизи и крови, болезненностью в левой подвздошной области. Возможны нарушения общего состояния: субфебрильная температура тела, слабость, снижение трудоспособности, резкое уменьшение веса.
Осложнения
Вследствие проникновения микроорганизмов из пищеварительного тракта в забрюшинную клетчатку могут возникать гнойно-воспалительные процессы – парапроктит, паранефрит, межкишечные или поддиафрагмальные абсцессы. У пациентов со сниженной реактивностью организма имеется склонность к генерализации микозов с развитием септицемии, приводящей к распространению грибков на другие органы. Наиболее опасно микотическое поражение гепатобилиарной системы, которое может вызывать желтуху и печеночную недостаточность. При тяжелом течении заболевания формируются некрозы стенки кишечника, иногда – с перфорацией. Возможны профузные желудочно-кишечные кровотечения, пенетрация язв в соседние органы.
Диагностика
Постановка диагноза микозов желудочно-кишечного тракта затруднена из-за полиморфности и неспецифичности клинической картины заболевания, которая сходна с проявлениями других патологий пищеварительной системы. Для диагностики грибкового поражения требуется комплексное обследование пациента. Наиболее информативными являются следующие методы:
- Эзофагогастродуоденоскопия. Характерные признаки микозов при эндоскопии – гиперемия, выраженная отечность и контактная ранимость слизистой оболочки, наличие белесоватого налета, язвенных дефектов. Во время исследования производится забор материала (налетов, биоптатов) для гистологического и цитологического анализа.
- Колоноскопия. Введение гибкого эндоскопа в толстую кишку позволяет оценить состояние кишечного эпителия, обнаружить эрозии или язвы слизистой, которые могут быть источником желудочно-интестинальных кровотечений, провести биопсию пораженных участков. Метод используется для дифференцировки микозов с другими патологиями толстой кишки.
- Электрогастрография. Регистрация биопотенциалов применяется для оценки моторно-эвакуаторной функции желудка, которая зачастую снижена при грибковых поражениях, что создает благоприятные условия для размножения микроорганизмов. Для изучения гастродуоденальной моторики также может назначаться сцинтиграфия.
- Микробиологическое исследование биоптата. Окраска материала по Граму, Романовскому-Гимзе позволяет определить грибки в материале, что подтверждает диагноз микоза. Выявление активной вегетации и формирования мицелия свидетельствует об остром процессе. Широко используется культурологическое исследование на среде Сабуро.
- Серологические реакции. Проведение реакций агглютинации, связывания комплемента, преципитации помогает обнаружить в крови пациента специфические противогрибковые антитела. ИФА повторяется через 10-15 дней для оценки количества антител в динамике – нарастание титра в 4 раза и более дает возможность верифицировать диагноз микоза.
В клиническом анализе крови наблюдаются неспецифические признаки воспалительного процесса: повышение СОЭ, незначительный лейкоцитоз, может выявляться снижение уровня эритроцитов и гемоглобина, что обусловлено кровотечениями. Для исследования структуры всех слоев стенки пищеварительного тракта выполняется эндоскопическая ультрасонография. Дифференциальная диагностика осуществляется с воспалительными заболеваниями кишечника (терминальным илеитом, неспецифическим язвенным колитом), злокачественными новообразованиями, псевдомембранозным энтероколитом, желудочно-кишечным туберкулезом. Помимо осмотра гастроэнтеролога пациенту могут потребоваться консультации инфекциониста, онколога, фтизиатра.
Лечение микозов ЖКТ
Основными задачами являются терапия расстройства, вызвавшего активацию микотической флоры, и этиопатогенетическое воздействие на возбудителя грибковой инфекции. Лечение болезней пищеварительного тракта, иммунодефицитных и других патологических состояний проводят по протоколам соответствующих заболеваний. Для подавления грибкового процесса используют:
- Антимикотики. По результатам наблюдений, наиболее эффективной является терапия триазолами. Средства этой группы угнетают систему цитохрома P-450 и синтез эргостерола клеточных мембран, нарушая рост и репликацию кандид и криптококков. В качестве альтернативы с учетом особенностей возбудителя могут применяться полиены, аллиламины, эхинокандины.
- Пробиотики. Препараты, в которых содержатся непатогенные и нетоксигенные микроорганизмы, позволяют восполнить естественную микрофлору кишечника, нормализовать ее состав после проведенной антибактериальной терапии. Апатогенные бактерии стимулируют кишечный иммунитет, оказывают антагонистический эффект по отношению к грибам, нарушают их адгезию к слизистым.
При отсутствии противопоказаний проводится неспецифическая иммунотерапия стимуляторами естественного иммунитета (высокополимерные полисахаридные комплексы, регенеранты, производные пиримидина), Т- и В-лимфоцитов (полипептидные экстракты вилочковой железы, культур клеток костного мозга, селезенки). Возможно дополнительное использование растительных иммуномодуляторов, витаминно-минеральных комплексов.
Прогноз и профилактика
Исход болезни зависит от степени повреждения пищеварительных органов, состояния иммунной системы пациента, своевременности диагностики и терапии. Прогноз сомнительный при генерализации процесса и наличии тяжелых сопутствующих заболеваний. Для предупреждения развития микозов необходимо не допускать неоправданного применения антибактериальных средств, назначать профилактические курсы противогрибковых препаратов при длительном лечении цитостатиками, кортикостероидами, другими медикаментами с иммунодепрессорным эффектом, осуществлять диспансерное наблюдение за пациентами с иммунодефицитом.
Источник
О том, что такое кандидоз половых органов, знает практически каждая женщина. Однако мало кто знает, что этот грибок также может поражать и желудочно-кишечный тракт, что существенно влияет на его работу. Заболевание славится своими совершенно различными клиническими формами, которые могут с легкостью маскироваться под другие недуги. Лечение кандидоза – длительный и крайне ответственный процесс: пациенту придется не только принимать необходимые медикаментозные средства, но и пересмотреть свой образ жизни и заняться укреплением иммунитета. MedMe попытался разобраться, как же правильно бороться с грибком.
Кандидоз кишечника: почему развивается болезнь?
Кишечный кандидоз представляет собой инфекционное заболевание грибковой природы, поражающее слизистые оболочки желудочно-кишечного тракта. Эта патология – одна из важнейших проблем современной гастроэнтерологии: довольно сложно вовремя определить природу недуга. Это связано с повсеместной распространенностью возбудителя – грибка рода Candida, который также является компонентом микрофлоры организма совершенно здорового человека (около 80% населения – бессимптомные носители).
Медики выделяют две основные формы грибковой инфекции: инвазивную и неинвазивную. Чаще всего встречается первая форма недуга: она развивается на фоне дисбактериоза и перенесенного инфекционного заболевания, поражающего желудочно-кишечный так. Грибки Candida начинают активно размножаться в просвете кишечника, но не проникают в слизистую оболочку. При этом выделяется большое количество токсичных продуктов обмена, которые оказывают раздражающее воздействие на кишечник. Они провоцируют дальнейшее прогрессирование дисбактериоза, а также способствуют формированию аллергических реакций.
Инвазивный кандидоз развивается по совершенно другому механизму. На фоне ослабленного иммунитета грибки плотно прикрепляются к кишечному эпителию, после чего проникают глубоко в его толщу. Нередко происходит распространение Candida по системному кровотоку, в результате чего поражаются другие органы и ткани (печень, поджелудочная железа). Вероятность развития недуга увеличивают следующие факторы:
- беременность;
- пожилой или молодой возраст;
- онкологические заболевания;
- курс антибактериальной, кортикостероидной или лучевой терапии;
- эндокринные патологии;
- врожденные и приобретенные иммунодефицитные состояния.
Как проявляется грибковая инфекция?
На сегодняшний день принято различать три основных разновидности кандидоза: неинвазивный, инвазивный диффузный и фокальный. Неинвазивная форма заболевания является самой распространенной. Для нее характерно довольно легкое течение: умеренное повышение температуры тела, неустойчивый стул, избыточное газообразование, а также незначительный дискомфорт в животе. На фоне недуга нередко происходит обострение аллергических заболеваний.
Инвазивная диффузная грибковая инфекция характеризуется крайне тяжелым состоянием больного. Интоксикация нарастает очень быстро: повышается температура тела, возникает резкая слабость, падает артериальное давление. Пациенты отмечают появление сильных болей в животе, диареи с примесью крови, постоянную тошноту и рвоту. Этот тип грибкового поражения чаще всего встречается у людей с иммуносупрессивными состояниями.
Инвазивная фокальная форма заболевания нередко осложняет течение язвенной болезни или язвенного колита. В этом случае возникает локальное поражение слизистой оболочки в области язвенного дефекта: там начинает активно расти и размножаться грибок. В этом случае симптомы не отличаются от обычных проявлений болезни.
Питание при кишечном кандидозе: на что стоит обратить внимание?
Одним из важных элементов в лечении заболевания является диета. Кандидоз требует от пациента серьезно пересмотреть питание: без этого выздоровление затянется надолго. Прежде всего, больному следует отказаться от тех продуктов, которые дают грибкам пищу для дальнейшего роста и размножения. В эту группу входят все сладости и сладкие напитки (соки, газировки), любой алкоголь, жирные и жареные блюда, а также грибы. Пациенту советуют обратить свое внимание на мясо птицы, красную рыбу, каши, некрахмалистые овощи. Фрукты и ягоды стоит употреблять ограничено: они также являются источником сахаров.
Стоит отметить, что питание должно быть дробным. Небольшие порции, получаемые 5-6 раз в день, усваиваются гораздо лучше. Все блюда стоит тушить, отваривать или запекать. От соли, специй и острых соусов лучше отказаться. Также больным не стоит забывать про соблюдение питьевого режима.
Лечение кандидоза кишечника
В большинстве случаев лечение кандидоза проводится амбулаторно, но при тяжелом состоянии пациента показана госпитализация в стационар. Основу терапии составляют антимикотические препараты, которые нарушают жизненный цикл грибка и препятствуют его развитию. Чаще всего с этой целью используют кетоконазол, итраконазол и флуконазол, а также амфотерицин B. Эти препараты активно всасываются из кишечника и обладают системным действием.
Неинвазивный кандидоз лечат с использованием нерезорбтивных полимикотиков, которые плохо всасываются слизистой оболочкой. К ним относят натамицин и нистатин. Также лечение кандидоза направлено на восстановление состава нормальной кишечной микрофлоры: с этой целью назначают пробиотики и пребиотики. После проведенного курса терапии больному показано укрепление иммунитета с помощью физиопроцедур и иммуностимуляторов.
Источник